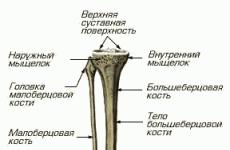
Функциональные нарушения желудочно-кишечного тракта у детей грудного возраста: роль диетотерапии. Функциональные нарушения ЖКТ у детей. Современные методы коррекции Функциональные абдоминальные боли
Традиционно нарушения, возникающие в любой системе человеческого организма, подразделяют на органические и функциональные. Органическая патология связана с повреждением структуры органа, степень выраженности которой может колебаться в самых широких пределах от грубой аномалии развития до минимальной энзимопатии. Если органическая патология исключается, то можно говорить о функциональных нарушениях (ФН). Функциональные нарушения — это симптомы физических недомоганий, вызванные не заболеваниями органов, а нарушениями их функций.
Функциональные нарушения со стороны желудочно-кишечного тракта (ФН ЖКТ) — одна из самых распространенных проблем, особенно среди детей первых месяцев жизни. По данным различных авторов, ФН ЖКТ сопровождают от 55% до 75% младенцев этой возрастной группы .
По определению D. A. Drossman (1994), функциональные нарушения пищеварения представляют собой «разнообразную комбинацию гастроинтестинальных симптомов без структурных или биохимических нарушений» функции самого органа .
С учетом данного определения, диагностика ФН зависит от уровня наших знаний и возможностей методов исследования, которые позволяют выявить у ребенка те или иные структурные (анатомические) нарушения и тем самым исключить их функциональный характер.
В соответствии с Римскими критериями III, предложенными Комитетом по изучению функциональных расстройств у детей и Международной рабочей группой по разработке критериев функциональных расстройств (2006), к ФН ЖКТ у младенцев и детей второго года жизни относят:
- G1. Синдром срыгивания;
- G2. Синдром руминации;
- G3. Синдром циклической рвоты;
- G4. Младенческие кишечные колики;
- G5. Синдром функциональной диареи;
- G6. Болезненность и затруднения при дефекации (дисхезия);
- G7. Функциональный запор.
Из представленных синдромов наиболее часто встречаются такие состояния, как срыгивание (23,1% случаев), младенческие кишечные колики (20,5% случаев) и функциональный запор (17,6% случаев). Наиболее часто данные синдромы наблюдаются в различных комбинациях, реже — как один изолированный синдром .
В клинической работе, выполненной под руководством профессора Е. М. Булатовой, посвященной изучению частоты встречаемости и причин развития ФН пищеварения у младенцев первых месяцев жизни, отмечена такая же тенденция. На амбулаторном приеме у врача-педиатра родители часто предъявляли жалобы на то, что их ребенок срыгивает (57% случаев), беспокоится, сучит ножками, у него отмечается вздутие живота, схваткообразные боли, крик, то есть эпизоды кишечных колик (49% случаев). Несколько реже были жалобы на жидкий стул (31% случаев) и затруднение дефекации (34% случаев). Следует отметить, что основная часть младенцев с затрудненной дефекацией страдала синдромом младенческой дисхезии (26%) и только в 8% случаев — запором. Наличие двух и более синдромов ФН пищеварения было зафиксировано в 62% случаев.
В основе развития ФН ЖКТ можно выделить ряд причин, как со стороны ребенка, так и со стороны матери. К причинам со стороны ребенка относят:
- перенесенную анте- и перинатальную хроническую гипоксию;
- морфологическую и (или) функциональную незрелость ЖКТ;
- более поздний старт развития вегетативной, иммунной и ферментных систем пищеварительной трубки, особенно тех ферментов, которые ответственны за гидролиз белков, липидов, дисахаридов;
- несоответствующее возрасту питание;
- нарушение техники вскармливания;
- насильственное кормление;
- недостаток или избыток питья и т. д.
Со стороны матери основными причинами развития ФН ЖКТ у ребенка являются:
- повышенный уровень тревожности;
- гормональная перестройка в организме кормящей женщины;
- асоциальные условия жизни;
- серьезные нарушения режима дня и питания.
Отмечено, что ФН ЖКТ значительно чаще встречаются у первенцев, долгожданных детей, а также у детей пожилых родителей .
Причины, лежащие в основе развития функциональных нарушений ЖКТ, оказывают влияние на моторную, секреторную и всасывающую способность пищеварительной трубки и негативно сказываются на формировании микробиоценоза кишечника и иммунного ответа.
Изменения микробного баланса характеризуются индуцированием роста условно-патогенной протеолитической микробиоты, продукцией патологических метаболитов (изоформы короткоцепочечных жирных кислот (КЦЖК)) и токсичных газов (метан, аммиак, серосодержащие), а также развитием у малыша висцеральной гиперальгезии, которая проявляется выраженным беспокойством, плачем и криком. Такое состояние обусловлено сформированной еще антенатально ноцицептивной системой и низкой активностью антиноцицептивной системы, которая начинает активно функционировать после третьего месяца постнатальной жизни малыша .
Избыточный бактериальный рост условно-патогенной протеолитической микробиоты стимулирует синтез нейротрансмиттеров и гастроинтестинальных гормонов (мотилина, серотонина, мелатонина), меняющих моторику пищеварительной трубки по гипо- или гиперкинетическому типу, вызывая спазм не только пилорического сфинктера и сфинктера Одди, но и анального сфинктера, а также развитие метеоризма, кишечных колик и нарушения дефекации.
Адгезия условно-патогенной флоры сопровождается развитием воспалительной реакции слизистой оболочки кишки, маркером которой является высокий уровень белка кальпротектина в копрофильтрате. При младенческих кишечных коликах, некротическом энтероколите его уровень резко возрастает по сравнению с возрастной нормой .
Связь воспаления и кинетики кишки осуществляется на уровне взаимодействия иммунной и нервной системы кишечника, причем эта связь двунаправленная. Лимфоциты собственной пластинки кишки обладают рядом нейропептидных рецепторов. Когда иммунные клетки в процессе воспаления высвобождают активные молекулы и медиаторы воспаления (простагландины, цитокины), то энтеральные нейроны экспрессируют рецепторы для этих иммунных медиаторов (цитокинов, гистамина) рецепторы, активируемые протеазами (protease-activated receptors, PARs) и др. Обнаружено, что толл-подобные рецепторы, распознающие липополисахариды грамотрицательных бактерий, представлены не только в подслизистом и мышечном сплетении ЖКТ, но и в нейронах задних рогов спинного мозга. Таким образом, энтеральные нейроны могут отвечать как на воспалительные стимулы, так и непосредственно быть активированы бактериальными и вирусными компонентами, участвуя в процессе взаимодействия организма с микробиотой .
Научная работа финских авторов, выполненная под руководством A. Lyra (2010), демонстрирует аберрантное формирование кишечной микробиоты при функциональных нарушениях пищеварения, так, микробиоценоз при синдроме раздраженной кишки характеризуется сниженным уровнем Lactobacillus spp. , повышением титра Cl. difficile и клостридий XIV кластера, обильным ростом аэробов: Staphylococcus, Klebsiella, E. coli и нестабильностью микробиоценоза при динамической его оценке .
В клиническом исследовании профессора Е. М. Булатовой, посвященном изучению видового состава бифидобактерий у младенцев, находящихся на разных видах вскармливания, автор показала, что видовое разнообразие бифидобактерий можно рассматривать как один из критериев нормальной моторной функции кишки. Отмечено, что у детей первых месяцев жизни без ФН (вне зависимости от вида вскармливания) видовой состав бифидобактерий достоверно чаще представлен тремя и более видами (70,6%, против 35% случаев), с доминированием младенческих видов бифидобактерий (B. bifidum и B. longum, bv. infantis ). Видовой состав бифидобактерий младенцев с ФН ЖКТ преимущественно был представлен взрослым видом бифидобактерий — B. adolescentis (p < 0,014) .
ФН пищеварения, возникшие в первые месяцы жизни малыша, без свое-временного и правильного лечения, могут сохраняться на протяжении всего периода раннего детства, сопровождаться существенным изменением в состоянии здоровья, а также иметь отдаленные негативные последствия.
У детей с синдромом упорных срыгиваний (оценка от 3 до 5 баллов) отмечаются отставание в физическом развитии, заболевания ЛОР-органов (средние отиты, хронический или рецидивирующий стридор, ларингоспазм, хронические синуситы, ларингиты, стенозы гортани), железодефицитная анемия. В возрасте 2-3 лет эти дети имеют более высокую частоту респираторных заболеваний, беспокойный сон и повышенную возбудимость. К школьному возрасту у них нередко формируется рефлюкс-эзофагит .
B. D. Gold (2006) и S. R. Orenstein (2006) отметили, что дети, страдающие в первые два года жизни патологическими срыгиваниями, составляют группу риска по развитию у них хронического гастродуоденита, ассоциированного с Helicobacter pylori , формированию гастроэзофагеальной рефлюксной болезни, а также пищевода Барретта и/или эзофагеальной аденокарциномы в более старшем возрасте .
В работах P. Rautava, L. Lehtonen (1995) и M. Wake (2006) показано, что младенцы, пережившие кишечные колики в первые месяцы жизни, в последующие 2-3 года жизни страдают нарушением сна, которое проявляется в трудности засыпания и частых ночных пробуждениях . В школьном возрасте эти дети значительно чаще, чем в общей популяции, проявляют приступы гнева, раздражения, плохого настроения во время еды ; имеют снижение общего и вербального коэффициента интеллектуального развития , пограничную гиперактивность и нарушения поведения . Кроме того, у них чаще отмечаются аллергические заболевания и абдоминальные боли, которые в 35% случаев носят функциональный характер, а 65% требуют стационарного лечения .
Последствия нелеченных функциональных запоров зачастую трагичны. Нерегулярное, редкое опорожнение кишечника лежит в основе синдрома хронической интоксикации, сенсибилизации организма и может служить предиктором колоректальной карциномы .
Для предупреждения таких серьезных осложнений детям с ФН ЖКТ необходимо оказывать своевременную помощь и в полном объеме.
Лечение ФН ЖКТ включает разъяснительную работу с родителями и их психологическую поддержку; использование позиционной (постуральной) терапии; лечебный массаж, упражнения, музыко-, арома- и аэроионотерапию; при необходимости назначение медикаментозной патогенетической и посиндромной терапии и, конечно же, диетотерапию.
Основная задача диетотерапии при ФН — координация двигательной активности ЖКТ и нормализация микробиоценоза кишечника.
Решить данную задачу возможно путем введения в рацион ребенка продуктов функционального питания.
Согласно современным воззрениям, функциональными называют продукты, которые за счет их обогащения витаминами, витаминоподобными соединениями, минералами, про- и (или) пребиотиками, а также другими ценными пищевыми веществами приобретают новые свойства — благоприятно влиять на различные функции организма, улучшая не только состояние здоровья человека, но и предупреждая развитие различных заболеваний .
Впервые о функциональном питании заговорили в Японии, в 1980-х гг.. Впоследствии это направление получило широкое распространение в других развитых странах. Отмечено, что 60% всех функциональных продуктов питания, особенно обогащенных про- или пребиотиками, направлены на оздоровление кишечника и иммунной системы .
Новейшие исследования по изучению биохимического и иммунологического состава грудного молока, а также лонгитудинальные наблюдения за состоянием здоровья детей, получавших грудное молоко, позволяют считать его продуктом функционального питания.
С учетом имеющихся знаний, производители детского питания для детей, лишенных грудного молока, выпускают адаптированные молочные смеси, а для детей старше 4-6 месяцев — продукты прикорма, которые можно отнести к продуктам функционального питания, поскольку введение в состав этих продуктов витаминов, витаминоподобных и минеральных соединений, полиненасыщенных жирных кислот, а именно докозагексаеновой и арахидоновой, а также про- и пребиотиков придают им функциональные свойства.
Про- и пребиотики хорошо изучены и широко используются как у детей, так и у взрослых для профилактики таких состояний и заболеваний, как аллергия, синдром раздраженного кишечника, метаболический синдром, хронические воспалительные заболевания кишечника, снижение минеральной плотности костной ткани, химически индуцированные опухоли кишечника .
Пробиотики — апатогенные живые микроорганизмы, которые при употреблении в достаточном количестве оказывают прямое положительное воздействие на состояние здоровья или физиологию организма-хозяина . Из всех изученных и производимых промышленностью пробиотиков подавляющее большинство относится к бифидобактериям и лактобациллам.
Сущность «пребиотической концепции», которая впервые была представлена G. R. Gibson и M. B. Roberftoid (1995), направлена на изменение кишечной микробиоты под действием пищи за счет избирательной стимуляции одного или нескольких видов потенциально полезных групп бактерий (бифидо- и лактобактерий) и уменьшения численности патогенных видов микроорганизмов или их метаболитов, что существенным образом улучшает состояние здоровье пациента .
В качестве пребиотиков в питании детей грудного и раннего возраста используют инулин и олигофруктозу, которые часто объединяют под термином «фруктоолигосахариды» (ФОС), или «фруктаны» .
Инулин — полисахарид, который содержится во многих растениях (корне цикория, репчатом луке, луке порее, чесноке, топинамбуре, бананах), имеет линейное строение, с широким разбросом по длине цепи, и состоит из фруктозильных звеньев, связанных между собой β-(2-1)-гликозидной связью.
Инулин, используемый для обогащения продуктов детского питания, в промышленном масштабе получают из корней цикория путем экстракции в диффузоре. Этот процесс не изменяет молекулярную структуру и состав природного инулина.
Для получения олигофруктозы «стандартный» инулин подвергают частичному гидролизу и очистке. Частично гидролизованный инулин состоит из 2-8 мономеров, имеющих на конце молекулу глюкозы — это короткоцепочечный фруктоолигосахарид (кцФОС). Из «стандартного» инулина образуют длинноцепочечный инулин. Возможны два способа его образования: первый — ферментативное удлинение цепи (фермент фруктозидаза) путем присоединения мономеров сахарозы — «удлиненные» ФОС, второй — физическое отделение кцФОС от инулина цикория — длинноцепочечный фруктоолигосахарид (длФОС) (22 мономера с молекулой глюкозы на конце цепи).
Физиологические эффекты длФОС и кцФОС различаются. Первый подвергается бактериальному гидролизу в дистальных отделах толстой кишки, второй — в проксимальных, в результате комбинация этих составляющих обеспечивает пребиотический эффект на протяжении всего толстого кишечника. Кроме того, в процессе бактериального гидролиза синтезируются разные по составу метаболиты жирных кислот. При сбраживании длФОС образуется в основном бутират, а при сбраживании кцФОС — лактакт и пропионат .
Фруктаны являются типичными пребиотиками, поэтому практически не расщепляются α-гликозидазами кишечника, а в неизмененной форме достигают толстой кишки, где служат субстратом для сахаролитической микробиоты, не влияя на рост других групп бактерий (фузобактерии, бактероиды и др.) и подавляя рост потенциально патогенных бактерий: Clostridium perfringens, Clostridium enterococcui . То есть фруктаны, способствуя увеличению численности бифидобактерий и лактобацилл в толстом кишечнике, по-видимому, являются одной из причин адекватного формирования иммунного ответа и устойчивости организма к кишечным патогенам .
Подтверждением пребиотического эффекта ФОС служит работа E. Menne (2000), показавшая, что после прекращения приема активного ингредиента (кцФОС/длФОС) число бифидобактерий начинает убывать и состав микрофлоры постепенно возвращается к исходному состоянию, наблюдавшемуся до начала эксперимента . Отмечено, что максимальный пребиотический эффект фруктанов наблюдается для дозировок от 5 до 15 г в сутки . Определен регулирующий эффект фруктанов: для людей с исходно низким уровнем бифидобактерий характерно явное увеличение их численности под действием ФОС по сравнению с людьми, имеющими изначально более высокий уровень бифидобактерий .
Положительное влияние пребиотиков на устранение функциональных нарушений пищеварения у детей установлено в ряде исследований. Первые работы по нормализации микробиоты и моторной функции пищеварительного тракта касались адаптированных молочных смесей, обогащенных галакто- и фруктоолигосахаридами .
В последние годы доказано, что внесение в состав молочных смесей и продуктов прикорма инулина и олиго-фруктозы оказывает благоприятное действие на спектр кишечной микробиоты и улучшение процессов пищеварения.
В мультицентровом исследовании, проведенном в 7 городах России, приняли участие 156 детей в возрасте от 1 до 4 месяцев. В основную группу вошли 94 ребенка, получавшие адаптированную молочную смесь с инулином, в группу сравнения — 62 ребенка, получавшие стандартную молочную смесь. У детей основной группы на фоне приема продукта, обогащенного инулином, было установлено достоверное увеличение количества бифидо- и лактобактерий и тенденция к снижению уровня как кишечной палочки со слабовыраженными ферментативными свойствами, так и лактозонегативной кишечной палочки .
В исследовании, выполненном в отделе детского питания НИИ питания РАМН, было показано, что ежедневный прием детьми второго полугодия жизни каши с олигофруктозой (0,4 г в одной порции) оказывает позитивное влияние на состояние микробиоты кишечника и нормализацию стула .
Примером продуктов прикорма, обогащенных пребиотиками растительного происхождения — инулином и олигофруктозой, могут служить каши транснациональной компании Heinz, вся линейка каш — низкоаллергенные, безмолочные, молочные, лакомые, «Любопышки» — содержит пребиотики.
Кроме того, пребиотик включен в состав монокомпонентного пюре из чернослива, и создана специальная линейка десертных пюре с пребиотиком и кальцием. Количество пребиотика, вносимого в продукты прикорма, широко варьируется. Это позволяет индивидуально подобрать продукт прикорма и добиться хороших результатов в профилактике и лечении функциональных нарушений у детей раннего возраста. Изучение продуктов, содержащих пребиотики, продолжается.
Литература
- Iacono G., Merolla R., D’Amico D., Bonci E., Cavataio F., Di Prima L., Scalici C., Indinnimeo L., Averna M. R., Carroccio A. Gastrointestinal symptoms in infancy: a population-based prospective study // Dig Liver Dis. 2005, Jun; 37 (6): 432-438.
- Rajindrajith S., Devanarayana N. M. Constipation in Children: Novel Insight Into Epidemiology // Pathophysiology and Management J Neurogastroenterol Motil. 2011, January; 17 (1): 35-47.
- Drossman D. А. The Functional Gastrointestinal Disorders. Diagnosis, Pathophysiology, and treatment. А Multinational Consensus. Little, brown and Company. Boston/New York/Toronto/London. 1994; 370.
- Конь И. Я., Сорвачева Т. Н. Диетотерапия функциональных нарушений органов ЖКТ у детей первого года жизни // Лечащий Врач. 2004, № 2, с. 55-59.
- Hyman P. E., Milla P. J., Bennig M. A. et al. Childhood functional gastrointestinal disorders: neonate/toddler // Am. J. Gastroenterol. 2006, v. 130 (5), p. 1519-1526.
- Gisbert J. P., McNicholl A. G. Questions and answers on the role of faecal calprotectin as a biological marker in inflammatory bowel disease // Dig Liver Dis. 2009, Jan; 41 (1): 56-66.
- Barajon I., Serrao G., Arnaboldi F., Opizzi E., Ripamonti G., Balsari A., Rumio C. Toll-like receptors 3, 4, and 7 are expressed in the enteric nervous system and dorsal root ganglia // J Histochem Cytochem. 2009, Nov; 57 (11): 1013-1023.
- Lyra A., Krogius-Kurikka L., Nikkila J., Malinen E., Kajander K., Kurikka K., Korpela R., Palva A. Effect of a multispecies probiotic supplement on quantity of irritable bowel syndrome-related intestinal microbial phylotypes // BMC Gastroenterol. 2010, Sep 19; 10: 110.
- Булатова Е. М., Волкова И. С., Нетребенко О. К. Роль пребиотиков в состоянии кишечной микробиоты у грудных детей // Педиатрия. 2008, т. 87, № 5, с. 87-92.
- Сорвачева Т. Н., Пашкевич В. В. Функциональные нарушения ЖКТ у грудных детей: методы коррекции // Лечащий Врач. 2006, № 4, с. 40-46.
- Gold B. D. Is gastroesophageal reflux disease really a life-long disease: do babies who regurgitate grow up to be adults with GERD complications? // Am J Gastroenterol. 2006, Mar; 101 (3): 641-644.
- Orenstein S. R., Shalaby T. M., Kelsey S. F., Frankel E. Natural history of infant reflux esophagitis: symptoms and morphometric histology during one year without pharmacotherapy // Am J Gastroenterol. 2006, Mar; 101 (3): 628-640.
- Rautava P., Lehtonen L., Helenius H., Sillanpaa M. Infantile colic: child and family three years later // Pediatrics. 1995, Jul; 96 (1 Pt 1): 43-47.
- Wake M., Morton-Allen E., Poulakis Z., Hiscock H., Gallagher S., Oberklaid F. Prevalence, stability, and outcomes of cry-fuss and sleep problems in the first 2 years of life: prospective community-based study // Pediatrics. 2006, Mar; 117 (3): 836-842.
- Rao M. R., Brenner R. A., Schisterman E. F., Vik T., Mills J. L. Long term cognitive development in children with prolonged crying // Arch Dis Child. 2004, Nov; 89 (11): 989-992.
- Wolke D., Rizzo P., Woods S. Persistent infant crying and hyperactivity problems in middle childhood // Pediatrics. 2002, Jun; 109 (6): 1054-1060.
- Savino F. Prospective 10-year study on children who had severe infantile colic // Acta Paediatr Suppl. 2005, Oct; 94 (449): 129-132.
- Canivet C., Jakobsson I., Hagander B. Infantile colic. Follow-up at four years of age: still more «emotional» // Acta Paediatr. 2000, Jan; 89 (1): 13-171.
- Kotake K., Koyama Y., Nasu J., Fukutomi T., Yamaguchi N. Relation of family history of cancer and environmental factors to the risk of colorectal cancer: a case-control study // Jpn J Clin Oncol. 1995, Oct; 25 (5): 195-202.
- Pool-Zobel B., van Loo J., Rowland I., Roberfroid M. B. Experimental evidences on the potential of prebiotic fructans to reduce the risk of colon cancer // Br J Nutr. 2002, May; 87, Suppl 2: S273-281.
- Шемеровский К. А. Запор — фактор риска калоректального рака // Клиническая медицина. 2005, т. 83, № 12, с. 60-64.
- Contor L., Asp N. G. Process for the assessment of scientific support for claims on foods (PASSCLAIM) phase two: moving forward // Eur J Nutr. 2004, Jun; 43 Suppl 2: II3-II6.
- Cummings J. H., Antoine J. M., Azpiroz F., Bourdet-Sicard R., Brandtzaeg P., Calder P. C., Gibson G. R., Guarner F., Isolauri E., Pannemans D., Shortt C., Tuijtelaars S., Watzl B. PASSCLAIM — gut health and immunity // Eur J Nutr. 2004 Jun; 43 Suppl 2: II118-II173.
- Bjorkstrn B. Effects of intestinal microflora and the environment on the development of asthma and allergy // Springer Semin Immunopathol. 2004, Feb; 25 (3-4): 257-270.
- Bezirtzoglou E., Stavropoulou E. Immunology and probiotic impact of the newborn and young children intestinal microflora // Anaerobe. 2011, Dec; 17 (6): 369-374.
- Guarino A., Wudy A., Basile F., Ruberto E., Buccigrossi V. Composition and roles of intestinal microbiota in children // J Matern Fetal Neonatal Med. 2012, Apr; 25 Suppl 1: 63-66.
- Jirillo E., Jirillo F., Magrone T. Healthy effects exerted by prebiotics, probiotics, and symbiotics with special reference to their impact on the immune system // Int J Vitam Nutr Res. 2012, Jun; 82 (3): 200-208.
- Food and Agriculture Organization of the United Nations and World Health Organization (FAO-WHO) (2002) Guidelines for the evaluation of probiotics in food. FAO of the United Nations and WHO working group report.
- Gibson G. R., Roberfroid M. B. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics // J Nutr. 1995, Jun; 125 (6): 1401-12.
- Rossi M., Corradini C., Amaretti A., Nicolini M., Pompei A., Zanoni S., Matteuzzi D. Fermentation of fructooligosaccharides and inulin by bifidobacteria: a comparative study of pure and fecal cultures // Appl Environ Microbiol. 2005 Oct; 71 (10): 6150-6158.
- Boehm G., Fanaro S, Jelinek J., Stahl B., Marini A. Prebiotic concept for infant nutrition // Acta Paediatr Suppl. 2003, Sep; 91 (441): 64-67.
- Fanaro S., Boehm G., Garssen J., Knol J., Mosca F., Stahl B., Vigi V. Galacto-oligosaccharides and long-chain fructo-oligosaccharides as prebiotics in infant formulas: a review // Acta Paediatr Suppl. 2005 Oct; 94 (449): 22-26.
- Menne E., Guggenbuhl N., Roberfroid M. Fn-type chicory inulin hydrolysate has a prebiotic effect in humans // J Nutr. 2000, May; 130 (5): 1197-1199.
- Bouhnik Y., Achour L., Paineau D., Riottot M., Attar A., Bornet F. Four-week short chain fructo-oligosaccharides ingestion leads to increasing fecal bifidobacteria and cholesterol excretion in healthy elderly volunteers // Nutr J. 2007, Dec 5; 6: 42.
- Euler A. R., Mitchell D. K., Kline R., Pickering L. K. Prebiotic effect of fructo-oligosaccharide supplemented term infant formula at two concentrations compared with unsupplemented formula and human milk // J Pediatr Gastroenterol Nutr. 2005, Feb; 40 (2): 157-164.
- Moro G., Minoli I., Mosca M., Fanaro S., Jelinek J., Stahl B., Boehm G. Dosage-related bifidogenic effects of galacto- and fructooligosaccharides in formula-fed term infants // J Pediatr Gastroenterol Nutr. 2002, Mar; 34 (3): 291-295.
- Savino F., Cresi F., Maccario S., Cavallo F., Dalmasso P., Fanaro S., Oggero R., Vigi V., Silvestro L. «Minor» feeding problems during the first months of life: effect of a partially hydrolysed milk formula containing fructo- and galacto-oligosaccharide // Acta Paediatr Suppl. 2003, Sep; 91 (441): 86-90.
- Конь И. Я., Куркова В. И., Абрамова Т. В., Сафронова А. И., Гультикова О. С. Результаты мультицентрового исследования клинической эффективности сухой адаптированной молочной смеси с пищевыми волокнами в питании детей первого года жизни // Вопросы практической педиатрии. 2010; 5 (2): 29-37.
- Конь И. Я., Сафронова А. И., Абрамова Т. В., Пустограев Н. Н., Куркова В. И. Каши с инулином в питании детей раннего возраста // Российский вестник перинатологии и педиатрии. 2012; 3: 106-110.
Н. М. Богданова, кандидат медицинских наук
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Функциональные заболевания пищеварительного тракта у детей. Принципы рациональной терапии
Хавкин А.И., Бельмер С.В., Волынец Г.В., Жихарева Н.С.
Функциональные нарушения (ФН) желудочно-кишечного тракта занимают одно из ведущих мест в структуре патологии органов пищеварения. Так, например, рекуррентные абдоминальные боли у детей носят функциональный характер у 90-95% детей и лишь у 5-10% связаны с органической причиной. Примерно в 20% случаев хроническая диарея у детей также обусловлена функциональными расстройствами.
В последние десятилетия, если ориентироваться на число публикаций по данному вопросу, интерес к функциональным нарушениям нарастает в геометрической прогрессии. Простой анализ числа публикаций по функциональным нарушениям, отображенных в базе данных Национальной Медицинской Библиотеки США, хорошо известной как Мedline, показал, что с 1966 по 1999 г. число статей по этой тематике за каждое десятилетие удваивалось. При этом, увеличение числа публикаций, относящихся к детскому возрасту, имело ту же тенденцию, стабильно занимая примерно одну четвертую часть от общего числа статей.
Диагностика ФН часто вызывает значительные трудности у практических врачей, приводя к большому числу ненужных обследований, а главное, к нерациональной терапии. При этом часто приходится сталкиваться не столько с незнанием проблемы, сколько с ее непониманием.
В терминологическом плане следует дифференцировать функциональные нарушения и нарушения функции, два созвучных, но несколько различных понятия, теснейшим образом связанных между собой. Нарушение функции того или иного органа может быть связано с любой причиной, в т.ч. и с органическим его повреждением. Функциональные нарушения, в этом свете, можно рассматривать как частный случай нарушения функции органа, не связанного с органическим его повреждением.
Основными физиологическими процессами (функциями), проистекающими в желудочно-кишечном тракте, являются: секреция, переваривание, всасывание, моторика, активность микрофлоры и активность иммунной системы. Соответственно, нарушениями указанных функций являются: нарушения секреции, переваривания (мальдигестия), всасывания (мальабсорбция), моторики (дискинезии), состояния микрофлоры (дисбиоз, дисбактериоз), активности иммунной системы. Все перечисленные дисфункции связаны между собой через изменение состава внутренней среды и если в начале заболевания может иметь место нарушение только одной функции, то по мере прогрессирования нарушаются и остальные. Таким образом, у больного, как правило, нарушены все функции желудочно-кишечного тракта, хотя степень этих нарушений различна.
Когда речь идет о функциональных нарушениях как нозологической единице, обычно подразумеваются нарушения моторной функции, однако вполне правомерно говорить о других функциональных нарушениях, например, связанных, с нарушениями секреции.
Согласно современным представлениям, ФН - это разнообразная комбинация гастроинтестинальных симптомов без структурных или биохимических нарушений (D.A. Drossman, 1994).
Причины функциональных нарушений лежат вне органа, функция которого нарушена, и связаны с нарушением регуляции данного органа. Наиболее изучены механизмы нарушений нервной регуляции, обусловленные либо вегетативными дисфункциями, нередко связанными с психоэмоциональными и стрессовыми факторами, либо органическим поражением центральной нервной системы и вторичной вегетативной дистонией. Гуморальные нарушения изучены в меньшей степени, но достаточно очевидны в ситуациях, когда на фоне заболевания одного органа, развивается дисфункция соседних: например, дискинезия желчевыводяших путей при язвенной болезни двенадцатиперстной кишки. Хорошо изучены нарушения моторики при ряде эндокринных заболеваний, в частности, при нарушениях со стороны щитовидной железы.
В 1999 году Комитетом по изучению функциональных расстройств у детей и Международной рабочей группой по разработке критериев функциональных расстройств (Римская группа II), совместно с сотрудниками клиники Монреальского Университета (Committee on Childhood Functional Gastrointestinal Disorders, Multinational Working Teams to Develop Criteria for Functional Disorders , University of Montreal, Quebec, Canada) была создана классификация функциональных расстройств у детей.
Данная классификация, построенная по клиническим критериям, в зависимости от преобладающих симптомов:
- расстройства, проявляющиеся рвотой: регургитапия, руминапия и циклическая рвота
- расстройства, проявляющиеся абдоминальными болями: функциональная диспепсия, синдром раздраженной кишки, функциональные абдоминальные боли, абдоминальная мигрень и аэрофагия
- расстройства дефекации: детская дисхезия (болезненная дефекация), функциональный запор, функциональная задержка стула, функциональный энкопрез.
Сами авторы признают несовершенство этой классификации, объясняя это недостаточными знаниями в области функциональных расстройств желудочно-кишечного тракта у детей, и подчеркивают необходимость дальнейшего изучения проблемы.
Клинические варианты функциональных нарушений
Гастро-эзофагальный рефлюкс
С точки зрения общей патологии, рефлюкс, как таковой, представляет собой перемещение жидкого содержимого в любых сообщающихся полых органах в обратном, антифизиологическом направлении. Это может произойти как в результате функциональной недостаточности клапанов и/или сфинктеров полых органов, так и в связи с изменением градиента давления в них.
Гастро-эзофагальный рефлюкс (ГЭР) означает непроизвольное затекание или заброс желудочного, либо желудочно-кишечного содержимого в пищевод. В основном, это нормальное явление, наблюдаемое у человека, при котором не развиваются патологические изменения в окружающих органах.
Помимо физиологического ГЭР, при длительной экспозиции кислого желудочного содержимого в пищеводе, может возникать патологический ГЭР, который наблюдается при ГЭРБ. ГЭР впервые описан Quinke в 1879 году. И, несмотря на такой длительный срок изучения данного патологического состояния, проблема остается до конца не разрешенной и достаточно актуальной. Прежде всего, это обусловлено широким спектром осложнений, которые вызывает ГЭР. Среди них: рефлюкс-эзофагит, язвы и стриктуры пищевода, бронхиальная астма, хроническая пневмония, фиброз легких и многие другие.
Выделяют ряд структур, обеспечивающих антирефлкжсный механизм: диафрагмально-пищеводную связку, слизистую "розетку" (складка Губарева), ножки диафрагмы, острый угол впадения пищевода в желудок (угол Гиса), протяженность абдоминальной части пищевода. Однако доказано, что в механизме закрытия кардии основная роль принадлежит нижнему пищеводному сфинктеру (НПС), недостаточность которого может быть абсолютной или относительной. НПС или кардиальное мышечное утолщение, строго говоря, не является анатомически автономным сфинктером. В то же время, НПС представляет собой мышечное утолщение, образованное мышцами пищевода, имеет особую иннервацию, кровоснабжение, специфическую автономную моторную деятельность, что позволяет трактовать НПС как обособленное морфофункциональное образование. Наибольшую выраженность НПС приобретает к 1-3 году жизни.
Кроме того, к антирефлюксным механизмам защиты пищевода от агрессивного желудочного содержимого можно отнести ощелачивающее действие слюны и "клиренс пищевода", т.е. способность к самоочищению посредством пропульсивных сокращений. В основе данного явления лежит первичная (автономная) и вторичная перистальтика, обусловленная глотательными движениями. Немаловажное значение среди антирефлкжсных механизмов занимает, так называемую, "тканевую резистентность" слизистой оболочки. Выделяют несколько составляющих тканевой резистентности пищевода: предэпителиальная (слой слизи, неперемешиваемый водный слой, слой бикарбонатных ионов); эпителиальная структурная (клеточные мембраны, межклеточные соединительные комплексы); эпителиальная функциональная (эпителиальный транспорт Na + /H + , Nа + -зависимый транспорт Cl - /HLO -3 ; внутриклеточные и внеклеточные буферные системы; клеточная пролиферация и дифференцировка); постэпителиальная (кровоток, кислотно-щелочное равновесие ткани).
ГЭР обычное физиологическое явление у детей первых трех месяцев жизни и часто сопровождается привычным срыгиванием или рвотой. Помимо недоразвития дистального отдела пищевода, в основе рефлюкса у новорожденных лежат такие причины как незначительный объем желудка и его шарообразная форма, замедление опорожнения. В основном физиологический рефлюкс не имеет клинических последствий и проходит спонтанно, когда эффективный антирефлюксный барьер постепенно устанавливается с введением твердой пищи. У детей более старшего возраста к ретроградному забросу пищи могут привести такие факторы, как увеличение объема желудочного содержимого (обильная еда, избыточная секреция соляной кислоты, пилороспазм и гастростаз), горизонтальное или наклонное положение тела, повышение внутрижелудочного давления (при ношении тугого пояса и употреблении газообразующих напитков). Нарушение антирефлюксных механизмов и механизмов тканевой резистентности приводят к широкому спектру патологических состояний, указанных ранее и требуют соответствующей коррекции.
Несостоятельность антирефлкжсного механизма может быть первичной и вторичной. Вторичная несостоятельность может быть обусловлена грыжей пищеводного отверстия диафрагмы, пилороспазмом и/или пилоростенозом, стимуляторами желудочной секреции, склеродермией, желудочно-кишечной псевдообструкцией и т.д.
Давление нижнего пищеводного сфинктера также снижается под влиянием гастроинтестинальных гормонов (глюкагона, соматостатина, холецистокинина, секретина, вазоактивного интестинального пептида, энкефалинов), ряда медикаментозных препаратов, пищевых продуктов, алкоголя, шоколада, жиров, пряностей, никотина.
В основе первичной несостоятельности антирефлюксных механизмов детей раннего возраста, как правило, лежат нарушения регуляции деятельности пищевода со стороны вегетативной нервной системы. Вегетативная дисфункция, чаще всего, обусловлена гипоксией головного мозга, развивающейся в период неблагоприятно протекающих беременности и родов.
Высказана оригинальная гипотеза о причинах реализации стойкого ГЭР. Данный феномен рассматривается с точки зрения эволюционной физиологии и ГЭР отождествляется с таким филогенетически древним приспособительным механизмом, как руминация. Повреждение демпинговых механизмов вследствие родовой травмы приводит к появлению функций не свойственных человеку как биологическому виду и носящих патологический характер. Установлена взаимосвязь между катальными повреждениями позвоночника и спинного мозга, чаще в шейном отделе, и функциональными расстройствами пищеварительного тракта. При исследовании шейного отдела позвоночника, у таких больных часто выявляются дислокация тел позвонков на различных уровнях, задержка сроков окостенения бугорка передней дуги 1-го шейного позвонка, ранние дистрофические изменения в виде остеопороза и платиспондилии, реже - деформации. У детей раннего возраста вторичное травмирование шейного отдела позвоночника может произойти при неправильном выполнении массажа. Указанные изменения обычно сочетаются с различными формами функциональных нарушений пищеварительного тракта и проявляются дискинезией пищевода, недостаточностью нижнего пищеводного сфинктера, кардиоспазмами, перегибом желудка, пилородуоденоспазмами, дуоденоспазмами, дискинезией тонкой и ободочной кишки. У 2/3 больных выявляются сочетанные формы функциональных нарушений: различные типы дискинезии тонкой кишки с ГЭР и стойким пилороспазмом.
Клинически это может проявиться следующими симптомами: усиление возбудимости ребенка, обильное слюнотечение, сильные срыгивания, интенсивные кишечные колики.
Клиническая картина ГЭР у детей характеризуется упорными рвотами, срыгиваниями, отрыжкой, икотой, утренним кашлем. В дальнейшем, присоединяются такие симптомы как изжога, боли за грудиной, дисфагия. Как правило, такие симптомы как изжога, боли за грудиной, в области шеи и спины наблюдаются уже при воспалительных изменениях слизистой оболочки пищевода, т.е. при рефлюкс-эзофагите.
Функциональная диспепсия
В 1991 году Tally дал определение неязвенной (функциональной) диспепсии. Симптомокомплекс, включающий в себя боли или чувство переполнения в подложечной области, связанное, либо несвязанное с приемом пищи или физическими упражнениями, раннее насыщение, вздутие живота, тошноту, изжогу, отрыжку, срыгивание, непереносимость жирной пищи и т.д., при котором в процессе тщательного обследования пациента не удается выявить какое-либо органическое заболевание.
В настоящее время в данное определение внесены уточнения. Заболевания, сопровождающиеся изжогой теперь рассматриваются в контексте ГЭРБ.
Согласно клинической картине в ФД выделяют 3 варианта:
- Язвенноподобный (локализованные боли в эпигастрии, голодные боли, или после сна, проходящие после приема пищи и (или) антацидов. Могут наблюдаться ремиссии и рецидивы;
- Дискинетический (раннее насыщение, чувство тяжести после еды, тошнота, рвота, непереносимость жирной пищи, верхнеабдоминальный дискомфорт, усиливающийся с приемом пищи);
- Неспецифический (разнообразные трудно классифицируемые жалобы).
Надо отметить, что деление довольно условное, так как жалобы в редких случаях бывают стабильными (по данным Johannessen T. et al. только 10% больных имеют стабильные симптомы). При оценке интенсивности симптомов больные чаще отмечают, что симптомы носят не интенсивный характер, за исключением боли при язвеноподобном типе.
В соответствии с Римскими II диагностическими критериями для ФД характерны 3 патогмоничных признака:
- Постоянная или рецидивирующая диспепсия (боль или дискомфорт, локализующийся в верхней части живота по средней линии), продолжительность которой составляет не менее 12 нед. за последние 12 мес;
- Отсутствие доказательств органического заболевания, подтверждаемое тщательным сбором анамнеза, эндоскопическим исследованием верхних отделов ЖКТ и ультразвуковым исследованием органов брюшной полости;
- Отсутствие доказательств, что диспепсия облегчается дефекацией или связана с изменением частоты или формы стула (состояния с такими симптомами относятся к СРК).
В отечественной практике если больной обращается с таким симптомокомплексом, то врач чаще всего поставит диагноз "хронически гастрит/гастродуоденит". В зарубежной гастроэнтерологии этим термином пользуются не клиницисты, а главным образом морфологи. Злоупотребление клиницистами диагнозом "хронический гастрит" превратил его по образному выражению, в "самый частый ошибочный диагноз" нашего столетия (Stadelman О., 1981). Многочисленные исследования проведенные в последние годы многократно доказали отсутствие какой-либо связи между гастритическими изменениями слизистой оболочки желудка и наличием у пациентов диспепсических жалоб.
Говоря об этиопатогенезе неязвенной диспепсии в настоящее время, большинство авторов значительное место отводят нарушению моторики верхних отделов ЖКТ, на фоне изменения миоэлектрической активности этих отделов ЖКТ, и связанной с этим задержки опорожнения желудка и многочисленных ГЭР и ДГР. X Lin et al. отмечают, что изменение желудочной миоэлектрической активности происходит после приема пищи.
К нарушениям гастродуоденальной моторики, выявленным у пациентов с неязвенной диспепсией, относятся: гастропарез, нарушение антродуоденальной координации, ослабление постпрандиальной моторики антрального отдела, нарушение распределения пищи внутри желудка (расстройства релаксации желудка; нарушения аккомодации пищи в дне желудка), нарушение циклической активности желудка в межпищеварительном периоде: желудочные дисритмии, ДГР.
При нормальной эвакуаторной функции желудка причинами диспептических жалоб может быть повышенная чувствительность рецепторного аппарата стенки желудка к растяжению (так называемая висцеральная гипречувствительность), связанная либо с истинным повышением чувствительности механорецептров стенки желудка или же с повышенным тонусом его фундального отдела. В ряде работ было показано, что у больных НД боли в эпигастральной области возникают при значительно меньшем повышении внутрижелудочного давления по сравнению со здоровыми лицами.
Ранее предполагалось, что в этиопатогенезе неязвенной диспепсии значительную роль играет НРБ, в настоящее время установлено, что этот микроорганизм не вызывает неязвенную диспепсию. Но есть работы которые показывают, что эррадикация НРБ приводит к улучшению состояния больных неязвенной диспепсией.
Не подтверждена ведущая роль пептического фактора в патогенезе неязвенной диспепсии. Проведенные исследования показали, что нет существенных различий в уровне секреции соляной кислоты у больных с неязвенной диспепсией и здоровых. Однако отмечена эффективность приема такими больными антисекреторных препаратов (ингибиторов протонной помпы и блокаторов Н 2 рецепторов гистамина). Можно предположить, что патогенетическую роль в этих случаях играет не гиперсекреция соляной кислоты, а увеличение времени контакта кислого содержимого со слизистой оболочкой желудка и двенадцатиперстной кишки, а также гиперчувствительность ее хеморецепторов с формированием неадекватного ответа.
У больных неязвенной диспепсией не было отмечено большей распространенности курения, употребления алкоголя, чая и кофе, приема НПВП по сравнению с пациентами страдающими другими гастроэнтерологическими заболеваниям.
Надо отметить, что не только изменения ЖКТ приводят к развитию неязвенной диспепсии. Эти больные значительно больше склонны к депрессии, и имеют отрицательное восприятие основных событий жизни. Это указывает что психологические факторы играют непоследнюю роль патогенезе неязвенной диспепсии. Поэтому в терапии неязвенной диспепсии должны приниматься во внимание как физические, так и психические факторы.
Продолжают вестись интересные работы по изучению патогенеза неязвенной диспепсии. Kaneko H. et al. выявили в своем исследовании, что концентрация Immimoreactive-somatostatin в слизистой желудка у больных с язвеноподобным типом неязвенной диспепсии значительно выше, чем в других группах неязвенной диспепсии, а так же в сравнении с больными с пептической язвой и контрольной группой. Также в этой группе была повышена концентрация вещества Р в сравнении с группой больных с пептической язвой.
Minocha A et al. провели исследование по изучению влияния газообразования на формирование симптомов у НР+ и HP- больных с неязвенной диспепсией.
Интересные данные получили Matter SE et al. Они выявили, что больные с неязвенной диспепсией, у которых повышенно количество тучных клеток в антральном отделе желудка хорошо поддаются терапии H 1 -антогонистами, в отличии от стандартной противоязвенной терапии.
Функциональные абдоминальные боли
Данное заболевание очень распространено, так по данным H.G.Reim et al. у детей с абдоминальной болью в 90% случаев нет органического заболевания. Преходящие эпизоды болей в животе встречаются у детей в 12% случаев. Из них только в 10% удается найти органическую основу этих абдоминалгий.
В клинической картине превалируют жалобы на абдоминальную боль, которая чаще локализуется в околопупочной области, но может отмечаться и в других регионах живота. Интенсивность, характер боли, частота атак очень вариабельны. Сопутствующими симптомами являются снижение аппетита, тошнота, рвота, диарея, головные боли, запоры бывают редко. У этих больных, так же как у пациентов с СРК и ФД отмечается повышенное беспокойство и психо-эмоциональные нарушения. Из всей клинической картины можно выделить характерные симптомы, основываясь, на которые можно поставить диагноз Функциональные абдоминальные боли (ФАБ).
- Часто повторяющаяся или непрерывная абдоминальная боль в течение, по крайней мере, 6 месяцев.
- Частичное или полное отсутствие связи между болью и физиологическими событиями (т.е. приемом пищи, дефекацией или менструациями).
- Некоторая потеря повседневной активности.
- Отсутствие органических причин боли и недостаточно признаков для диагностики других функциональных гастроэнтерологических заболеваний.
Для ФАБ очень характерны сенсорные отклонения, характеризующиеся висцеральной гиперчувствительностью, т.е. изменением чувствительности рецепторного аппарата к различным раздражителям и снижением болевого порога. В реализации болевых ощущений принимают участие как центральные, так и периферические болевые рецепторы.
Очень важную роль в развитии функциональных расстройств и в возникновении хронической абдоминальной болезни играют психосоциальные факторы и социальная дизадаптация.
Независимо от характера боли, особенностью болевого синдрома при функциональных расстройствах является возникновение болей в утреннее или дневное время при активности больного и стихание их во время сна, отдыха, отпуска.
У детей первого года жизни диагноз функциональные абдоминальные боли не ставится, а состояние с похожими симптомами называют Детскими коликами, т.е. неприятное, часто вызывающее дискомфорт, чувство распирания или сдавливания в брюшной полости у детей первого года жизни.
Клинически детские колики протекают, как у взрослых - боли в животе носящие спастический характер, но в отличие от взрослых у ребенка это выражается длительным плачем, беспокойством, сучением ножками.
Абдоминальная мигрень
Боль в животе при абдоминальной мигрени чаще всего встречается у детей и юношей, однако, нередко выявляется и у взрослых. Боль носит интенсивный, диффузный характер, но может иногда быть локализована в области пупка, сопровождаться тошнотой, рвотой, поносом, побледнением и похолоданием конечностей. Вегетативные сопутствующие проявления могут варьировать от негрубых, умеренно выраженных до ярких вегетативных кризов. Длительность болей колеблется от получаса до нескольких часов или даже нескольких суток. Возможны различные сочетания с мигренозной цефалгией: одновременное появление абдоминальной и цефалгической боли, их чередование, доминирование одной из форм при одновременном их присутствии. При диагностике необходимо учитывать следующие факторы: связь абдоминальной боли с головной болью мигренозною характера, характерные для мигрени провоцирующие и сопровождающие факторы, молодой возраст, семейный анамнез, терапевтический эффект противо-мигренозных препаратов, увеличение скорости линейного кровотока в брюшной аорте при доплерографии (особенно во время пароксизма).
Синдром раздраженного кишечника
Синдром раздраженного кишечника (СРК) - функциональное кишечное расстройство, проявляющееся абдоминальным болевым синдромом и/или нарушениями дефекации и/или метеоризмом. СРК - одно из очень частых заболеваний в гастроэнтерологической практике: 40-70% пациентов обращающихся к гастроэнтерологу, имеют СРК. Он может проявляться в любом возрасте в т.ч. у детей. Соотношение девушек и юношей - 2-4:1.
Ниже приводятся симптомы, на основе которых можно диагностировать СРК (Рим 1999)
- Частота стула менее чем 3 раза в неделю.
- Частота стула более чем 3 раза в день.
- Твердый или бобовидный кал.
- Разжиженный или водянистый кал.
- Натуживание на протяжении акта дефекации.
- Императивные позывы на акт дефекации (невозможность задержать опорожнение кишечника).
- Ощущение неполного опорожнения кишечника.
- Выделение слизи во время акта дефекации.
- Чувство переполнения, вздутия или переливания в животе.
Болевой синдром характеризуется многообразием проявлений: от диффузных тупых болей до острых, спазматических; от постоянных до пароксизмов болей в животе. Длительность болевых эпизодов - от нескольких минут до нескольких часов. Помимо основных "диагностических" критериев, у больного могут наблюдаться следующие симптомы: учащение мочеиспускания, дизурия, никтурия, дисменорея, утомляемость, головная боль, боль в спине. Изменение психической сферы в виде тревожных и депрессивных расстройств встречается у 40-70% больных с синдромом раздраженного кишечника.
В 1999 в Риме были разработаны диагностические критерии синдрома раздраженного кишечника: наличие абдоминального дискомфорта или болей в течение 12 необязательно последовательных недель за последние 12 месяцев, в сочетании с двумя из следующих трех признаков:
- купирующиеся после акта дефекации; и/или
- ассоциирующиеся с изменением частоты стула; и/или
- ассоциирующиеся с изменением формы кала.
Много лет изучаются патогенетические механизмы СРК. Двигательно-эвакуаторная функция кишечника у больных синдромом раздраженного кишечника изучалась многими исследователями, так как в клинической картине болезни нарушения именно этой функции выступают на первый план. Выявлены, по крайней мере, два типа двигательной активности дистальных отделов толстой кишки: сегментарные сокращения, которые возникают асинхронно в соседних сегментах кишки, и перистальтические сокращения. Большинство полученных данных относится только к сегментарной двигательной активности. Это обусловлено двумя обстоятельствами. Перистальтическая активность возникает редко, только один или два раза в день у здоровых волонтеров. Сегментарные сокращения, которые являются наиболее частым типом двигательной активности толстой кишки, скорее задерживают пассаж содержимого кишечника по направлению к анальному отверстию, чем продвигают его вперед.
Однако выявить специфичные для СРК нарушения моторики не удалось; наблюдаемые изменения регистрировались и больных с органическими заболеваниями кишечника и плохо коррелировали с симптомами СРК.
Больные СРК имеют значительно сниженную устойчивость к растяжению толстой кишки баллоном. На этом основании высказано предположение, что, измененная рецепторная чувствительность может быть причиной болевых ощущений при растяжении кишки у пациентов с СРК. Показано также, что у пациентов с СРК повышена чувствительность к растяжению толстой кишки и увеличена болевая чувствительность.
При СРК отмечался диффузный характер нарушения восприятия боли на всем протяжении кишечника. Выраженность синдрома висцеральной гипералгезии хорошо коррелировала с симптоматикой СРК.
Среди больных СРК, обращающихся к врачам, все исследователи отмечают большую частоту отклонений от нормы в психическом статусе и обострения заболевания при различных стрессовых ситуациях.
Больные, имеющие признаки СРК и, состоящие на диспансерном наблюдении, имеют определенный тип личности, который характеризуется импульсивным поведением, невротическим состоянием, беспокойством, мнительностью и ТА Депрессия и тревожность чаще всего характеризуют этих пациентов. Нарушение нервно-психического статуса проявляется в самых разнообразных симптомах. Среди них: утомляемость, слабость, головные боли, анорексия, парастезии, бессонница, повышенная раздражительность, сердцебиение, головокружение, потливость, чувство недостатка воздуха, боли в груди, учащенно мочеиспускание.
По мнению других ученых, кишечные нарушения и изменения психического статуса у больных СРК причинно не связаны и сосуществуют в большом проценте случаев только среди больных, обращающихся к врачам.
Установлено, что лица с невротическим типом личности больше акцентируют свое внимание на кишечных симптомах, что служит поводом обращения за медицинской помощью. Даже благоприятный прогноз СРК, у этих пациентов, вызывает чувство внутренней неудовлетворенности, усугубляет невротические расстройства, что может, в свою очередь, вызвать обострение синдрома раздраженного кишечника. Ряд исследователей показали, что больные, имеющие СРК, но с устойчивой нервной системой, как правило, за медицинской помощью не обращаются, либо обращаются при наличие сопутствующей патологии.
Таким образом, в настоящее время вопрос о роли стресса в этиопатогенезе СРК однозначно не может быть решен и требует дальнейшего изучения.
Запоры вызываются нарушением процессов формирования и продвижения кала по всей кишке. Запор - хроническая задержка опорожнения кишечника более чем на 36 часов, сопровождающаяся затруднением акта дефекации, чувством неполного опорожнения, отхождением малого (
Одной из наиболее частых причин запоров является дисфункция и некоординированная работа мышечных структур тазового дна и прямой кишки. В этих случаях происходит отсутствия или неполная релаксация задних или передних леваторов, пуборектальной мышцы. К запорам приводят расстройства кишечной моторики, чаще усиление непропульсивных и сегментирующих движений и снижение пропульсивной активности с повышением тонуса сфинктеров - "высыхание" калового столба, несоответствие емкости ТК и объема кишечного содержимого. Возникновение изменений структуры кишечника и близлежащих органов, может препятствовать нормальному продвижению. Также причиной функциональных запоров может стать угнетение дефекационного рефлекса, наблюдающееся у стеснительных детей (условно-рефлекторные запоры). Они возникают чаще всего с началом посещения ребенком детских дошкольных учреждений, при развитии анальных трещин и при сопровождении акта дефекации болевым синдромом - "боязнь горшка". Также запоры могут возникнуть при позднем вставании из постели, утренней спешке, учебе в разные смены, плохих санитарных условиях, чувстве ложного стыда. У детей-невропатов при длительной задержке стула, дефекация вызывает удовольствие.
Хроническая функциональная диарея
Разделение диареи на острую и хроническую произвольно, но обычно хронической считается диарея, продолжающаяся не менее 2 нед. Диарея представляет собой клиническое проявление нарушения всасывания воды и электролитов в кишечнике.
У детей раннего возраста диареей считается объем стула более 15 г/кг/сут. К трехлетнему возрасту объем стула приближается к таковому у взрослых, и в этом случае диареей считается объем, превышающий 200 г/сут. В плане определения функциональной диареи есть и другое мнение. Так, по мнению А.А. Шептулина при функциональном характере заболевания объем кишечного содержимого не увеличивается - масса кала у взрослого не превышает 200 г/сут. Меняется характер стула: жидкий, чаще кашицеобразный, с частотой 2-4 раза в день, чаще в утренние часы. Сопровождается усиленным газообразованием, позывы на дефекацию нередко носят императивный характер.
Функциональная диарея в объеме хронической диареи занимает значительное место. Примерно в 80% случаев в основе хронической диареи у детей лежат функциональные расстройства. По мнению И. Мадьяра в 6 из 10 случаев диарея носит функциональный характер. Чаще функциональная диарея является клиническим вариантом СРК, но если остальные диагностические критерии отсутствуют, то хроническая функциональная диарея рассматривается как самостоятельное заболевание. Этиология и патогенез функциональной диареи до конца не изучены, но установлено, что у таких пациентов отмечается усиление пропульсивной моторики кишечника, которое приводит к уменьшению времени транзита кишечного содержимого. Дополнительную роль могут играть и расстройства всасывания короткоцепочных жирных кислот в результате быстрого транзита содержимого по тонкой кишке с последующим нарушением абсорбции воды и электролитов в толстой кишке.
Дисфункции билиарного тракта
Из-за тесной анатомической и функциональной близости пищеварительных органов и особенностей реактивности растущего организма у гастроэнтерологических больных наблюдается, как правило, вовлечение в патологический процесс желудка, двенадцатиперстной кишки, желчевыводяших путей и кишечника. Поэтому вполне естественным является включение в классификацию функциональных нарушений моторики органов пищеварения и дисфункций желчевыводящих путей.
Классификация функциональных расстройств билиарного тракта:
- первичные дискинезии, обусловливающие нарушение оттока желчи и/или панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий;
- дисфункция желчного пузыря;
- дисфункция сфинктера Одди;
- вторичные дискинезии билиарного тракта, сочетающиеся с органическими изменениями желчного пузыря и сфинктера Одди.
В отечественной практике данное состояние описывается термином "дискинезия желчевыводящих путей". Дисфункции билиарного тракта сопровождаются нарушением процессов переваривания и всасывания, развитием избыточного бактериального роста в кишечнике, а так же нарушением моторной функции желудочно-кишечного тракта.
Диагностика
Диагностика функциональных заболеваний желудочно-кишечного тракта строится по их определению и предполагает тщательное обследование больного с целью исключения у него органических поражений ЖКТ. С этой целью, проводится тщательный сбор жалоб, анамнеза, общеклинические лабораторные исследования, биохимических исследований крови. Необходимо проводить соответствующие ультразвуковые, эндоскопические и рентгенологические исследования позволяющие исключить язвенную болезнь, опухоли желудочно-кишечного тракта, хронические воспалительные заболевания кишечника, хронический панкреатит, желчнокаменную болезнь.
Среди инструментальных методов диагностики ГЭР наиболее информативными являются 24-часовая рН-метрия и функциональные диагностические тесы (эзофагальная манометрия). 24-часовое мониторирование рН пищевода дает возможность выявить общее число эпизодов рефлюкса в течение суток и их продолжительность (нормальные показатели рН пищевода составляют 5,5-7,0, в случае рефлюкса менее 4). ГЭРБ диагностируется лишь в том случае, если общее количество эпизодов ГЭР в течение суток более 50 или общая продолжительность снижения рН в пищеводе до 4 и менее, превышает 1 ч. Сопоставление результатов исследования с данными записей дневника пациента (регистрация периодов приема пищи, препаратов, времени появления болей, изжоги и т. д) позволяет оценить роль наличия и выраженности патологического рефлюкса в возникновении тех или иных симптомов. При необходимости больным проводят сцинтиграфию.
При всех функциональных нарушениях ЖКТ важную роль играет психо-эмоциональный статус больного, поэтому при диагностике таких заболеваний необходима консультация психоневролога.
Необходимо обязательно обращать внимание на наличие у пациентов с ФН ЖКТ "симптомов тревоги" (alarm symptoms) или так называемых, "красных флагов" (red flags), к которым относятся лихорадка, немотивированное похудание, дисфагия, рвота с кровью (гематемезис) или черный дегтеобразный стул (мелена), появление алой крови в кале (гематохезия), анемия, лейкоцитоз, увеличение СОЭ. Обнаружение любого из этих симптомов делает диагноз функционального расстройства маловероятным и требует тщательного диагностического поиска с целью исключения серьезного органического заболевания.
Так как для точной диагностики ФН ЖКТ больному надо провести массу инвазивных исследований (ФЭГДС, рН-метрия, колоноскопия, холепистография, пиелография и т.п.), поэтому очень важно провести тщательный сбор анамнеза у больного, выявить симптомы и после этого провести необходимые исследования.
Лечение
В терапии всех выше указанных состояний важную роль играет нормализация режима питания, охранительный психоэмоциональный режим, разъяснительные беседы с больным и его родителями. Выбор лекарственных препаратов - сложная задача врача-гастроэнтеролога при функциональных заболеваниях ЖКТ.
Детям, с ФН ЖКТ, проводится лечение в соответствии с принципами стептерапии ("step-up/down treatment"). Сущность, т. н. "пошаговой" терапии, заключается в наращивании терапевтической активности по мере расходования средств из терапевтического арсенала. По достижении стабилизации или ремиссии патологического процесса, аналогичная тактика проводится и для снижения терапевтической активности.
Классическая схема терапии функциональных нарушений ЖКТ включает в себя прием биопрепаратов, спазмолитиков, антидепресантов.
Проблема микроэкологии кишечника в последние годы привлекает большое внимание не только педиатров, но и врачей других специальностей (гастроэнтерологов, неонатологов, инфекционистов, бактериологов). Известно, что микроэкологическая система организма, как взрослого, так и ребенка, - очень сложный филогенетически сложившийся, динамичный комплекс, включающий в себя разнообразные по количественному и качественному составу ассоциации микроорганизмов и продукты их биохимической активности (метаболиты) в определенных условиях среды обитания . Состояние динамического равновесия между организмом хозяина, микроорганизмами его заселяющими и окружающей средой принято называть "эубиоз", при котором здоровье человека находится на оптимальном уровне.
Существует множество причин, из-за которых происходит изменение соотношения нормальной микрофлоры пищеварительного тракта Эти изменения могут быть как кратковременными - дисбактериалъные реакции, так и стойкими - дисбактериоз. Дисбиоз представляет собой состояние экосистемы, при котором нарушается функционирование всех ее составных частей - организма человека, его микрофлоры и окружающей среды, а также механизмов их взаимодействия, что ведет к возникновению заболевания. Под дисбактериозом кишечника (ДК) понимают качественные и количественные изменения характерной для данного биотипа нормофлоры человека, влекущие за собой выраженные клинические реакции макроорганизма или являющиеся следствием каких-либо патологических процессов в организме. ДК следует рассматривать как симптомокомплекс, но не как заболевание. Совершенно очевидно, что ДК всегда вторичен и опосредован основным заболеванием. Именно этим объясняется отсутствие такого диагноза, как "дисбиоз" или "дисбактериоз кишечника" в Международном классификаторе заболеваний человека (МКБ-10), принятом в нашей стране, как и во всем мире.
В период внутриутробного развития жедудочно-кишечный тракт плода стерилен. Во время родов новорожденный колонизирует ЖКТ через рот, проходя по родовым путям матери. Бактерии E.Coli и стрептококки можно обнаружить в ЖКТ через несколько часов после рождения, причем они распространяются ото рта к анусу. Различные штаммы бифидобактерий и бактероиды появляются в ЖКТ спустя 10 дней после рождения. Дети, рожденные путем кесарева сечения, имеют значительно более низкое содержание лактобактерий, чем появившиеся естественным путем. Только у детей, находящихся на естественном вскармливании (грудное молоко), в микрофлоре кишечника преобладают бифидобактерий, с чем связывают меньший риск развития гастроинтестинальных инфекционных заболеваний.
При искусственном вскармливании у ребенка не формируется преобладание какой-либо группы микроорганизмов. Состав кишечной флоры ребенка после 2 лет незначительно отличается от взрослою: более 400 видов бактерий, причем большинство - анаэробы, плохо поддающиеся культивированию. Все бактерии попадают в ЖКТ оральным путем. Плотность бактерий в желудке, тощей, подвздошной и ободочной кишках соответственно равна 1000,10 000,100 000 и 1000 000 000 в 1 мл содержимого кишечника.
К факторам, влияющим на разнообразие и плотность микрофлоры в различных отделах ЖКТ, в первую очередь относятся моторика (нормальное строение кишечника, его нервно-мышечного аппарата, отсутствие дивертикулов тонкой кишки, дефектов илеоцекального клапана, стриктур, спаек и т.д.) кишечника и отсутствие возможных влияний на этот процесс, реализуемых функциональными расстройствами (замедление прохождения химуса через толстую кишку) или заболеваниями (гастродуоденит, сахарный диабет, склеродермия, болезнь Крона, язвенно-некротический колит и др.). Это позволяет рассматривать нарушение микрофлоры кишечника как следствие "синдрома раздраженной толстой кишки" - синдрома функциональных и двигательно-эвакуаторных расстройств ЖКТ с/без изменений биоценоза кишечника. Другими регуляторными факторами являются: рН среды, содержание в ней кислорода, нормальный ферментный состав кишечника (поджелудочной железы, печени), достаточный уровень секреторного IgA и железа. Рацион питания ребенка старше года, подростка, взрослого не имеет такого большого значения, как в период новорожденности и в первый год жизни.
В настоящее время биологически активные вещества, применяемые для улучшения функционирования пищеварительного тракта, регуляции микробиоценоза ЖКТ, профилактики и лечения некоторых специфических инфекционных заболеваний подразделяют на диетические добавки, функциональное питание, пробиотики, пребиотики, синбиотики, бактериофаги и биотерапевтические агенты. По данным литературы, первые три группы объединяются в одну - пробиотики. Применение пробиотиков и пребиотиков приводит к одному и тому же результату - увеличению числа молочнокислых бактерий, естественных обитателей кишечника (табл.1). Таким образом, эти препараты в первую очередь должны назначаться детям грудного возраста, пожилым людям и тем, кто находится на стационарном лечении.
Пробиотики - живые микроорганизмы: молочнокислые бактерии, чаще бифидо - или лактобактерий, иногда дрожжи, которые, как следует из термина "пробиотик", относятся к нормальным обитателям кишечника здорового человека.
Препараты-пробиотики на основе этих микроорганизмов широко используются в качестве питательных добавок, а также в йогуртах и других молочных продуктах. Микроорганизмы, входящие в состав пробиотиков, не патогенны, не токсичны, содержатся в достаточном количестве, сохраняют жизнеспособность при прохождении через желудочно-кишечный тракт и при хранении. Пробиотики, в основном, не считаются лекарственными препаратами и рассматриваются как средства, полезно влияющие на состояние здоровья людей.
Пробиотики могут включаться в питание в качестве диетических добавок в виде лиофилизированных порошков, содержащих бифидобактерий, лактобактерий и их комбинации, используются без назначения врача для восстановления микробиоценоза кишечника, для поддержания хорошего состояния здоровья, поэтому разрешение на производство и применение пробиотиков в качестве диетических добавок от государственных структур, контролирующих создание лекарственных препаратов (в США - Food and Drug Administration (PDA), а в России - Фармакологический комитет и Комитет медицинских и иммунобиологических препаратов МЗ РФ) не требуется.
Пребиотики. К пребиотикам относятся частично или полностью неперивариваемые ингредиенты пищи, которые способствуют улучшению здоровья за счет избирательной стимуляции роста и/или метаболической активности одной или нескольких групп бактерий, обитающих в толстой кишке. Чтобы компонент пищи был классифицирован как пребиотик, он не должен подвергаться гидролизу пищеварительными ферментами человека, не должен абсорбироваться в верхних отделах пищеварительного тракта, однако должен являться селективным субстратом для роста и/или метаболической активации одного вида или определенной группы микроорганизмов, заселяющих толстый кишечник, приводя к нормализации их соотношения. Ингредиенты питания, которые отвечают этим требованиям, являются низкомолекулярными углеводами. Свойства пребиотиков наиболее выражены во фруктозо-олигосахаридах (ФОС), инулине, галакто-олигосахаридах (ГОС), лактулозе, лактитоле. Пребиотики находятся в молочных продуктах, кукурузных хлопьях, крупах, хлебе, луке репчатом, цикории полевом, чесноке, фасоли, горохе, артишоке, аспарагусе, бананах и многих других продуктах. На жизнедеятельность микрофлоры кишечника человека в среднем расходуется до 10% поступившей энергии и 20% объема принятой пищи.
Несколько исследований, проведенных на взрослых добровольцах, доказали выраженное стимулирующее влияние олигосахаридов, особенно тех, которые содержат фруктозу, на рост бифидо- и лактобактерии в толстом кишечнике. Инулин - полисахарид, содержащийся в клубнях и корнях георгинов, артишоков и одуванчиков. Он представляет собой фруктозам, так как при его гидролизе образуется фруктоза. Было показано, что инулин помимо стимуляции роста и активности бифидо- и лактобактерии, повышает всасывание кальция в толстом кишечнике, т.е. снижает риск остеопороза, влияет на метаболизм липидов, уменьшая риск атеросклеротических изменений в сердечно-сосудистой системе и, возможно, предотвращая развитие сахарного диабета II типа, имеются предварительные данные о его антиканцерогенном эффекте. Олигосакариды, включая М-ацетилглюкозамин, глюкозу, галактозу, олигомеры фукозы или другие гликопротеины, которые в значительной пропорции составляют грудное молоко, являются специфичными факторами для роста бифидобактерий.
Лактулоза (Дюфалак) - синтетический дисахарид, не встречающийся в природе, в котором каждая молекула галактозы связана (3-1,4-связью с молекулой фруктозы. Лактулоза попадает в толстый кишечник в неизмененном виде (лишь около 0,25-2,0% всасывается в неизмененном виде в тонкой кишке) и служит питательным субстратом для сахаролитических бактерий. Лактулоза уже более 40 лет применяется в педиатрии для стимуляции роста лактобактерии у детей грудного возраста.
В процессе бактериального разложения лактупозы на короткоцепочечные жирные кислоты (молочная, уксусная, пропионовая, масляная) снижается рН содержимого толстой кишки. За счет этого же повышается осмотическое давление, ведущее к задержке жидкости в просвете кишки и усилению ее перистальтики. Использование лактулозы (Дюфалака) как источника углеводов и энергии приводит к увеличению бактериальной массы, и сопровождается активной утилизацией аммиака и азота аминокислот. Эти изменения в конечном итоге ответственны за профилактический и терапевтический эффекты лактупозы: при запорах, портосистемной энцефалопатии, энтеритах (Salmonella enteritidis, Yersinia, Shigella), сахарном диабете и других возможных показаниях.
До настоящего времени еще мало изучены свойства таких пребиотиков, как маннозо-, мальтозо-, ксилозо- и глюкозо-олигосахаридов.
Смесь пробиотиков и пребиотиков объединена в группу синбиотиков, которые оказывают полезный эффект на здоровье организма-хозяина, улучшая выживаемость и приживляемость в кишечнике живых бактериальных добавок и избирательно стимулируя рост и активацию метаболизма индигенных лактобактерии и бифидобактерий.
Применение прокинетиков в лечении функциональных нарушений имеет место, но их эффективность не очень высока и они не могут использоваться в виде монотерапии.
С давних времен расстройства работы кишечника лечили энтеросорбентами. При этом использовались древесные угли и сажа. Метод энтеросрбции основан на связывании и выведении из ЖКТ различных микроорганизмов, токсинов, антигенов, химических веществ и т.п. Адсорбционные свойства сорбентов обусловлены наличием в них развитой пористой системы, обладающей активной поверхностью, способной удерживать газы, пары, жидкости или вещества находящиеся в растворе. Механизмы лечебного действия энтеросорбции связаны с прямыми и опосредованными эффектами:
| Прямое действие | Опосредованные эффекты |
| Сорбция ядов и ксенобиотиков, поступающих per os | Предотвращение или ослабление токсико-аллергических реакций |
| Сорбция ядов, выделяемых в химус секретом слизистых оболочек, печени, поджелудочной железы | Профилактика соматогенной стадии экзотоксикоза |
| Сорбция эндогенных продуктов секреции и гидролиза | Снижение метаболической нагрузки на органы экскреции и детоксикации |
| Сорбция БАВ - нейропептидов, простогландинов, серотонина, гистамина и др. | Коррекция обменных процессов и иммунного статуса. Улучшение гуморальной среды |
| Сорбция патогенных бактерий и бактериальных токсинов | Восстановление целостности и проницаемости слизистых оболочек |
| Связывание газов | Устранение метеоризма, улучшение кровоснабжения кишечника |
| Раздражение рецепторных зон ЖКТ | Стимуляция моторики кишечника |
В качестве энтеросорбентов в основном используют пористые углеродные адсорбенты в частности активированные угли различного происхождения, получаемые из богатого углеродом растительного или минерального сырья. Основными медицинскими требованиями к энтеросорбентам являются:
- нетоксичность;
- атравматичность для слизистых оболочек;
- хорошая эвакуация из кишечника;
- высокая сорбционная емкость;
- удобная фамацевтическая форма;
- отсутствие отрицательных органолептических свойств сорбента (что особенно важно в детской практике);
- благоприятное воздействие на процессы секреции и биоценоз кишечника.
Отвечают всем вышеперечисленным требованиям энтеросорбенты, созданные на основе природного полимера растительного происхождения лигнина. Он был разработан еще в 1943 году под названием "пролизан" в Германии Г.Шоллером и Л. Меслером. Также успешно применялся как противодиарейное средство, а детям раннего возраста вводился с помощью клизмы. В 1971 году в Ленинграде создали "медицинский лигнин", который позднее был переименован в полифепан. Одним из отрицательных свойств препарата является то, что наибольшей адсорбционной активностью он обладает в форме влажного порошка, который является благоприятной средой для размножения микроорганизмов. Поэтому препарат достаточно часто бракуется контрольными лабораториями МЗ РФ, а выпуск препарата в виде сухих гранул приводит к значительному снижению его адсорбционной способности.
Как уже было отмечено ранее, одним из ведущих патологических механизмов в функциональных заболеваниях кишечника является чрезмерное сокращение гладкой мускулатуры кишечной стенки и связанная с этим абдоминальная боль. Поэтому в терапии этих состояний рационально использовать лекарственные средства обладающие спазмолитической активностью.
Многочисленные клинические исследования доказали эффективность и хорошую переносимость миотропных спазмолитиков при функциональных заболеваниях кишечника. Однако эта фармакологическая группа неоднородна, и при выборе препарата следует учитывать его механизм действия, поскольку абдоминальная боль очень часто сочетается с другими клиническими симптомами, в первую очередь, с метеоризмом, запором и диареей.
Действующим началом препарата Дюспаталин является мебеверин гидрохлорид, производное метоксибензамина. Особенностью препарата Дюспаталин является то, что гладкомышечные сокращения подавляются мебеверином не полностью, что указывает на сохранение нормальной перистальтики после подавления гипермоторики. Действительно, не существует известной дозы мебеверина, которая бы полностью ингибировала перистальтические движения, т.е. вызывала бы гипотонию. Экспериментальные исследования показывают, что мебеверин обладает двумя эффектами. Первое, препарат оказывает антиспастический эффект, снижая проницаемость клеток гладкой мускулатуры для Na+. Второе, он непрямым образом уменьшает отток К+, и, соответственно, не вызывает гипотонию.
Основное клиническое преимущество препарата Дюспаталин заключается в том, что он показан пациентам с синдромом раздраженного кишечника и абдоминальной болью функционального генеза, которая сопровождается как запором, так и диареей, поскольку препарат оказывает нормализующее действие на функцию кишечника.
При необходимости в терапию функциональных нарушений кишечника включают антидиарейные, слабительные препараты, но во всех случаях эти средства нельзя использовать в качестве монотерапии.
Дискутируется роль Helicobacter pylori (HP) в патогенезе хронической абдоминальной боли. Проведенные исследования показали, что значимой роли инфецированность HP не играет, но некоторые авторы представляют данные о некотором снижения интенсивности болей после эррадикации HP. Рекомендуется обследовать пациентов с абдоминальной болью только при подозрении на структурные изменения в органах.
Применение прокинетиков в лечении функциональных нарушений имеет место, но их эффективность не очень высока и они не могут использоваться в виде монотерапии. Наиболее широко прокинетики используются при лечении ГЭР. Среди прокинетиков наиболее эффективными антирефлкжсными лекарственными препаратами, используемыми в настоящее время в педиатрической практике, являются блокаторы дофаминовых рецепторов - прокинетики, как центральных (на уровне хеморецепторной зоны мозга), так и периферических. К ним относятся метоклопрамид и домперидон. Фармакологическое действие этих препаратов заключается в усилении антропилорической моторики, что приводит к ускоренной эвакуации содержимого желудка и повышению тонуса нижнего пищеводного сфинктера. Однако при назначении церукала, особенно у детей раннего возраста в дозе 0,1 мг/кг 3-4 раза в сутки мы наблюдали экстапирамидные реакции. Более предпочтителен в детском возрасте антагонист дофаминовых рецепторов - домперидон Мотилиум. Данный препарат имеет выраженный антирефлюксный эффект. Кроме того, при его применении практически не отмечены экстрапирамидные реакции у детей. Также обнаружено позитивное влияние домперидона при запорах у детей: он приводит к нормализации процесса дефекации. Мотилиум назначается в дозе от 0,25 мг/кг (в виде суспензии и таблеток) 3-4 раза в день за 30-60 минут до приема пищи и перед сном. Его нельзя сочетать с антацидными препаратами, так как для его всасывания необходима кислая среда и с антихолинергическими препаратами, которые нивелируют эффект мотилиума.
Учитывая, что гграктически, при всех выше указанных заболеваниях не маловажную роль играет психо-эмоциональный статус больного то необходимо после консультации психоневролога решить вопрос о назначении психотропных препаратов (антидепресантов).
Часто при ФН ЖКТ у больных, как отмечалось выше, наблюдается не только моторная дисфункции, но и нарушение переваривания. В связи с этим правомерно при таких заболеваниях применять в терапии ферментативные препараты. В настоящее время на фармацевтическом рынке есть множество ферментов. Далее приведены требования предъявляемые к современным ферментным препаратам:
- нетоксичность;
- хорошая переносимость;
- отсутствие побочных реакций;
- оптимум действия при рН 5-7,5;
- устойчивость к действию НСl, пепсинов, протеаз;
- содержание достаточного количества активных пищеварительных ферментов;
- длительный срок хранения.
Все представленные на рынке ферменты можно разделить на следующие группы:
- экстракты слизистой оболочки желудка (пепсин): абомин, ацидинпепсин, пепсидил, пепсин;
- панкреатические энзимы (амилаза, липаза, трипсин): креон, панкреатин, панцитрат, мезим-форте, трифермент, пангрол, пролипаза, панкурмен;
- ферменты, содержащие панкреатин, компоненты желчи, гемицеллюлазу: дигестал, фестал, котазим-форте, панстал, энзистал;
- комбинированные ферменты: комбицин (панкреатин + экстракт рисового грибка), панзинорм-форте (липаза + амилаза + трипсин + химотрипсин + холевая кислота + гидрохлориды аминокислот), панкреофлат (панкреатин + диметикон);
- ферменты, содержащие лактазу: тилактаза, лактраза.
Для коррекции панкреатической недостаточности часто наблюдаемой при ФН ЖКТ используются панкреатические энзимы. В сводной таблице приведен состав этих препаратов.
Такие препараты, как КРЕОН®, Панцитрат, Пангрол относятся к "терапевтической" группе энзимов и характеризуется высокой концентрацией энзимов, возможностью замещение внешнесекреторной функции поджелудочной железы, и что очень важно быстрым наступлением лечебного эффекта. Однако надо отметить, что длительное применение высоких доз ферментов Пангрол, Панцитрат в отличие от препарата Креон опасно развитием структур в восходящем отделе и илеоцекальной области толстой кишки.
Заключение
В заключение хотелось бы отметить, что изучение проблемы функциональных нарушений ЖКТ у детей в настоящее время поставило больше вопросов, чем дало ответов. Так до сих пор не разработана классификация ФН ЖКТ у детей, удовлетворяющая всем требованиям. В связи с неизученностью механизмов этиопатогенеза нет патогенетической терапии данных заболеваний. Подбор симптоматической терапии сложный "творческий" процесс врача-гастроэтеролога и педиатра. Для обозначения часто встречающихся в клинической практике жалоб, связанных с дисфункциями пищеварительного тракта, существует довольно запутанное многообразие понятий, нередко являющихся синонимами. В связи с этим, становится крайне желательным единое определение различных обозначений данной патологии. Значительная распространенность функциональных заболеваний желудочно-кишечного тракта у детей порождает необходимость определить некоторые положения, имеющие первостепенное значение для практического врача:
- определение групп риска по каждой нозологической форме;
- планомерные профилактические мероприятия, включая диетическое питание;
- своевременная и правильная трактовка первых клинических признаков;
- щадящий, то есть предельно обоснованный, выбор методов диагностики, дающих максимально полную информацию.
Список литературы
- Детская гастроэнтерология. Руководство на компакт-диске. Под общей редакцией С.В. Бельмера и А.И. Хавкина. Москва, 2001 г., 692 MB.
- А.А. Шептулин. Современные возможности применения различных форм имодиума в лечении больных с острой диареей и СРК (функциональной диареей) Клинические перспективы гастроэнтерологии, гепатологии. 3, 2001 26-30.
- А.М. Вейн, А.Б. Данилова. Кардиалгии и абдомиалгии РМЖ, Том 7 № 9,1999.
- А.И. Лобаков, Е.А. Белоусова. Абдоминальная боль: трудности трактовки и методы купирования. Врачебная газета, 2001, №05.
- А.И. Парфенов. Диарея. РМЖ, Том 6. № 7, 1998.
- Б.Д. Старостин Современные представления о функциональной (неязвенной) диспепсии. Болезни органов пищеварения. Том 2, № 1, 2000.
- Вегетативные расстройства: Клиника, лечение диагностика // Под редакцией А.М. Вейна. - М.: Медицинское информационное агентство, 1998. - 752с.
- Е.С.Рысс. Современные представления о синдроме раздраженного кишечника. Гастробюллетень №1 2001
- Е. Нурмухаметова. Хроническая осмотическая диарея у детей. РМЖ Т.6 №23 1998. 1504-1508
- Избранные лекции по гастроэнтерологии // Под ред. ВТ. Ивашкина, А.А. Шептулина. - М.: МЕДпрсс, 2001. - 88 с.
- И.Мадьяр. Дифференциальная диагностика заболеваний внутренних органов: Пер. с венг. - Т. 1 - Будапешт, 1987. - 771с.
- Особенности фармакотерапии в детской гастроэнтерологии // Под редакцией проф. А.М. Запруднова // М. 1998. - 168с.
- Функциональные заболевания кишечника и желчевыводяших путей: вопросы классификации и терапии. Международный бюллетень: Гастроэнтерология, 2001, №5.
- Фролькис А.В. Функциональные заболевания желудочно-кишечного тракта. Л., Медицина, 1991. - 224 с.
- В Pfafifenbach, RJ Adamek, G Lux. The place of electrogastrography in the diagnosis of gastroenterological functions. Deutsche Medizinische Wochenschrift 123 (28-29) 1998, 855-860.
- Clouse RE; Lustman PJ; Geisman RA; Alpers DH. Antidepressant therapy in 138 patients with irritable bowel syndrome: a five-year clinical experience // Aliment.Pharmacol.Ther.-1994.- Vol.8.- N4.- P.409-416.
- Cucchiara S; Bortolotti M; Colombo C; Boccieri A, De Stefano M; Vitiello G; Pagano A; Ronchi A; Auricchio S. Abnormalities of gastrointestinal motility in children with nonulcer dyspepsia and in children with gastroesophageal reflux disease. Dig Dis Sci 1991 Aug;36(8):1066-73.
- Chang CS; Chen GH; Kao CH; Wang SJ; Peng SN, Huang CK. The effect of Helicobacter pylori infection on gastric emptying of digestible and indigestible solid-s in patients with nonulcer dyspepsia. Am J Gastroenterol 1996 Mar;91(3):474-9.
- Di Lorenzo C; Lucanto C; Flores AF; Idries S, Hyman PE. Effect of octreotide on gastrointestinal motility in children with functional gastrointestinal symptoms // J. Pediatr. Gastroenterol. Nutr.- 1998.- Vol.27.- N5:- P.508-512.
- Drossman D.A. The Functional Gastrointestinal Disorders. Diagnosis, Pathophysiology, and treatment. A Multinational Consensus. Little, brown and Company. Boston/ Hew York/ Toronto/ London. 1994. 370 p.
- Drossman D.A. The Functional Gastrointestinal Disorders and the Rome II process // Gutl999;45(Suppl.2)
- Drossman D.A, Whitehead WE, Toner BB, Diamant N, Hu YJ, Bangdiwala SI, Jia H. What determines severity among patients with painful functional bowel disorders? Am J Gastroenterol. 2000 Apr;95(4):862-3
- Farfan Flores G; Sanchez G; Tello R; Villanueva G. Estudio clinico у etiologico de 90 casos de diarrea cronica // Rev.Gastroenterol.Peru - 1993.- Vol.13.- N1.- P.28-36.
- Forbes D. Abdominal pain in childhood. Aust Fam Physician 1994 Mar;23 (3)347-8, 351, 354-7.
- Fleisher DR. Functional vomiting disorders in infancy: innocent vomiting, nervous vomiting, and infant rumination syndrome // J.Pediatr- 1994- Vol.125.- N6 Pt 2-P.S84-S94.
- Franchini F; Brizzi. Il pediatra ed il bambino con malattia psicosomatica: alcune riflessioni // Pediatr.Med.Chir.- 1994.- Vol.16.- N2.- P.I 55-1 57.
- Gorard DA, J.E.Gomborone, G.W.Libby, M.J.G.Farthing. GUT 39: 551-555. 1996
- Gottrand F. The role of Helicobacter pylori in abdominal pain in children. Arch Pediatr 2000 Feb;7(2):l 97-200.
- Goodwin S; Kassar-Juma W; Jazrawi R; Benson M, Northfield T. Nonulcer dyspepsia and Helicobacter pylori, with comment on posteradication symptoms. Dig Dis Sci 1998 Sep;43(9 Suppl):67S-71S.
- George AA; Tsuchiyose M; Dooley CP. Sensitivity of the gastric mucosa to acid and duodenal contents in patients with nonulcer dyspepsia. Gastroenterology 1991.
- Haruma K; Wiste JA; Camilleri M. Effect of octreotide on gastrointestinal pressure profiles in health and in functional and organic gastrointestinal disorders // Gut-1994.- Vol.35.- N8.- P.1064-1069.
- Hotz J; Plein K; Bunke R. Wirksamkeit von Ranitidin beim Reizmagensyndrom (funktionelle Dyspepsie) im Vergleich zu einem Antacidum // Med.Klin.- 1994.-Vol.89.- N2.- P.73-80.
- Kohutis EA. Psychological aspects of irritable bowel syndrome // N.JAded.- 1994.-Vol.91.-Nl.-P.30-32.
- Koch K.L. Motility disorders of the stomach // Innovation towards better GI care. 1. Janssen-Cilag congress. Abstracts. - Madrid, 1999. - P.20-21.
- Lydiard RB; Greenwald S; Weissman MM; Johnson J. Panic disorder and gastrointestinal symptoms: findings from the NIMH. Epidemiologic Catchment Area project // Am.J.Psychiatry.- 1994.- Vol.151.- N1.- P.64-70.
- McColl K; Murray L; El-Omar E; Dickson A; El-Nujumi A; Wirz A; Kelman A; Penny C; Knill-Jones R; Hilditch Т N. Symptomatic benefit from eradicating Helicobacter pylori infection in patients with nonulcer dyspepsia. Engl J Med 1998 Dec 24;339(26):1869-74.
- Patients with dyspepsia. A heterogeneous population. Gastrointestinal dysmotility. Focus of cisapride. Eds. R.C. Headimg, J.D. Wood, NJ 1992.
- Reimm H.G., Koken M.. Functional abdominal pain in childhood. Medical treatment with mebeverine (DuspatalR suspension)
- Rasquin-Weber A; Hyman PE; Cucchiara S; Fleisher DR. Hyams JS; Milla PJ; Staiano Childhood functional gastrointestinal disorders // Gut- 1999.- Vol.45.- Suppl.2:-P.II60-II68.
- Riezzo G; Cucchiara S; Chiloiro M; Minella R, Guerra V; Giorgio I. Gastric emptying and myoelectrical activity in children with nonulcer dyspepsia. Effect of cisapride. Dig Dis Sci 1995 Jul;40(7):1428-34.
- Scott RB. Recurrent abdominal pain during childhood // Can.Fam.Physician- 1994.-Vol.40.- P.539-547.
- Sheu BS; Lin CY; Lin XZ; Shiesh SC; Yang HB; Chen CY. Long-term outcome of triple therapy in Helicobacter pylori-related nonulcer dyspepsia: a prospective controlled assessment Am J Gastroenterol 1996 Mar;91(3)441-7.
- Staiano A; Cucchiara S; Andreotti MR; Minella R, Manzi G. Effect of cisapride on chronicidiopathic constipation in children // Dig.Dis.Sci- 1991- Vol.36.- N6- P.733-736.
- Staiano A; Del Giudice E. Colonic transit and anorectal manometry in children with severe brain damage // Pediatrics.-1994.- Vol.94.- N2 Pt 1.- P.169-73.
- Talley NJ. Nonulcer dyspepsia: myths and realities. Aliment. Pharmacol. Ther. 1991. Vol 5.
- Talley NJ. and working team for functional gastroduodenal disorders. Functional gastroduodenal disorders// In: The functional gastroduodenal disorders. - Boston - New York - Toronto - London, 1994. - P. 71-113.
- Van Outryve M; Milo R; Toussaint J; Van Eeghem P. "Prokinetic" treatment of constipation-predominant irritable bowel syndrome: a placebo-controlled study of cisapride // J.Clm.Gastroenterol - 1991. - Vol. 13. - N 1. - P.49-57.
- Velanovich V. A prospective study of Helicobacter pylori nonulcer dyspepsia. Mil Med 1996, Apr;161(4):197-9.
Парфенов А.И., Ручкина И.Н., Усенко Д.В.
Функциональную патологию кишечника отличает отсутствие морфологических изменений, которыми можно было бы объяснить имеющиеся клинические симптомы, и их связь с:
повышенной возбудимостью моторики,
сенсорной гиперчувствительностью,
неадекватной реакцией внутренних органов на сигналы ЦНС при воздействии психосоциальных факторов .
Этиология и патогенез
На формирование функциональных нарушений кишечника (ФНК) оказывают влияние генетические факторы, окружающая среда, психосоциальные факторы, висцеральная гиперчувствительность и инфекции.
Генетическую предрасположенность к ФНК подтверждает искаженный ответ слизистой оболочки больных с синдромом раздраженного кишечника (СРК) на воздействие нейротрансмиттера 5-HT , a2-адренорецепторов и неадекватная реакция гипоталамо-адреналовой системы на стрессы .
На влияние окружающей среды указывают факты более частого формирования ФНК у детей, родители которых страдают этой патологией и чаще посещают врача, чем дети родителей, не считающих себя больными .
Известно, что систематическое психическое напряжение способствует появлению, хронизации и прогрессированию ФНК .
Особенностью больных ФНК является повышение двигательной и сенсорной реакции, появление боли в животе в ответ на стрессы и нейрохимические посредники типа кортикотропина . На клиническую картину ФНК решающее влияние оказывает повышение или снижение чувствительности механорецепторов, мышечного аппарата кишечника . Повышением висцеральной чувствительности объясняют механизм боли у больных с СРК и функциональным болевым абдоминальным синдромом . У этих больных снижен порог болевой чувствительности при растяжении кишки баллоном.
Одной из причин нарушения чувствительности может служить воспаление слизистой оболочки у больных, перенесших острую кишечную инфекцию (ОКИ). Воспаление вызывает дегрануляцию тучных клеток вблизи от энтериновых сплетений, увеличенную продукцию серотонина и провоспалительных цитокинов . Этим объясняется повышение висцеральной чувствительности у больных с ФНК.
Нарушения висцеральной чувствительности часто вызывают ОКИ вследствие воспаления слизистой оболочки кишечника. Это является причиной развития синдрома, подобного СРК, у 25% лиц, перенесших ОКИ . По нашим данным, у 30% СРК болезни предшествовала ОКИ . В патогенезе хронизации заболевания кишечника имеет значение высокое бактериальное обсеменение тонкой кишки, выявленное с помощью дыхательного водородного теста, а также повреждение энтериновой нервной системы антигенами ОКИ на фоне снижения иммунной защиты организма .
Таким образом, одним из факторов, способствующих формированию СРК, могут быть ОКИ . И.Н. Ручкина установила, что у больных постинфекционным СРК в той или иной степени формируется дисбиоз (часто с избыточным ростом микрофлоры в тонкой кишке) и сформулировала его критерии .
Известны и другие работы, показывающие возможную роль повышенного бактериального роста в патогенезе СРК . L. O’Mahony и соавт. наблюдали хороший эффект лечения больных с СРК пробиотиком, содержащим Bifidobacter infantis. Авторы объясняют прекращение болей и диареи восстановлением соотношения про- и противовоспалительных интерлейкинов 10 и 12 .
Классификация ФН кишечника
Клинические проблемы функциональных нарушений органов пищеварения на протяжении последних 20 лет активно обсуждаются в рамках Римского консенсуса. Консенсус сыграл ведущую роль в классификации, уточнении клинических и диагностических критериев этих заболеваний. Последняя классификация утверждена в мае 2006 г. В таблице 2 представлены функциональные болезни кишечника.
Эпидемиология
Эпидемиологические исследования показывают примерно одинаковую частоту ФНК в странах Западной Европы, США и Австралии и более низкую заболеваемость в странах Азии и среди африканских американцев . Различия могут объясняться также типом используемых критериев и эффективности лечения .
Принципы диагностики
Диагностика ФНК согласно классификации Рим-III основана на предпосылке, что каждое ФНК имеет симптомы, отличающиеся особенностями моторной и сенсорной дисфункции. Следствием моторной дисфункции являются диарея и запор. Боль в значительной мере определяется степенью нарушения висцеральной чувствительности, объясняемой дисфункцией ЦНС. Сложность заключается в том, что не существует надежных инструментальных способов оценки функции. Поэтому применяют клинические критерии, подобные тем, которые используются в психиатрии . Благодаря совершенствованию клинических критериев диагностики СРК и других ФНК можно предотвратить грубые ошибки диагностики и уменьшить число ненужных диагностических исследований. Так, клиническим критериям СРК соответствует дискомфорт в животе или боль, которые имеют не менее двух из трех следующих характеристик: а) уменьшение после дефекации; и/или б) связь с изменением частоты стула; и/или в) с изменением формы стула.
Функциональный метеоризм, функциональный запор и функциональная диарея предполагают изолированное ощущение вздутия живота или нарушение стула. Согласно Римским критериям III ФНК должны продолжаться не менее 6 месяцев, из них 3 месяца - непрерывно. При этом психоэмоциональные нарушения могут отсутствовать.
Непреложным условием также является соблюдение правила: не относить к больным ФНК лиц, у которых имеются тревожные симптомы, часто встречающиеся при воспалительных, сосудистых и опухолевых заболеваниях кишечника.
К ним относятся кровотечения, снижение веса тела, хроническая диарея, анемия, лихорадка, начало болезни у лиц старше 50 лет, рак и воспалительные заболевания кишечника у родственников и ночная симптоматика.
Соблюдение этих условий позволяет с большой долей вероятности установить функциональное заболевание, исключив болезни, при которых нарушения функции вызываются воспалительными, анатомическими, метаболическими и неопластическими процессами.
По степени тяжести ФНК условно подразделяют на три степени: легкую, среднюю и тяжелую.
Пациенты с легкой степенью функциональных нарушений не отягощены психоэмоциональными проблемами. Они обычно отмечают хотя и временный, но положительный результат от назначенного лечения.
Больные со средней степенью тяжести в той или иной мере неустойчивы в психологическом отношении и требуют специального лечения.
Тяжелая степень функциональных нарушений отличается связью с психосоциальными трудностями, сопутствующими психоэмоциональными нарушениями в форме тревоги, депрессии и др. Эти пациенты стремятся часто общаться с гастроэнтерологом, хотя и не верят в возможность выздоровления.
Пробиотические продукты питания в лечении ФНК
Пробиотики и содержащие их продукты с каждым годом находят все большее применение в лечении заболеваний кишечника. Их включение в пищевой рацион обеспечивает организм энергетическим и пластическим материалом, положительно влияет на функции кишечника, смягчает воздействие стрессов и снижает риск развития многих заболеваний . В целом ряде стран организация функционального питания стала государственной политикой в области здравоохранения и пищевой промышленности .
Одной из разрабатываемых в последние годы категорий функционального питания являются пробиотические продукты, содержащие бифидобактерии, молочнокислые бактерии и пищевые волокна.
С 1997 году компанией Данон выпускаются кисломолочные продукты "Активиа", обогащенные пробиотическим штаммом Bifidobacterium animalis штамм DN-173 010 (коммерческое название ActiRegularis). Высокая концентрация (не менее 108 КОЕ/г) остается стабильной в продукте в течение всего срока годности. Были проведены специальные исследования по оценке выживаемости Bifidobacterium ActiRegularis в кишечнике человека. Установлена достаточно хорошая выживаемость бактерий в желудке (снижение концентрации бифидобактерий менее чем на 2 порядка в течение 90 мин) и в самом продукте на протяжении допустимого срока его хранения .
Значительный интерес представляет изучение влияния Активии и Bifidobacterium ActiRegularis на скорость кишечного транзита. В параллельном исследовании, включавшем 72 здоровых участника (средний возраст 30 лет), было отмечено, что ежедневное употребление Активии с Bifidobacterium ActiRegularis сокращало время транзита в толстой кишке на 21% и в сигмовидной кишке на 39% по сравнению с людьми, принимавшими продукт, не содержащий бактерий .
По нашим данным, у 60 больных СРК с преобладанием запоров, получавших Активию, к концу второй недели прекращались запоры, существенно сокращалось время транзита карболена (у 25 больных - с 72 до 24 ч, а у 5 - с 120 до 48 ч). Одновременно уменьшались болевой синдром, метеоризм, вздутие и урчание в животе. К концу третьей недели у больных выросла концентрация бифидо- и лактобактерий в кишечнике, уменьшилось число гемолизирующей кишечной палочки, клостридий и протея . Полученные результаты позволили рекомендовать Активию для лечения больных СРК с запорами.
В 2006 году D. Guyonnet с соавт. использовали Активию в течение 6 недель для лечения 267 пациентов с СРК . В контрольной группе больные получали термически обработанный продукт. Установлено, что к концу второй недели употребления Активиа частота стула была достоверно больше в сравнении с термизированным продуктом; через 3 недели у больных, употреблявших Активию, достоверно чаще исчезал абдоминальный дискомфорт.
Таким образом, проведенное исследование показало, что Активиа уменьшает выраженность симптомов у больных СРК и повышает качество их жизни. Наиболее выраженный положительный эффект отмечет в подгруппе больных с частотой стула менее 3 раз в неделю.
Резюмируя данные представленных исследований, можно утверждать, что Активиа, содержащая Bifidobacterium ActiRegularis, является достаточно эффективным средством восстановления и нормализации моторики и микрофлоры кишечника у пациентов с СРК.
Заключение
Особенностями функциональных заболеваний кишечника являются связь с психоэмоциональными и социальными факторами, широкая распространенность и отсутствие эффективных способов лечения. Эти особенности выдвигают проблему ФНК в число наиболее актуальных в гастроэнтерологии.
Становится все более очевидным, что в лечении больных с тяжелым течением ФНК основное значение должны играть антидепрессанты. Трициклические антидепрессанты, ингибиторы рецепторов серотонина и адреналина имеют важное значение в борьбе с болью, т.к. не только уменьшают немотивированную тревогу и связанную с ней депрессию, но и воздействуют на центры аналгезии. При достаточно отчетливом эффекте лечение можно продолжать до года и лишь затем постепенно снижать дозу . Поэтому лечение подобных больных должно осуществляться совместно с психиатром.
Для лечения больных с менее тяжелыми формами ФНК, как показывает опыт, в том числе и наш, хороший результат удается получить с помощью пробиотиков и продуктов функционального питания. Особенно хороший эффект можно видеть в лечении больных постинфекционным СРК. Причина этого кроется в непосредственной связи этиологии и патогенеза заболевания с нарушениями микробиоценоза кишечника.
Литература
1. Drossman D.A.The Functional Gastrointestinal Disorders and the Rome III Process.Gastroenterology 2006;130:5:1377-1390
2. Yeo A, Boyd P, Lumsden S, Saunders T, Handley A, Stubbins M, et al.. Association between a functional polymorphism in the serotonin transporter gene and diarrhoea predominant irritable bowel syndrome in women. Gut. 2004;53:1452-1458
3. Kim HJ, Camilleri M, Carlson PJ, Cremonini F, Ferber I,Stephens D, et al.. Association of distinct alpha(2) adrenoceptor and serotonin transporter polymorphisms with constipation and somatic symptoms in functional gastrointestinal disorders. Gut. 2004;53:829-837
4. Caspi A, Sugden K, Moffitt TE, Taylor A, Craig IW, Harrington H, et al.. Influence of life stress on depression (moderation by a polymorphism in the 5-HTT gene 57). Science. 2003;301:386-389
5. Levy RL, Jones KR, Whitehead WE, Feld SI, Talley NJ, Corey LA. Irritable bowel syndrome in twins (heredity and social learning both contribute to etiology). Gastroenterology. 2001;121:799-804
6. Drossman DA. Functional GI disorders (what’s in a name?). Gastroenterology. 2005;128:1771-1772
7. Murray CD, Flynn J, Ratcliffe L, Jacyna MR, Kamm MA, Emmanuel AV. Effect of acute physical and psychological stress on gut autonomic innervation in irritable bowel syndrome. Gastroenterology. 2004;127:1695-1703
8. Tache Y. Corticotropin releasing factor receptor antagonists (potential future therapy in gastroenterology?). Gut. 2004;53:919-921
9. Parkman HP, Hasler WL, Fisher RS. American Gastroenterological Association technical review on the diagnosis and treatment of gastroparesis. Gastroenterology. 2004;127:1592-1622
10. Drossman DA, Camilleri M, Mayer EA, Whitehead WE. AGA technical review on irritable bowel syndrome. Gastroenterology. 2002;123:2108-2131
11. Jones MP, Dilley JB, Drossman D, Crowell MD. Brain-gut connections in functional GI disorders: anatomic and physiologic relationships. Neurogastroent Motil 2006;18:91-103
12. Delgado-Aros S, Camilleri M. Visceral hypersensitivity 2. J Clin Gastroenterol. 2005;39:S194-S203
13. Gershon MD. Nerves, reflexes, and the enteric nervous system (pathogenesis of the irritable bowel syndrome 2). J Clin Gastroenterol. 2005;39:S184-S193
14. Dunlop SP, Coleman NS, Blackshaw E, Perkins AC, Singh G, Marsden CA, et al.. Abnormalities of 5-hydroxytryptamine metabolism in irritable bowel syndrome. Clin Gastroenterol Hepatol. 2005;3:349-357
15. Chadwick VS, Chen W, Shu D, Paulus B, Bethwaite P, Tie A, et al.. Activation of the mucosal immune system in irritable bowel syndrome. Gastroenterology. 2002;122:1778-1783
16. Dunlop SP, Jenkins D, Neal KR, Spiller RC. Relative importance of enterochromaffin cell hyperplasia, anxiety, and depression in postinfections IBS. Gastroenterology. 2003;125:1651-1659
17. Gwee KA, Collins SM, Read NW, Rajnakova A, Deng Y, Graham JC, et al.. Increased rectal mucosal expression of interleukin 1beta in recently acquired post-infectious irritable bowel syndrome. Gut. 2003;52:523-526
18. McKendrick W, Read NW. Irritable bowel syndrome- post-salmonella infection. J Infection. 1994;29:1-4
19. Gwee KA, Leong YL, Graham C, McKendrick MW, Collins SM, Walters SJ, et al.. The role of psychological and biological factors in post-infective gut dysfunction. Gut. 1999;44:400-406
20. Mearin F, Perez-Oliveras M, Perello A, Vinyet J, Ibanez A, Coderch J, et al.. Dyspepsia after a Salmonella gastroenteritis outbreak (one-year follow-up cohort study). Gastroenterology. 2005;129:98-104
21. Парфенов А.И., Ручкина И.Н., Екисенина Н.И. Антибактериальная терапия при синдроме раздраженного кишечника. Клин.мед.1996:5:41-43
22. Ручкина И.Н., Белая О.Ф., Парфенов А.И. и др. Роль Campylobacter jejunum в патогенезе синдрома раздраженного кишечника. Российский гастроэнтерологический ж-л.2000:2: 118-119
23. Парфенов А.И. Постинфекционный синдром раздраженного кишечника:вопросы лечения и профилактики. Consilium medicum 2001:6;298-300
24. Парфенов А.И., Ручкина И.Н., Осипов Г.А., Потапова В.Б. Постинфекционный синдром раздраженного кишечника или хронический колит? Материалы V съезда общества гастроэнт. России и XXXII сессии ЦНИИГ, Москва 3-6 февраля 2005 г.-М.: Анахарсис, 2005.-С 482-483
25. Парфенов А.И., Ручкина И.Н. Постинфекционный синдром раздраженного кишечника. Избранные главы клинической гастроэнтерологии: сб.трудов/Под ред Лазебника.-М.:Анахарсис, 2005. Раздел 3.Болезни кишечника. С 277-279
26. Ручкина И.Н. Роль острых кишечных инфекций и нарушений микробиоценоза в этиологии и патогенезе синдрома раздраженного кишечника. Автореф. Дисс. докт. М.2005, 40 с
27. Pimentel M, Chow EJ, Lin HC. Eradication of small intestinal bacterial overgrowth reduces symptoms of irritable bowel syndrome. Am J Gastroenterol. 2000;95:3503-3506
28. O’Mahony L, McCarthy J, Kelly P, Hurley G, Luo F, O’Sullivan G, et al.. Lactobacillus and bifidobacterium in irritable bowel syndrome (symptom responses and relationship to cytokine profiles). Gastroenterol. 2005;128:541-551
29. Saito YA, Schoenfeld P, Locke GR. The epidemiology of irritable bowel syndrome in North America (a systematic review). Am J Gastroenterol. 2002;97:1910-1915
30. Wigington WC, Johnson WD, Minocha A. Epidemiology of irritable bowel syndrome among African Americans as compared with whites (a population-based study). Dig Dis. 2005;3:647-653
31. Thompson WG, Irvine EJ, Pare P, Ferrazzi S, Rance L. Functional gastrointestinal disorders in Canada (first population-based survey using Rome II criteria with suggestions for improving the questionnaire). Dig Dis Sci. 2002;47:225-235
32. American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders- DSM-IV. 4th ed.. Washington, DC: American Psychiatric Association; 1994
33. Шендеров Б.А. Медицинская и микробная экология и функциональное питание. Т.3: Пробиотики и функциональное питание. М.:Грантъ, 2001.-286с
34. Хавкин А.И. Микрофлора пищеварительного тракта. М.:Фонд социальной педиатрии, 2006.- 416с
35. Berrada N, et al. Bifidobacterium from fermented milks: Survival during gastric transit. J. Dairy Sci. 1991; 74: 409-413
36. Bouvier M, et al. Effects of consumption of a milk fermented by the probiotic Bifidobacterium animalis DN-173 010 on colonic transit time in healthy humans. Bioscience and Microflora, 2001,20(2): 43-48
37. Парфенов А.И., Ручкина И.Н. Профилактика и лечение запоров пробиотиками. Фарматека, 2006; 12 (127): 23-29
38. D.Guyonnet, O. Chassany, P. Ducrotte et al. Effect of a fermented milk containing Bifidobacterium animalis DN-173 010 on bloating and health-related quality of life in Irritable Bowel Syndrome (IBS) adult patients - A randomized, double-blind, controlled trial. Poster presentation at the Neurogastroenterology and Motility Joint international Meeting, September 14-17, 2006, Boston
Согласно статистических данных около 20% населения страдают от разнообразных проявлений дисфункции желудочно-кишечного тракта, в структуру которого непосредственно входит и кишечник. К наиболее распространенным заболевания относится расстройство кишечника или так называемый «синдром раздраженного кишечника».Содержание:
Этиология заболевания
Функциональное нарушение работы кишечника – это патологический процесс в организме, связанный с сбоем работы органа. Характеризуется хронической абдоминальной болью, дискомфортными ощущениями, вздутием живота и нарушениями в поведении кишечника при отсутствии конкретных факторов.
Расстройство кишечника проявляется в любом возрасте независимо от половых признаков. Причин для появления данного патологического процесса в организме существует множество, среди которых стоит выделить следующие:
В случае проведения хирургической терапии отдельных органов желудочно-кишечного тракта.
Длительная терапия с использованием антибиотиков, противосудорожных, противоопухолевых и гормональных, наркотических и других лекарственных средств.Нерациональный прием медикаментозных препаратов.

Наличие вредных привычек: табакокурение, алкоголь, стимулирующие чрезмерную выработку желудочного сока.
Также одним из факторов, способствующих появлению функционального расстройства кишечника, является употребление продуктов питания и воды из отдельных регионов во время командировки или путешествий.
К основным причинам развития дисфункции кишечника у детей стоит отнести: кишечные инфекции и палочки, сальмонелез и другие виды пищевой токсикоинфекции.
В связи с тем, что факторов, способствующих развитию функционального нарушения работы кишечника, существует множество, и все они различные по уровню опасности для жизни и здоровья больных, не рекомендуется заниматься самостоятельным лечением данного недуга.
В первую очередь для успешной терапии необходимо исключить наличие вероятных причин, которые могут вызывать нарушения работы кишечника. Соответственно очень важно придерживаться правильного сбалансированного рациона, полноценного отдыха и систематических силовых нагрузок.
Факторы, обуславливающие проявление расстройства кишечника
Самостоятельно диагностировать функциональное расстройство кишечника на начальном этапе значительно проблематично, а в большинстве случаев просто невозможно. Это связано с тем, что данное заболевание является функциональным и именно поэтому его достаточно сложно подтвердить при помощи целого ряда диагностических процедур и лабораторных обследований.
Единственным характерным фактором, указывающим на наличие кишечных расстройств, является ярко выраженные дискомфортные ощущения, которые объединяют все патологические процессы в организме.

Помимо характерных проявлений функциональное расстройство кишечника достаточно часто сопровождается симптоматикой хронической интоксикации. Она проявляется в наличии головных болей, слабости, повышенном потоотделении, нарушении дыхания и спазмировании живота.
Также дисфункция кишечника сопровождается развитием кожных заболеваний (псориаз, высыпания, угри). Наблюдается снижение эластичности хрящевой ткани и ускоряется процесс старения в организме.
При хронической форме заболевания у больного наблюдается возникновение артритов, дисбаланс в деятельности сердечно-сосудистой системы, образование камней в почках, частые судороги, скачки артериального давления и развитие вегетососудистой дистонии.

В каждом индивидуальном случае, в зависимости от вида патологии и стадии ее протекания, симптоматика дисфункции кишечника у каждого больного разная. Наличие всех признаков данного недуга одновременно исключено.
Если дискомфортные ощущения сохраняются длительный период при этом, не снижая свою интенсивность, а только прогрессируя необходимо немедленно обратится на консультативный осмотр врача и пройти полное обследование.
Функциональное нарушение работы кишечника у детей
Дисфункция кишечника у ребенка – является достаточно распространенным патологическим процессом. Достаточный уровень информации о причинах возникновения данного недуга позволит родителям своевременно выявить первые симптомы и оказать помощь своему чаду в любом возрасте.
Основные причины дисбаланса в работе кишечника:
- Развитие органов пищеварительной системы на недостаточном уровне, которые еще не адаптированы к естественному усвоению отдельных продуктов питания. В большинстве случаев относится к детям грудничкового возраста.
- Этиология дисфункции у пациентов старшего возраста аналогична взрослым причинам. К ним стоит отнести психосоматическое состояние, инфицирование организма и органов ЖКТ разнообразными болезнетворными микроорганизмами.
- Протекание недуга у детей существенно отличается от взрослых. Это связано с тем, что детский организм тяжелее переносит диарею и сопровождающие ее симптомы.
- Продолжительность заболевания значительно превышает сроки и не ликвидируется естественным путем без вмешательства из вне. Без медикаментозной помощи нормализовать функционирование кишечника у малыша будет невозможно. Запускать заболевание нельзя, так как высока вероятность того, что обычный понос может трансформироваться в дисбиоз.

Сбои в работе пищеварительной системы, способствую развитию дисбаланса многих метаболических процессов, что в свою очередь значительно ухудшает общее состояния здоровья.
Характерная симптоматика у детей:
- Ослабление иммунной системы
- Слабость, вялость
- Чрезмерная раздражительность
- Снижение внимательности
Природа данного заболевания у детей носит инфекционный и неинфекционный характер. Только после досконального обследования и установления причины расстройства, лечащим врачом, исключительного детского профиля, назначается лечение.
Диагностирование заболевания
В случае если дисфункции кишечника стали систематичным явлением в работе вашего организма, необходимо немедленно записаться на прием к профилирующему специалисту. Начинать поход по врачам рекомендуется с терапевта, который осуществит первичный осмотр и выдаст направление на консультативный осмотр к узкому специалисту.
Это могут быть:
- Гастроэнтеролог – специализируется на заболеваниях органов желудочно-кишечного тракта. По результатам гастроэнтерологического обследования установит причины заболевания и назначит эффективные методы терапии.
- Диетолог – поможет грамотно сбалансировать диетическое питание в рамках диагностированного заболевания.
- Проктолог – главная специализация основана на патологических процессах толстой кишки, негативно воздействующих на нормальное функционирование ЖКТ.

Основным манипуляциям диагностирования:
- Консультативный осмотр врачей узких специализаций
- Физикальное обследование
- Интервьюирование
- Общий анализ мочи и крови
- Копрограмма
- Ультразвуковое исследование внутренних органов
- Колоноскопия кишечника
- Ректоскопия
- Ирригоскопия
- Компьютерная томография
- Биопсия кишечника
Данный комплекс способов обследования включает максимально развернутую информацию. В каждом отдельном случае врачами устанавливается необходимый спектр диагностирующих процедур для определения заболевания и назначения правильного лечения. Диагностика функционального нарушения работы кишечника основана на применении эксклюзивного метода исключения.
По результатам обследования определяется причина и степень тяжести заболевания с последующим назначением правильной терапии. Приблизительно около 20% пациентов страдают хроническим расстройством кишечника, связанным с психосоматическим состоянием человека. В таких случаях лечение состоит из курса психотерапии и обязательного изменения привычного образа жизни.
Лечение различных форм дисфункции кишечника
Залогом успешного лечения дисфункций кишечника является определение с последующей ликвидацией всех причин ее появления. Также особое внимание уделяется нормализации функционирования всех органов пищеварительной системы.
Методы лечения, используемый при расстройствах кишечника:
- Терапевтический способ: определение диетического питания, медитации, коррекция образа жизни, посещение психиатра.
- Медикаментозная терапия: назначается при тяжелых формах протекания данного заболевания, в зависимости от характерных проявлений заболевания. Это могут быть скрепляющие, слабительные, антибактериальные препараты, спазмолитики. Если нарушения в работе кишечника вызваны соматическими расстройствами, назначается курс приема антидепрессантов, нейролептиков.

Физиотерапевтический комплекс состоит из:
- Аутогенных тренировок
- Плавания в бассейне
- Проведения специальной ЛФК
- Криомассажи
- Углекислые и бишофитные ванны
- Интерференционные токи
- Иглоукалывание
- Фитотерапия
- Низкоинтенсивной импульсной биосинхронизированной магнитотерапии
- Использования ректальных тампонов с сульфидной либо тамбуканской грязью в сочетании с рефлекторно-сегментарными аппликациями
- Электрофорез и так далее в зависимости от формы протекания заболевания
Альтернативные методы лечения заключаются в употреблении различных натуральных настоек и отваров. К максимально эффективным стоит отнести следующее: перечную мяту, высушенную пленку куриного желудка, ромашку, кору дуба, порошок корицы, сухие перегородки грецких орехов, пижма, коренья лапчатки прямостоячей.
Но стоит помнить о том, что лечение должно быть назначено исключительно врачом. И только комплексный подход к лечению, после установления причины заболевания, позволит в кротчайшие сроки восстановить свое здоровье.
Также не стоит забывать о том, что методы народной медицины при грамотном подборе могут быть эффективными только на ранних стадиях развития заболевания.
При хронической либо тяжелой форме данного недуга исключительной употребление средств альтернативной медицины может только навредить здоровью, усугубив общую картину.
Во время просмотра видео Вы узнаете о еде для кишечника.
Дисфункция кишечника является достаточно распространенным заболеванием, которое поражает организм каждого человека на протяжении жизни. Своевременнее диагностирование и правильно подобранное лечение, подкрепленное специальным диетическим питанием, позволит в кротчайшие сроки победить данный недуг, нормализовав все процессы в организме.
improvehealth.ru
Дисфункция кишечника: причины и лечение заболевания, а также его особенности у детей
Приблизительно пятая часть взрослого населения планеты, как говорит статистика, страдает от различных проявлений дисфункции кишечника. Это заболевание возникает при некоторых нарушениях работы кишечника и часто называется расстройством кишечника либо же «синдромом раздраженного кишечника».
Проявляется оно в виде болей в животе и нарушений стула, для возникновения которых нет определенных причин. Данное заболевание является функциональным и по этой причине, редко подтверждается с помощью различных лабораторных анализов.
Причины и симптомы дисфункции кишечника

Внутренние органы человека: кишечник
Дисфункция кишечника проявляется у людей всех возрастов: от детей, до людей в зрелом возрасте. Наиболее частой причиной для развития заболевания является постоянное стрессовое состояние больного. Также причинами для развития дисфункции кишечника могут быть:
Помимо различных инфекционных заболеваний, причиной для возникновения дисфункции кишечника может быть индивидуальная непереносимость определенных продуктов из рациона. Поэтому, в ряде случаев, заболевание возникает после неумеренного употребления жирной пищи или продуктов, в которых содержится большое количество клетчатки.
Порой аллергические реакции на некоторые продукты могут вызвать дисфункцию кишечника. Также, она возникает при употреблении несовместимых между собой продуктов или плохой, некачественной пищи. Важно помнить о том, что по мере развития патологии в кишечнике, в нем начинают появляться токсины, которые плохо влияют на весь организм больного.
Дисфункция кишечника у женщин может появляться по особенным причинам. Она возникает во время менструального цикла, вследствие различных гормональных нарушений, которые иногда могут появляться. Расстройство кишечника характеризуется различными негативными симптомами. К ним относятся:
- вздутие живота
- болевые ощущения в области кишечника
- диарея
- запор
Поэтому, если в ходе какого-либо обследования не выявляется объективная причина для возникновения любого из вышеперечисленных симптомов, то они могут быть вызваны именно дисфункцией кишечника. Боли, в области живота, чаще всего появляются утром, после сна. Они характеризуются различной интенсивностью и могут быть как терпимыми, так и достаточно сильными.
Также в утреннее время суток больной может страдать от метеоризма и постоянной диареи. Его сопровождает постоянное чувство заполненного кишечника, которое порой не пропадает даже после дефекации. Помимо всего этого, больной испытывает урчание в животе, а в стуле часто может быть обнаружена слизь.
Болевые ощущения и диарея, при дисфункции кишечника, часто могут особенно ярко проявляться после приема пищи или во время стресса. Некоторые люди могут испытывать тенезмы – ложные позывы к дефекации, во время которых ощущается боль или неприятные ощущения в прямой кишке.
Данные симптомы дисфункции кишечника могут по-разному проявляться у различных пациентов: у кого-то они ярко выражены, у кого-то наоборот. Тем не менее, если какие-либо симптомы все-таки возникают, то это вполне объективный повод обратиться к специалисту.
Читайте: Лимфома кишечника: симптомы, которые должны насторожить
Расстройство кишечника – заболевание, для возникновения которого есть ряд причин. Оно сопровождается различными симптомами, проявление которых у разных людей по-разному выражено. Наиболее распространенными из них являются: запор, диарея, болевые ощущения в области живота. В случае возникновения этих симптомов желательно обратиться за консультацией к специалисту.
Лечение дисфункции кишечника
Врачу необходимо установить причину дисфункции кишечника
Прежде, чем заниматься лечением дисфункции кишечника, врач должен определить причину заболевания. Если причиной для его развития послужил длительное стрессовое состояние, то лечащий врач может порекомендовать больному различные релаксирующие занятия: йога, бег, пробежки, прогулка на свежем воздухе.
Они способствуют расслаблению организма и стабилизируют состояние нервной системы. Если же стрессовое состояние не проходит и сопровождает больного очень длительное время, то ему могут быть приписаны различные успокоительные препараты и антидепрессанты.
Если же причины возникновения дисфункции кишечника заключается в чем-то другом, то в зависимости от них могут быть назначены следующие лекарственные средства:
Для удаления болевых ощущений при дисфункции кишечника, часто используется спарекс, ниаспам, дюспаталин и т.д. Они оказывают расслабляющее воздействие на кишечник и способствуют нормальному его сокращению. Тем не менее, в некоторых случаях их применение запрещается, поскольку они содержат масло перечной мяты, которое нельзя принимать женщинам во время беременности.

Дисфункция кишечника носит еще одно название – синдром раздраженного кишечника
Слабительные препараты размягчают кал и способствуют нормализации процесса дефекации. Принимая эти лекарственные средства больной должен употреблять большое количество жидкости, дабы защитить организм от обезвоживания. Дисфункция кишечника, сопровождающаяся диареей, потребует применения различных связывающих препаратов, например, имодиума и лоперамида.
Они замедляют перистальтику кишечника и увеличивают длительность нахождения каловых масс в нем. В результате этого, жидкие каловые массы имеют больше времени, чтобы загустеть и опорожнение кишечника нормализуется.
При расстройстве кишечника рекомендуется следование различным диетам, терапевтическое воздействие которых аналогично воздействию лекарственных препаратов. Пациентам, которые страдают от запоров, необходимо принимать больше жидкости, есть отрубной хлеб, различные масла, рыбу, мясо, каши. В то же время им крайне нежелательно употреблять кофе, какое, кисели, шоколады и выпечку из сдобного теста.
При диарее, из рациона больного следует исключить пищу, ускоряющую перистальтику кишечника и процесс его опорожнения. В рацион может входить кофе, чай, сухое печенье. Рекомендуется употребление кефира и творога, а яйца и мясо – на некоторое время исключаются.
К пище могут добавляться специальные добавки, содержащие полезные бактерии, способствующие нормализации работы кишечника.
Лечение дисфункции кишечника производится в зависимости от причин, которыми было вызвано заболевание. Если причина заболевания – стресс, то рекомендуются занятия и препараты, оказывающие успокаивающее воздействие на нервную систему. При запорах и диарее рекомендуется прием специальных лекарственных средств и различные диеты, способствующие нормализации функций кишечника.
Дисфункция кишечника у ребенка

Дисфункция кишечника бывает довольно часто у пациентов гастроотделений
Расстройство кишечника у детей – довольно частое заболевание, поэтому родителям необходимо знать, чем оно может быть вызвано. У детей малого возраста, расстройства кишечника могут быть обусловлены недостаточным развитием системы пищеварения, не приспособленной к нормальному усвоению некоторых продуктов. Дети постарше могут страдать от дисфункции кишечника по тем же причинам, что и взрослые.
Различия в том, что у детей и взрослых заболевание проходит с некоторыми различиями. Дети хуже переносят диарею и симптомы, которые ее сопровождают. Дисфункция кишечника у детей длится дольше, чем у взрослого и не проходит самостоятельно. Организму малыша необходима помощь для борьбы с заболеванием. Родителям следует внимательно следовать предписаниям врача-педиатра, поскольку есть опасность того, что обычная диарея перерастет в дисбактериоз, а это уже намного более серьезное заболевание.
Читайте: Функциональные заболевания жкт: самые распространенные
Отклонения от нормального функционирования пищеварительной системы приводит к нарушению различных обменных процессов, что приводит к общему ухудшению состояния всех систем организма. Из них можно выделить:
- снижение иммунитета
- снижение внимания и памяти малыша
- вялость
- повышенная раздражительность
У детей данное заболевание может иметь инфекционную, либо неинфекционную природу. Первые более просты в диагностике и лечении, а вот вторые потребуют более серьезного анализа симптомов и проведения различных тестов. При диарее неинфекционного типа, лечащим врачом могут быть прописаны препараты, предназначенные для борьбы с микробами: наиболее вероятными виновниками возникновения расстройства. Неадекватное лечение диареи у малыша может привести к возникновению острой формы заболевания, которая обычно проходит в течение недели.
Дисфункция кишечника имеет много дополнительных симптомов
В тех случаях, когда диарея и сопутствующие ей симптомы длятся дольше обычного срока, возможно проявление хронического расстройства кишечника. Эта форма заболевания характеризуется тем, что даже после того, как диарея прекращается, возможны единичные случаи проявления тошноты и рвоты, резкие подъемы температуры у малыша.
Диарея у детей постарше может быть вызвана неправильным рационом, отсутствием в нем различных витаминов, отравлениями плохими продуктами питания, инфекциями и аллергическими реакциями. Если понос имеет продолжительность более суток, то крайне желательно обратиться за помощью к врачу-специалисту.
Эти симптомы могут быть вызваны некоторыми заболеваниями детей (скарлатина, корь), которые не рекомендуется лечить самостоятельно, поскольку это опасно для ребенка. Лечащий врач проведет необходимую диагностику и назначит правильное лечение. Расстройство кишечника у детей различается в зависимости от их возраста. Так, у детей до года, оно может быть вызвано недостаточным развитием системы пищеварения, а у детей постарше причины для дисфункции кишечника могут быть аналогичны причинам этого заболевания у взрослых.
В случае возникновения различных симптомов патологии у ребенка, нужно обязательно обращаться к врачу, поскольку самолечение в этом случае может быть опасным для здоровья малыша.
Дисфункция кишечника – заболевание, от которого страдает до 20% взрослого населения планеты. Оно может характеризоваться различными симптомами: боли в области живота, запоры, поносы. При лечении заболевания необходимо правильно установить его причину, и после этого назначать адекватный курс лечения, подкрепленный специальной диетой.
Нарушения функционирования кишечника у детей несколько опаснее, чем у взрослых, особенно если ребенок возрастом меньше одного года. Лечения заболевания в этом случае обязательно нужно проводить только в зависимости от рекомендаций врача-специалиста.
Синдром раздраженного кишечника – тема видеоматериала:
Расскажите друзьям! Расскажите об этой статье своим друзьям в любимой социальной сети с помощью социальных кнопок. Спасибо!
pishhevarenie.com
Функциональные заболевания кишечника у детей
Профессор А.И. Хавкин, Н.С. Жихарева
НИИ педиатрии и детской хирургии МЗ РФ, Москва МГМСУ им. Н.А. Семашко
Функциональные нарушения (ФН) желудочно–кишечного тракта занимают одно из ведущих мест в структуре патологии органов пищеварения. Так, например, рекуррентные абдоминальные боли у детей носят функциональный характер у 90–95% детей и лишь у 5–10% связаны с органической причиной. Примерно в 20% случаев в основе хронической диареи у детей также лежат функциональные расстройства. Диагностика ФН часто вызывает значительные трудности у практических врачей, приводя к большому числу ненужных обследований, а главное – к нерациональной терапии. При этом, часто приходится сталкиваться не столько с незнанием проблемы, сколько с ее непониманием.
Согласно современным представлениям, ФН это многовариантная комбинация гастроинтестинальных симптомов без структурных или биохимических нарушений (D.A. Drossman, 1994).
ФН чаще всего обусловлены нарушением нервной и гуморальной регуляции деятельности пищеварительного тракта. Они имеют разное происхождение и могут возникать вследствие заболеваний или патологических состояний нервной системы: незрелость нервномышечной передачи, повреждение (ишемия или кровоизлияния) ствола мозга и верхнешейных отделов спинного мозга, травмирование верхнешейного отдела, внутричерепная гипертензия, миелодисплазия, инфекция, опухоль, аневризма сосудов и др.
Попытка создать классификацию функциональных расстройств в детском возрасте была предпринята Комитетом по изучению функциональных расстройств у детей и Международной рабочей группой по разработке критериев функциональных расстройств (Римская группа II) совместно с сотрудниками клиники Монреальского Университета (Committee on Childhood Functional Gastrointestinal Disorders, Multinational Working Teams to Develop Criteria for Functional Disorders , University of Monreal, Quebec, Canada). Данная классификация построена по клиническим критериям, в зависимости от преобладающих симптомов:
Синдром раздраженного кишечника
К кишечным функциональным нарушениям согласно МКБ10 относится синдром раздраженного кишечника (СРК). В эту же группу отечественные авторы относят функциональный метеоризм, функциональный запор, функциональную диарею.
СРК функциональное кишечное расстройство, проявляющееся абдоминальным болевым синдромом и/или нарушениями дефекации и/или метеоризмом. СРК одно из очень частых заболеваний в гастроэнтерологической практике: 4070% пациентов, обращающихся к гастроэнтерологу, имеют СРК. Он может проявляться в любом возрасте, в т.ч. у детей. Соотношение девушек и юношей 24:1.
Ниже приводятся симптомы, на основе которых можно диагностировать СРК (Рим, 1999):
Болевой синдром характеризуется многообразием проявлений: от диффузных тупых болей до острых, спазматических; от постоянных до пароксизмов болей в животе. Длительность болевых эпизодов – от нескольких минут до нескольких часов. Помимо основных «диагностических» критериев, у больного могут наблюдаться следующие симптомы: учащение мочеиспускания, дизурия, никтурия, дисменорея, утомляемость, головная боль, боль в спине. Изменение психической сферы в виде тревожных и депрессивных расстройств встречается у 40–70% больных с синдромом раздраженного кишечника.
В 1999 г. в Риме были разработаны диагностические критерии синдрома раздраженного кишечника. Это наличие абдоминального дискомфорта или болей в течение 12 необязательно последовательных недель за последние 12 месяцев, в сочетании с двумя из следующих трех признаков:
СРК является диагнозом исключения, но для полной диагностики больному необходимо провести массу инвазивных исследований (колоноскопия, холецистография, пиелография и т.п.), поэтому очень важно провести тщательный сбор анамнеза у больного, выявить симптомы и после этого провести необходимые исследования.
Функциональные абдоминальные боли
В различных классификациях этот диагноз занимает разное место. По мнению D.A. Drossman, функциональные абдоминальные боли (ФАБ) являются самостоятельным вариантом ФН ЖКТ. Некоторые врачи рассматривают ФАБ в рамках язвенноподобного типа функциональной диспепсии или как вариант СРК. Согласно классификации, разработанной Комитетом по изучению функциональных расстройств у детей, ФАБ рассматривается как расстройство, проявляющиеся абдоминальными болями, наряду с функциональной диспепсией, синдромом раздраженной кишки, абдоминальной мигренью и аэрофагией.
Данное заболевание очень распространено. Так, по данным H.G. Reim et al., у детей с абдоминальной болью в 90% случаев нет органического заболевания. Преходящие эпизоды болей в животе встречаются у детей в 12% случаев. Из них только в 10% удается найти органическую основу этих абдоминалгий.
В клинической картине превалируют жалобы на абдоминальную боль, которая чаще локализуется в околопупочной области, но может отмечаться и в других регионах живота. Интенсивность, характер боли, частота атак очень вариабельны. Сопутствующими симптомами являются снижение аппетита, тошнота, рвота, диарея, головные боли; запоры бывают редко. У этих больных так же, как у пациентов с СРК отмечается повышенное беспокойство и психоэмоциональные нарушения. Из всей клинической картины можно выделить характерные симптомы, основываясь на которых можно поставить диагноз ФАБ:
В плане диагностики надо отметить, что это, как и другие ФН ЖКТ, ФАБ, является диагнозом исключения, причем очень важно исключить не только другую патологию пищеварительной системы пациента, но и патологию мочеполовой и сердечно–сосудистой систем.
У детей первого года жизни диагноз функциональные абдоминальные боли не ставится, а состояние с похожими симптомами называют детскими коликами, т.е. неприятное, часто вызывающее дискомфорт чувство распирания или сдавливания в брюшной полости у детей первого года жизни.
Клинически детские колики протекают, как и у взрослых боли в животе спастического характера, но в отличие от взрослых у ребенка это выражается длительным плачем, беспокойством, сучением ножками.
Абдоминальная мигрень
Боль в животе при абдоминальной мигрени чаще всего встречается у детей и юношей, однако нередко выявляется и у взрослых. Боль носит интенсивный, диффузный характер, но иногда может быть локализована в области пупка, сопровождаться тошнотой, рвотой, поносом, побледнением и похолоданием конечностей. Вегетативные сопутствующие проявления могут варьировать от негрубых, умеренно выраженных до ярких вегетативных кризов. Длительность болей колеблется от получаса до нескольких часов или даже нескольких суток. Возможны различные сочетания с мигренозной цефалгией: одновременное появление абдоминальной и цефалгической боли, их чередование, доминирование одной из форм при одновременном их присутствии. При диагностике необходимо учитывать следующие факторы: связь абдоминальной боли с головной болью мигренозного характера, характерные для мигрени провоцирующие и сопровождающие факторы, молодой возраст, семейный анамнез, терапевтический эффект противомигренозных препаратов, увеличение скорости линейного кровотока в брюшной аорте при допплерографии (особенно во время пароксизма).
Функциональная задержка стула и функциональный запор
Запоры вызываются нарушением процессов формирования и продвижения кала по всей кишке. Запор хроническая задержка опорожнения кишечника более чем на 36 часов, сопровождающаяся затруднением акта дефекации, чувством неполного опорожнения, отхождением малого (
www.medvopros.com
Лечение кишечной дисфункции
Дисфункция кишечника диагностирована у пятой части всего населения земного шара. Болезнь проявляется в виде проблем со стулом и болезненных ощущений в животе. При этом особенных причин для подобных расстройств может быть не замечено. Из-за специфики заболевания, а его считают функциональным, обнаружить патологию с помощью лабораторного теста сложно.

Диагностика заболевания
Когда дисфункция уже становится систематическим явлением, то прием к врачу откладывать не нужно. Для начала требуется обращение к терапевту, после первичного осмотра он выдаст лист с направлением на анализы. Также, у него получают талон на консультацию узкого специалиста.
Кто занимается проблемами ЖКТ?
- Диетолог. Помогает пациенты составить план сбалансированного питания, проведет консультацию по пользе продуктов. При этом пища будет направлена на лечение патологического процесса.
- Гастроэнтеролог. Врач, который специализируется на проблемах с органами пищеварения. После того, как будет сделано дообследование, медик сможет понять причину болезни и прописать эффективную терапию.
- Проктолог. Более узкий специалист, разбирающийся в патологиях кишечника. Он способен восстановить нормальное функционирование кишечного тракта.

Комплекс обследования для определения патологии
Чтобы получить максимально точную информацию о состоянии больного придется провести достаточно исследовательских манипуляций. Для каждого пациента предполагается свой комплекс процедур, позволяющий определить заболевание и назначить лечебное питание. Диагностические меры будут направлены на исследование функционального нарушения работы органа.
После того, как результаты будут получены, специалист может узнать причину и стадию тяжести болезни. Пятая часть пациентов имеют дисфункцию кишечного тракта из-за расстройств психологического характера. В подобной ситуации предполагается проведение курса психотерапии и кардинальное изменение повседневного графика жизни.
Диагностические манипуляции:
- прием консультативного характера у медиков узких специальностей;
- интервьюирование;
- физикальное обследование;
- назначение сдачи общего анализа крови и мочи;
- копрограмма;
- ультразвуковое исследование брюшной полости и иных внутренних органов;
- ректоскопия;
- колоноскопия;
- компьютерная томография или МРТ;
- по показаниям предполагается проведение биопсии кишечника.
Если возникают спорные моменты, то возможно проведение иных процедур, позволяющих получить более картину состояния больного.

Лечение кишечных проблем
Для назначения качественной терапии при проблемах ЖКТ, требуется определение причины болезни. При условии, что на проявление симптоматики повлияло стрессовое состояние, которое длилось долгий период, то предполагается релаксирующая терапия. В нее входит пробежка, прогулки на свежем воздухе, йога, посещение приятных мероприятий.
При помощи неё организм пациента будет расслабляться, а нервная система стабилизирует свое состояние. При условии, что положительного эффекта от назначений медика нет, возможно, использование успокоительных средств и антидепрессантов.
При наличии иных причин, повлекших нарушение в работе кишечника, назначают иные группы лекарственных препаратов:
- противодиарейные средства – для устранения затяжных поносов;
- спазмолитики – способствуют снятию болевого синдрома;
- слабительные лекарства – помогут побороть запоры.
Зачастую, что снять боль, когда диагностирована дисфункция желудочно-кишечного тракта, используют Ниаспам, Спарекс или Дюспаталин. Препараты обладают расслабляющим действием и позволяют наладить нормальную систему сокращения кишечника. Иногда не рекомендовано включать в терапию лекарства из этой линейки, так как в составе присутствует перечная мята. К примеру, ее запрещено употреблять женщинам, которые вынашивают ребенка.
Под воздействием слабительного, каловые массы становятся мягкими, и процесс дефекации происходит гораздо легче. В период приема подобных лекарств организму требуется большое количество жидкости, чтобы обезопасить себя от возможного обезвоживания.

Если кишечное расстройство сопровождается диареей, то стоит употребить Имодиум или Лоперамид. За счет их действия замедляется перистальтика кишечника, а время нахождения каловой массы внутри увеличивается. Как итог, жидкое состояние кала успевает преобразоваться в более густое. Впоследствии происходит нормализация процесса дефекации.
Предполагается соблюдение определенного графика питания с иным рационом. Терапевтический эффект будет схож с тем, который дают лекарственные препараты. При условии, что у больного диагностированы запоры, ему требуется пить больше жидкости, есть хлеб из отрубей, каши, рыбу, масло. А вот от кофе, киселя, выпечки, шоколада и какао придется отказаться.
В период затяжных поносов стоит не вкушать пищу, которая ускоряет перистальтику и процесс акта дефекации. Предполагается исключение яиц, мясной продукции, но ограничения носят временный характер. Полезно включить в меню кефир, творог, сухое печенье и чай.
К питанию хорошо добавлять специальные добавки, в составе которых будут бактерии, нормализирующие работу кишечника.
Проблемы в работе кишечника у детей
Большое распространение имеет патологический процесс у детей, кишечная дисфункция у данной категории пациентов диагностируется регулярно. При условии, что родители имеют определенные знания в этой области, они достаточно быстро заметят раннюю симптоматику и окажут помощь малышу. Ребенок не всегда способен рассказать о проблеме и правильно описать ее, поэтому ответственность ложится на плечи взрослых.

Главными факторами, влияющими на появление дисбаланса, считают:
- Если речь идет о грудничках, то в данной ситуации многое сводится к тому, что пищеварительная система еще недостаточно развита. Также, ряд продукт не способен хорошо усвоиться естественным образом.
- Течение болезни имеет более тяжелое течение, в сравнении со взрослыми. Детский организм плохо переносит понос и все сопровождающие его признаки.
- Дисфункция кишечника у детей может проявиться по тем же причинам, что и у старшего поколения. Причиной развития дисбаланса может быть проблема в психосоматическом состоянии, инфекция в организме.
- Длительность болезни может носить затяжной характер, чтобы проблему купировать, требуется принять определенные меры. Без использования медикаментов невозможно побороть дисфункцию у малышей. Лечение должно быть назначено вовремя, так как в ряде случаев диарея трансформируется в дисбиоз.
Природа патологии у ребенка не всегда имеет инфекционный характер. Помочь в установке причины может только подробное обследование. Результаты анализов изучает медицинский специалист детского профиля.
Сбои в работе пищеварительной системы влекут за собой проявление дисбаланса ряда метаболических процессов. Подобное явление может сильно повлиять на общее состояние здоровья.
Симптоматика, выявленная у детей:
- излишняя раздражительность;
- ослабленная иммунная система;
- вялость;
- невнимательность.