К комбинированному лекарственному препарату анальгезирующего действия. Анальгетики (Анальгезирующие средства). При зубной боли
Анальгетики - это лекарства, способные уменьшать или устранять боль. Различают наркотические и ненаркотические анальгетики. Наркотические обезболивающие препараты назначают крайне редко по определенным показаниям. А вот к употреблению ненаркотических анальгетиков мы прибегаем часто, если нас беспокоит боль.
Особенности наркотических анальгетиков
Наркотические обезболивающие средства угнетают структуры центральной нервной системы, воспринимающие боль. Эта группа препаратов представлена агонистами опиодных рецепторов: морфин, промедол, кодеин, фентанил и прочие.
Эта группа препаратов обладает сильным обезболивающим действием. Однако наркотические анальгетики влияют не только на болевой центр, но и на другие отделы ЦНС. Так, эти лекарства угнетают дыхательный, кашлевой, сосудодвигательный, терморегуляторный центры. Кроме того, нарушается поведение человека из-за снижения самоконтроля. К наркотическим анальгетикам формируется зависимость и как следствие наркомания.
Важно! Учитывая большой спектр побочных эффектов, а также риск развития лекарственной зависимости, наркотические анальгетики могут применяться лишь только при назначении врача.
В основном к использованию этих препаратов прибегают при острой, угрожающей жизни человека боли, а также при болевом синдроме на фоне неоперабельных злокачественных новообразованиях.
Особенности ненаркотических анальгетиков
Ненаркотические обезболивающие лекарства уменьшают выраженность боли и не воздействуют на другие структуры нервной системы. Механизм их действия основан на снижении возбудимости подкоркового центра боли, повышении порога его болевой чувствительности, угнетении синтеза простагландинов - медиаторов воспаления. Благодаря такому многокомпонентному действию ненаркотические анальгетики оказывают не только болеутоляющее, но еще противовоспалительное, жаропонижающее действия.
Ненаркотические обезболивающие препараты обладают менее выраженным противоболевым эффектом в сравнении с наркотическими. Однако их действия достаточно для купирования , мышечной боли, с которой мы часто сталкиваемся. Главным преимуществом ненаркотических обезболивающих лекарств является отсутствие лекарственной зависимости к ним. Именно благодаря этим свойствам ненаркотические анальгетики широко используются в медицине.
Применение ненаркотических анальгетиков может сопровождаться развитием побочных действий:
- Ульцерогенное действие (изъязвление слизистой оболочки желудка, двенадцатиперстной кишки);
- Нефро- и гепатотоксичность.
Основными противопоказаниями к применению медикаментов из этой лекарственной группы являются язвенная болезнь, нарушения свертывания крови, печеночная и , беременность, лактация.
Обратите внимание : в аннотации ко многим обезболивающим препаратам производители указывают, что совместное применение с другими анальгетиками противопоказано. Это чревато возникновением нежелательных клинических эффектов.
Популярные обезболивающие препараты
Группа ненаркотических анальгетиков представлена большим разнообразием синтетических препаратов. Различают следующие ненаркотические анальгетики в зависимости от их происхождения:
- Производные салициловой кислоты: ;
- Производные анилина: , фенацетин;
- Производные алкановых кислот: , диклофенак натрия;
- Производные пиразолона: бутадион, анальгин;
- Производные антраниловой кислоты: мефенамовая кислота;
- Прочие: пироксикам, димексид.
Кроме того, многие фармацевтические препараты сейчас предлагают комбинированные медикаментозные препараты, в состав которых входят сразу несколько лекарственных средств.

Анальгин
 Этот препарат известен всем, он был синтезирован в 1920 году. И хотя метамизол натрия (анальгин) относится к группе НПВС, его противовоспалительное и жаропонижающее действие выражены незначительно. Зато анальгин обладает выраженным болеутоляющим эффектом.
Этот препарат известен всем, он был синтезирован в 1920 году. И хотя метамизол натрия (анальгин) относится к группе НПВС, его противовоспалительное и жаропонижающее действие выражены незначительно. Зато анальгин обладает выраженным болеутоляющим эффектом.
Анальгин быстро всасывается из желудочно-кишечного тракта, поэтому и обезболивающий эффект возникает быстро, хоть длится и не совсем долго. Анальгин применяют при , мышечной, менструальной боли, .
Важно! Опасным побочным эффектом Анальгина является развитие агранулоцитоза. Это патологическое состояние, для которого характерно критическое снижение уровня лейкоцитов за счет гранулоцитов и моноцитов, в итоге повышается восприимчивость организма к всевозможным инфекциям. Из-за этого Анальгин был изъят из оборота во многих странах. Риск возникновения агранулоцитоза при использовании Анальгина оценивается как 0,2-2 случая на миллион.
Аспирин
 Ацетилсалициловую кислоту () применяют не только лишь как обезболивающее, противовоспалительное средство. Препарат подавляет агрегацию тромбоцитов, благодаря чему используется для профилактики в. Однако необходимо учитывать тот факт, что при нарушении свертывания крови (в частности при ), возможно возникновение кровотечения.
Ацетилсалициловую кислоту () применяют не только лишь как обезболивающее, противовоспалительное средство. Препарат подавляет агрегацию тромбоцитов, благодаря чему используется для профилактики в. Однако необходимо учитывать тот факт, что при нарушении свертывания крови (в частности при ), возможно возникновение кровотечения.
Аспирин не рекомендуют использовать детям, особенно при подозрении на вирусную инфекцию. При употреблении аспирина в этом случае существует риск формирования синдрома Рея. Заболевание характеризуется быстро прогрессирующей энцефалопатией и жировой дистрофией печени. Летальность у детей с синдромом Рея составляет приблизительно 20-30%.
Важно также учитывать, что при длительном, бесконтрольном применении аспирина происходит изъязвление слизистой оболочки желудка и кишечника, а также желудочные кровотечения. Для снижения ульцерогенного действия аспирин следует применять после еды.
Кетанов
 Кетанов (кеторолак) - ненаркотический анальгетик из группы производных уксусной кислоты. Выпускается Кетанов в виде таблеток, а также раствора для внутримышечных инъекций. После внутримышечной инъекции раствора Кетанова и после приема таблетки обезболивающее действие отмечается спустя полчаса и час соответственно. А максимальный эффект достигается спустя один-два часа.
Кетанов (кеторолак) - ненаркотический анальгетик из группы производных уксусной кислоты. Выпускается Кетанов в виде таблеток, а также раствора для внутримышечных инъекций. После внутримышечной инъекции раствора Кетанова и после приема таблетки обезболивающее действие отмечается спустя полчаса и час соответственно. А максимальный эффект достигается спустя один-два часа.
Кетанов обладает выраженным болеутоляющим действием, превышая эффект от других ненаркотических обезболивающих препаратов . Поэтому неудивительно, что многим людям с выраженной зубной, головной болью удается избавиться от неприятных ощущений только с помощью Кетанова.
Помимо традиционных для ненаркотических анальгетиков побочных действий, при использовании Кетанова возможно появление побочных эффектов со стороны ЦНС (сонливость, ). Поэтому при использовании Кетанова рекомендовано избегать вождения автомобиля.
Доларен
 Это комбинированный препарат, который содержит и диклофенак натрия. Оба этих лекарственных вещества усиливают действие друг друга. После употребления таблеток Доларена максимальная концентрация действующих веществ достигается спустя час-полтора. Многие люди отмечают выраженный болеутоляющий эффект Доларена в сравнении с другими ненаркотическими обезболивающими препаратами.
Это комбинированный препарат, который содержит и диклофенак натрия. Оба этих лекарственных вещества усиливают действие друг друга. После употребления таблеток Доларена максимальная концентрация действующих веществ достигается спустя час-полтора. Многие люди отмечают выраженный болеутоляющий эффект Доларена в сравнении с другими ненаркотическими обезболивающими препаратами.
Доларен применяют при всевозможных болезнях опорно-двигательного аппарата, а также болевом синдроме любого происхождения . От применения Доларена придется отказаться при наличии реакции гиперчувствительности к каким-либо НПВС, в период после проведения операции , печеночной и , язвенных дефектах органов желудочно-кишечного тракта, желудочном кровотечении. Кроме того, препарат с осторожностью используют при наличии у человека , хронической и .
Нимесил
Действующим веществом лекарства является нимесулид - это НПВС из класса сульфонамидов. Нимесил выпускается в виде пакетов с порошком. Содержимое пакетика необходимо растворить в стакане со ста миллилитрами воды.
Л ЕКЦИЯ екци я № 9 109
АНАЛЬГЕЗИРУЮЩИЕ СРЕДСТВА.
План лекции.
22. Анальгетические средства (определение, классификация , сравнительная характеристика групп препаратов ).
23. Наркотические анальгетики: определение, классификация (с учетом влияния на опиатные рецепторы), механизм действия.
22. Сравнительная характеристика групп анальгетиков.
22. Фармакологическая характеристика ненаркотических анальгетиков (анальгетиков-антипиретиков), применение.
23. Ноцицептивная и антиноцицептивная системы, их взаимосвязь.
23. Наркотические анальгетики: определение, класс и фикация (с учетом влияния на опиатные рецепторы), механизм действия, сравнительная характеристика, применение.
23. Медико-биологические и социальные проблемы опийных наркоманий.
23. Острое отравление морфином (клиника, лекарственная помощь).
Л екция ЕКЦИЯ № 109 10
Анальгезирующие средства.
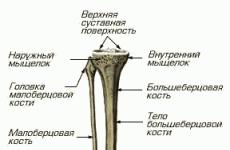
Ноцицептивная система - это система, которая обеспечивает поступление в мозг болевых ощущений. Сообщение о боли идут в головной мозг по двум различным путям (рис. 10.1).
Первый путь передачи боли (красный).: эЭто миелинизированные быстропроводящие толстые волокна. Их активация дает ощущение острой боли. Эти волокна (“быстрый путь”) направляются от болевых рецепторов прямо в таламус. и далее Затем в сенсорную и двигательную области задней центральной извилины коры головного мозга. Эта система выполняет функцию предупреждения. Она нНемедленно доставляет информацию в мозге о повреждении, его размерах и локализации. Она оОтвечает на вопрос “где болит?”
Второй путь передачи боли (синий).: Ббезмиелиновые медленно проводящие волокна. При их возбуждении возникает разлитая ноющая боль. Эти волокна (“медленный путь”) идут от болевых рецепторов к ретикулярной формации, гипоталамусу, таламусу и лимбической системе. Заканчиваются в верхней лобной и теменной извилине коры головного мозга. Наличие большого числа синапсов, отсутствие миелиновой оболочки и меньшая толщина волокон замедляют прохождение импульсов по этому пути. Эта система позволяет человеку, получившему травму, приписывать своим ощущениям те или иные качества. Она дает ответ на вопрос: «Как болит»?
Боль передают: ацетилхолин, норэпинефрин, дофамин, серотонин и субстанция Р.
23. Антиноцицептиная система .
Это система, которая тормозит поступление в мозг болевых ощущений.
23. Взаимосвязь ноцицептивной и антиноцицептивной систем.
На телах нейронов, ноцицептивной системы, передающей боль, имеются синапсы с другими нейронами. Это нейроны антиноцицептивной системы, которая как тень следует за ней. Они выделяют 3 типа медиаторова, каждый из которых состоящите из 5 аминокислот: 1) эндорфин-;, 2) энкефалин-;, 3) динорфин. Каждый из них преимущественно вВозбуждаеют собственный опиоидныей рецепторы на телах нейронов ноцицептивной системы: 1) эндорфин мю, 2) энкефалин - дельта, и 3) 3) динорфин - каппа опиоидный рецептор. Возбуждение опиоидных рецепторов вызывает фармакологические эффекты (рис. 10.2).
22. Определение.
22. Классификация.
1. Наркотические (опиоидные) и 2) ненаркотические (неопиоидные) анальгетики.
22. Опиоидные анальгетики.
22. Определение.
Это вещества, способные при резорбтивном действии подавлять внутрицентральное проведение и восприятие боли, а при повторном применении вызывать психическую и физическую зависимость (морфинизм).
23. Классификация (рис. 10.3).
Морфин
Героин
Метадоин
Меперидин
Тримеперидин
Фентанил
Суфентанил
Кодеин
Пропоксифен
Бупренорфик
Пентазоцин
Трамадол
Налоксон
Натрексон
Рисунок 10.3 Опиоидные анальгетики и антагонисты.
22. Анальгетические средства.
22. Определение.
Анальгетические средства это средства, которые при резорбтивном действии избирательно подавляют болевую чувствительность без выключения сознания и без угнетения других видов чувствительности.
тическ
тические.Н).
22. Наркотические Опиоидные анальгетики.
эЭ
23. Классификация наркотических (опиоидных) анальгетиков (с учетом влияния на опиатные рецепторы) (рис. 10.3).
1.Вызывают гиперполяризацию и торможение нейронов ноцицептивной системы за счет выхода из них K + .
2. Уменьшают поступление С a ++ в пресинаптические нервные окончания нейронов ноцицептивной системы. Си, тем самым, снижаюется высвобождение медиатора в синапс.
Опиоидные рецепторы.
Серпентинные. Сопряжены с G -белком. Экзогенные опиоиды подражают действию эндогенных. Вопиопептинов и вызывают эффекты в зависимости от типа опиоидных рецепторов, которые они возбуждают (рис. 10.4).
Ненаркотические (неопиоидные) анальгетики. Это вещества, проявляющие умеренный анальгезирующий эффект преимущественно на патогенетическом уровне, блокируя образование и действие на болевые окончания тканевых “альгогенных” веществ, которые образуются при воспалении, ишемии и травматизации тканей.
22. Сравнительная характеристика групп препаратов (рис. 10.1).
2 3. Ноцицептивная и антиноцицептивная системы.
Ноцицептивная система - это система, которая обеспечивает поступление в мозг болевых ощущений. Сообщение о боли идут в головной мозг по двум различным путям (рис. 10.2).
Первый путь передачи боли: это миелинизированные быстропроводящие толстые волокна, их активация дает ощущение острой боли. Эти волокна (“быстрый путь”) направляются от болевых центров прямо в таламус и далее в сенсорную и двигательную области задней центральной извилины коры головного мозга. Эта система выполняет функцию предупреждения, она немедленно доставляет информацию о повреждении, его размерах и локализации. Она отвечает на вопрос “ Где болит ?”
Второй путь передачи боли: безмиелиновые медленно проводящие волокна. При их возбуждении возникает разлитая ноющая боль. Эти волокна (“медленный путь”) идут от болевых рецепторов к ретикулярной формации, гипоталамусу, таламусу, лимбической системе. Заканчиваются в верхней лобной и теменной извилине коры головного мозга. Наличие большого числа синапсов, отсутствие миелиновой оболочки и меньшая толщина волокон замедляют прохождение импульсов по этому пути. Эта система позволяет человеку, получившему травму, приписывать своим ощущениям те или иные качества. Она дает ответ на вопрос: «Как болит»? Боль передают: ацетилхолин, норэпинефрин, дофамин, серотонин и субстанция Р.
23. Антиноцицептиная система . Это система, которая тормозит поступление в мозг болевых ощущений.
23. Взаимосвязь полицептивной и антиноцицептивной систем.
На телах нейронов, ноцицептивной, передающей чувство боли, имеются синапсы с другими нейронами. Это нейроны антиноцицептивной системы, которая как тень следует за ней. Они выделяют 3 типа медиаторов, каждый из которых состоит из 5 аминокислот: 1) эндорфин; 2) энкефалин; 3) динорфин. Каждый из них преимущественно возбуждает собственный опиоидный рецептор: 1) эндорфин МЮ, 2) энкефалин-дельта и 3) динорфин-каппа опиоидный раствор. Возбуждение опиоидных рецепторов вызывает эффекты (рис. 4).
У людей с недостаточной выработкой опиопептинов, слабый удар или царапина вызывают сильную боль. Наибольшее количество опиопептинов выделяется в области центрального околоводопроводного вещества. Они тормозят проведение болевых импульсов в ЦНС.
23. Наркотические (опиоидные) анальгетики.
23. Определение.
Опиоидные анальгетики это препараты, способные при резорбтивном действии подавлять внутрицентральное проведение и восприятие боли, а при повторном применении вызывать психическую и физическую зависимость (морфинизм).
23. Классификация наркотических (опиоидных) анальгетиков (с учетом влияния на опиатные рецепторы) (рис. 10.5).
23. Механизм действия опиоидных анальгетиков.
- Вызывают гиперполяризацию и торможение нейронов ноцицептивной системы за счет выхода из них K + .
- Уменьшают выход С a ++ в пресинаптические нервные окончания и, тем самым, снижая высвобождение медиатора. Опиоидные рецепторы-серпентинные сопряжены с G -белками. Экзогенные опиоиды подражают действию эндогенных опиопептинов от типа опиоидных рецепторов, которые они возбуждают (рис. 4).
23. Сравнительная характеристика и применение опиоидных анальгетиков.
Сильные агонисты.
Обладают высоким сродством к мю-рецепторам и, различноеменьшим сродством к дельта-, и каппа-рецепторам.
Влияние на ЦНС.
Это: 1) анальгезия,; 2) эйфория,; 3) заторможенность,; 4) угнетение дыхания, 5) угнетение кашля, 6) миоз, 7) тошнота и рвота, 8) брадикардия. При повторном введении развивается выраженная толерантность к этим эффектам.
1. Анальгезия. Больные получающие сильные агонисты, не чувствуют боль, но чувствительность сохраняется. То есть боль воспринимается как что-то приятное.
2. Эйфория . Больной, ощущающий боль, или наркоман после введения сильных агонистов, испытывают сильное удовлетворение и благополучие. Исчезают тревога и дискомфорт. Эйфория обусловлена стимуляцией вентральной покрышки.
3. Заторможенность . Проявляется сонливостью, затуманиванием сознания, нарушением способности к рассуждению. Сон развивается чаще у молодых здоровых людей, чем у пожилых. Он не глубокий. Сочетание сильных агонистов с седативными и снотворнымиогипнотическими средствами потенцирует их действие. Более выраженным седативным действием обладает морфин . и вВ меньшей степени - синтетические вещества ммеперидин и, фентанил .
4. Угнетение дыхания . Дозозависимое.ы До остановки. мМеханизм: уменьшается чувствительность нейронов дыхательного центра к СО 2 . В результате угнетения дыхания в крови накапливается СО 2 . Это приводит к расширению и уменьшению сопротивляемости мозговых сосудов. Повышается мозговой кровоток и внутричерепное давление. Поэтому морфин противопоказан людям с тяжелым поражением мозга.
Примечание. Угнетение дыхкния - причина смерти при острой передозировке опиоидов.
5. Угнетение кашля. Не коррелирует с обезболивающим действием и угнетением дыхания. Рецепторы, вовлеченные в противокашлевое действие, отличаются от таковых, вовлеченных в обезболивание.
Подавление кашля опиоидами кашля может привести к накоплению секрета с последующей обструкцией дыхательных путей и ателектазам. К этому эффекту развивается толерантность.
6) МиозМиоз (сС ). Опиоиды возбуждают ядра глазодвигательных нервов. Увеличевается парасимпатическая стимуляция глаз. Толерантность не развивается. У всех наркоманов выясняют состояние зрачка.
Прим е чание . Это важный диагностический прием. В большинстве других случаев комы и угнетения дыхания развивается мидриаз. Миоз устраняют атропин и антагонист.
7.8. Тошнота и рвота. Опиоидные анальгетики активируют триггерную хеморецепторную зону ствола мозга и могут вызвать тошноту и рвоту. Стимулируют вестибулярный аппарат. При движении тошнота и рвота усиливаются. Рвота не вызывает неприятных ощущений.
Примечание. Рвотный центр угнетают.
8. Брадикардия . Следствие стимуляции ядер блуждающих нервов.
Нейроэндокринные эффекты . Сильные агонисты ингибируют высвобождение гонадотропин и кортикотропин рилизинг гормонов. Снижают концентрацию: лютеинизирующего, фолликулостимулирующего, адренокортикотропного гормонов и бета-эндорфинов; тестостерона и кортизола. Повышают высвобождение пролактина и гормона роста за счет ослабления на них дофаминергического ингибирующего действия.
Периферические эффекты.
Ригидность мышц туловища . Сильные агонисты повышают тонус скелетной мускулатуры. Действие развивается на спинальном уровне. Уменьшается эффективность работы грудных мышц. Снижается легочная вентиляция. Эффект наиболее выражен при быстром внутривенном введении больших доз липофильных опиоидов (фентанил , суфентанил ). Устраняется опиоидными антагонистами. учащается СО 2
ЖКТ . Запор. Опиоидные рецепторы имеют высокую плотность в ЖКТ. Механизм. Блокируется выделение ацетилхолина в ЖКТ.
Мочеполовая система. Опиоиды снижают интенсивность кровотока в почках и снижают их функцию. Тонус мочеточников и мочевого пузыря повышается. Увеличение тонуса сфинктера уретры приводит к задержке мочи, особенно в послеоперационном периоде.
Матка . Опиоидные анальгетики удлиняют родовой акт.иф
Другие эффекты . Опиоидные анальгетики вызывают покраснение кожи и ощущение тепла за счет (расширенияе сосудов.), иИногда сочетающиесябывает с потливостью и крапивницаей. Эти реакции связаны с:
центральными эффектами и;
выделением гистамина из тучных клеток.
Толерантность и физическая зависимость .
При часто повторяющихся введениях в лечебных дозах морфина и его аналогов развивается толерантность. Для получения ответа, равного первоначальному, приходится увеличивать дозу. С этого периода формируется физическая зависимость. Становится необходимым продолжение введения вещества для предупреждения возникновения синдрома отмены или абстиненции.
Механизмы развития толерантности и физической зависимости:
1) :
изменение системы вторичных посредников; 2)
ингибирование аденилатциклазы; 3)
синтез G -белков.
Степень толерантности к некоторым эффектам опиоидов рис. .10.5).
Опиоидные анальгетики проникают через плаценту. Их применение для обезболивания в акушерстве может привести к рождению ребенка с угнетенным дыханием.
Новорожденные, родившиеся от матерей-наркоманок, характеризуются физической зависимостью с симптомами отмены опиоидов, если они не поступают в их организм.
Характеристика препаратов.
Морфин . Эффективен при лечении тяжелого болевого синдрома.
Применение.
Обезболивание. Вызываюет обезболивание и засыпание. Это важно, особенно в реанимации после операции. Может использоваться, как дополнение к снотворному действию при наличии боли снижается.
Лечение поноса. Морфин снижает сократимость гладкой мускулатуры кишечника и повышает ее тонус. Применяют при холере.
Облегчение кашля . Морфин подавляет кашлевой рефлекс. Чс; однако чаще используют кодеин или декстрометорфан .
Побочное действие. Тяжелое угнетение дыхания, рвота, дистрофияфория, гипотония. Повышает
Увеличение внутричерепногое давленияе. Это Пприводит к ишемии головного и спинного мозга. При гипертрофии простаты может вызвать острую задержку мочеотделения. Серьезное осложнение угнетение дыхания при эмфиземе и у больных с легочно-сердечными заболеваниями.
Героин.
Получение. (рис. 6).
Героин. Не встречается в природе. Полученают путем при ацетилированиия морфина в позиции, обозначенной точкой (рис. 10.6).
Действие. В 3 раза сильнее морфина. Вызывает выраженную эфарию.
Фармакокинетмка.
Это Героин более жирорастворим. Быстрее морфина проникает через гематоэнцефалический барьер,. В мозгу превращается в морфин . вызывая выраженную эйфорию приПри вызывает выраженную эйфорию Применение . Не используется в медицине.
Метадон . Синтетический пероральный опиоид. . В. Ддольше
Механизм действия. Метадон преимущественно возбуждает мю-рецепторы.обладает выраженным действием на мио-рецепторы.
Действие. Обезболивающая активность метадона эквивалентна морфину . Обладает сильным обезболивающим действием при приеме через рот.
Примечание . Морфин , чвсасывается из ЖКТ частично. Сужение зрачка и угнетение дыхания метадоном длиятся 24 часа. Повышает давление в желчных протоках и вызывает запоры. Эйфория выражена в меньшей степени, чем у морфина.
Фармакокинетмка.
Метадон хорошо всасывается при приеме через рот.
Применение. 1. Для контроля симптомов отмены у героиновых и морфиновых наркоманов. 2. Для лечения наркоманов. Больных затем медленно выводилият из метадоновой зависимости.
Примечание. Метадон вызывает средней степени выраженности синдромы отмены,. Он протекает не так тяжелокоторые развиваются,. Переносится легче. чем синдромы отмены от морфина .
Побочное действие . Наркомания. Синдромы отмены выражены в средней степени и более длительные (от дней до недель).
Меперидин. С Меперидин синтетический опиоид для приёма через рот и парентерально.
Механизм действия . Агонист опиоидных рецепторов, особенно каппа.
Действие.
Дыхание. Угнетение. дыхания как у морфина .
Сердечно-сосудистая система. Незначительное действие при приеме через рот. При внутривенном введении вызывает: 1) снижение периферической сопротивляемости сосудов и 2) увеличение периферического тока крови; 32) тахикардию. Последняя за счет антимускариновых свойств. Обладает отрицательным инотропным действием. Расширяет сосуды мозга и повышает давление ликвора.
ЖКТ. Меперидин сокращает гладкую мускулатуру. Приводит к запорам.
Глаз . Меперидин , в отличие от морфина , вызывает расширение зрачка.
Применение . Меперидин вызывает обезболивание при тяжелой боли. В отличие от морфина не используется при поносе или кашле. Вызывает менее выраженную задержку мочеотделения, чем морфин .
Побочное действие. Большие дозы меперидина вызывают дрожь, подергивание мышц и судороги. Отличается от других опиоидов тем, что в больших дозах расширяет зрачок и вызывает чрезмерные рефлексы. Меперидин наркотик. Заменять морфин и героин при использовании наркоманами. У больных почечной недостаточностью накапливается его метаболит - нормеперидин. Развиваются судороги.
Подгруппа фентанила фентанил , суфентанил и алфентанил .
Тримеперидин (промедол ).
Действие . Сильный анальгетик. при введениианестетиковСлабее морфина угнетает дыхание, ядра блуждающего нерва и рвотный центр. Спазмолитик, но стимулирует матку.
Фармакокинетмка.
Быстро всасывается. Эффективен при приёме внутрь и при парентеральном введении.
Взаимодействие . Усиливает действие местных анестетиков.
Фентанил .
Действие. По силе обезболивающего действия в 80 раз превосходит морфин .
Фармакокинетмка.
Обладает быстрым началом и короткой (15-30 минут) продолжительностью действия.
Взаимодействие .В комбинации с дроперидолом он вызывает разобщенную анестезию (нейролептанальгезия).
Суфентанил . Действие. вВ 5-7 раз активнее фентанила .
Умеренные агонисты.
Кодеин . Действие. Слабее, чем морфина . Однако при приеме внутрь кодеин эффективнее его морфина .
Применение. Редко используются самостоятельно. Чаще в сочетанных лекарственных формах с аспирином , парацетамолом и другими НПВС. Обладает хорошим противокашлевым действием в дозах, которые не устраняют боль. Обезболивающее действие эквивалентно аспирину .
Побочные действия. Кодеин вызывает менее выраженную эйфорию, чем морфин . Редко вызывает наркоманию. [Примечание:. В Для устранения кашля вместо кодеина используют декстраметорфан . Это синтетическое вещеНство не обладает обезболивающим действием. Имеет низкий потенциал зависимости].
Слабые агонисты.
Пропоксифен .
Действие. Производное метадона . При парентеральном применении вызывает обезболивание, которое в 2 раза слабее, чем у кодеина . При приеме через рот его активность составляет только 1/3 от таковой у кодеина .
Фармакокинетмка. Хорошо всасывается после приема через рот с пиком уровня в плазме через 1 час. Метаболизируется в печени.
Применение . В комбинации с аспирином для усиления обезболивающего действия.
Побочные действия. черезМТошнота, апорексия, запоры.
Передозировка . Заторможенность, угнетение дыхания, судороги, галлюцинации. Кардиотоксичность и отек легкого.
Помощь при передозировке . Налоксоном . Устроняет заторможенность и угнетение дыхания, но не кардиотоксичность. При
Взаимодействие . С алкоголем и успокаивающими средствами. Развивается тяжелое угнетение ЦНС, приводящее к смерти от угнетения дыхания и развития кардиотоксичности.
Частичные агонисты .
Бупренорфин . Активный и длительно действующий опиоид. Частичный агонист мю-рецепторов.
Действие. Длительное. действие оОбусловлено прочным связыванием с мю-рецеторами.
Примечание. Используют при Для детоксикации и поддерживающем лечении героиновых наркоманов.
Агонисты-антагонисты. (рис. 10.7).
Механизм действия. СОпиоиды, которые стимулируют одни, но блокируют другие рецепторы (рис. 10.7),.
Действие. называются агонистами-антагонистами.У людей, которые недавно получили опиоиды, агонисты-антагонисты обладают агонистическим действием. Ис устранения У больных с зависимостью к опиоидам, обладают антагонистическим действием. О, обостряют симптомы отмены. Вызывают не скорее дистрофию, чем эйфорию, а дисфорию (плохое настроение).
Примечание. Болевой синдром.
Характеристика препаратов. .
Пентозоцин .
Механизм действия. Агонист каппа-, и дельта- и сСлабыйОбладает слабой антагонистической активностью к мю- и дельта-рецепторамов. ИюустраненияПрименяют
Действие. Эйфория, менее выражена, чем у морфина.
Фармакокинетмка. Применяют через рот и парентерально.
Примечание. Умеренная боль. Для снижения симптомов зависимости к морфину.
Побочные действия. В больших дозах угнетает дыхание и перистальтику ЖКТ,. Повышает повышает кровяное давление. Может и может Вызывает галлюцинации, кошмары и головокружение. При стенокардии пентазоцин повышает давление в аорте и легочной артерии. Поэтому и, поэтому повышает нагрузку на сердце. Снижает ток крови в почкахпочке.
Взаимодействие. С морфином. Не устраняет угнетение дыхания,. Может мптомы
Трамадол .
Примечание. Сильный анальгетик.
Фармакокинетмка . Назначают внутрь и парентерально. Действует быстро и долго.
Прим введенииПрименение . Сильные боли. Особенно у онкобольных.
Частичные агонисты .
Бупренорфин активный и длительно действующий опиоид. Частичный агонист мю-рецептор. Длительное действие обусловлено прочным связыванием с мю-рецеторами, что делает его устойчивым к устранению налоксоном . Используют при детоксикации и поддерживающем лечении героиновых наркоманов.
Антагонисты.
Строение. Производные морфина с громоздкими заместителями у атома азота (см. рис. 10.7).
Механизм действия. Блокада опиоиднымх рецепторов особенно с мюи блокируют их.
Действие. вызывают обусловленный рецептором ответ. Нормальные люди - не действует. Наркоманы быстро приводят к прекращению действия героина. Развивается синдрома отмены. Механизм: вытесняют героин с рецептора.
Характеристика препаратов. (см. рис. 10.7).
Налоксон .
Механизм действия. Конкурентный антагонист опиоидныхов. Быстро вытесняет их из рецепторов. Блокирует рецептор (рис 10.7). рецепторов.
Применение . Передозировка опиоидов. (рис 10.7).
В течение 30 секунд после внутривенного введения налоксона угнетение дыхания и кома, характерные для передозировки героина, исчезают,. Возвращается сознание, появляется приводя больных в чувство и настороженность. Налоксон конкурентный антагонист опиоидных рецепторов.
Налтрексон . См. налоксон .
Действие . Действует дольше н а локсона. подобно налоксону . Обладает более длительным действием, чем налоксон . При однократном приёме внутрь блокирует действие инъецированного героина в течение 48 часов. [Примечание. Толерантность и синдром отмены к налтрексону и налоксону не развивается].
Применение. Июся 1. Налтрексон применяют при создании опиатзависимых поддерживающих программ для лечения наркоманов. У больных с зависимостью к опиоидам, которые внешне выглядят нормально налтрексон вызывает абстинентный синдром. 2.. При длительном применении не развивается синдром НС нижает тягу к алкоголю у хронических алкоголиков.
23. Медико-биологические проблемы опийных наркоманий.
1. Риск смертельной передозировки. 2.
Полинаркомания. Алкоголь, седативные и стимуляторы заменители опиоидов. 3.
Гепатит В. 4.
СПИД. 5.
Бактериальные инфекции с септическими осложнениями (менингиты, остеомиелиты, абсцессы во внутренних органах).
23. Социальные проблемы опийных наркоманий.
Убийства, самоубийства, несчастные случаи, расходы общества на лечение наркоманов, распад семьи.
23. Острое отравление морфином: клиника.
Эйфория, беспокойство, ощущение жара, сухость во рту, головокружение, головная боль, потливость, позывы к мочеиспусканию, сонливость, оглушенность, кома. Редкое (3-5 дыханий в минуту) и поверхностное дыхание. Снижение АД, точечные резко суженные зрачки. ([Примечание. По мере прогрессирования гипоксии зрачки расширяются]). П; пововышенные спинальные рефлексы, гипотермия,. С смерть в результате паралича дыхательного центра.
23. Лекарственная помощь. Налоксон в вену.
Применение опиоидов (резюме)..
Морфин . Боль, понос при холере, кашель при переломе рёбер.
Героин. Не Не применяется.
Метадон . Для контроля симптомов отмены у наркоманов.
Меперидин . Тримеперидин. Боль..
Фентанил . Для разобщенной анестезии (с дроперид о лом ).
Суфентанил . Боль.
Кодеин . Кашель.
Пропоксифен . С НПФС при болях воспалительного происхождения.
Бупренорфин и пентазоцин . Лечение героиновых наркоманов.
Трамадол . Боли у онкобольных.
Налоксон . При передозировке опиоидов (кома, угнетение дыхания).я). Для снижения влечения к алкоголю.
Налтрексон . Для снижения влечения к алкоголю.
22. Ненаркотическипиоидные анальгетики.
Определение. Это вещества, проявляющие умеренный анальгезирующий эффект преимущественно на патогенетическом уровне, блокируя образование и действие на болевые окончания тканевых “ альгогенных ” веществ, которые образуются при: 1) воспалении, 2) ишемии и 3) травматизации тканей.
22. Фармакологическая характеристика неопиоидных анальгетиков (анальгетиков-антипиретиков), применение.
е. Не Снимают боль и но Но снижают температуру тела (анальгетиками-антипиретиками). анальгетикамипосколькупотому чтоНе вызывают физическую зависимость.
Это нестероидные противовоспалительные средства со слабо выраженной противовоспалительной активностью или не обладающие ею. (рис. 10.2).
Классификация (рис 10.8).
Анальгезирующий эффект .
В большой степени проявляется при болях слабой и средней интенсивности исходящих из тканей эктодермального происхождения (мышцы, суставы, сухожилия, нервные стволы, ЦНС, зубы). При сильных висцеральных болях мало эффективны.еми [Примечание. Метамизол и кеторолак эффективны при коликах и послеоперационных болях. Их эффективность при почечной колике, связана с торможением образования простагландина Е 2 в почках за счет ингибирования циклооксигеназы. Снижается почечный кровоток и образование мочи. Это ведет к уменьшению давления в почечных лоханках и мочеточниках выше места обструкции. Обеспечивает длительный обезболивающий эффект ] . Блокада неожиданныминеопиоидными анальгетиками превращения арахидоновой кислоты в простагландины является основным в их обезболивающей активности при болях различной локализации. [Примечание. Простагландины вызывают боль путем сенсибилизации рецепторов к медиаторам боли (гистамину, брадикинину) и механическим воздействием, понижая порог болевой чувствительности].
Кроме того, анальгезирующий эффект неопиоидных анальгетиков связан с нарушением проведения болевых импульсов в спинном мозге.
Жаропонижающий эффект.
Снижают температуру тела только при лихорадке. На нормальную температуру не влияют.
Механизм жаропонижающего действия.
Простагландин Е 2 повышает чувствительность гипоталамических центров терморегуляции к действию эндогенных пирогенов (интерлейкина 1 и других), образующихся в организме под влиянием микроорганизмов, вирусов и токсинов. Блокируя синтез простагландина Е 2 , они снижают повышенную температуру тела.
Применение.
Ревматизм; ревматоидный, подагрический и псориатический артриты; анкилозирующий спондилит, синдром Рейтера. [Примечание. Синдром Рейтера это уретрит + иридоциклит + артрит → уретроокулосиновиальный синдром] . При ревматоидном артрите оказывают только симптоматический эффект. Не влиют на течение заболевания. Не могут приостановить прогрессирование процесса, вызвать ремиссию и предупредить развитие деформации суставов. Но облегчение, которое неопиоидные анальгетики приносят больным ревматоидным артритом, настолько существенно, что больные не могут обойтись без них.
2. Неревматические заболевания опорно-двигательного аппарата (остеоартроз, миозит, тендовагинит, травма). Чаще местно (мази, кремы, гели).
3.2. Невралгия, радикулит, ишиас, люмбаго.
43Почечная и печеночная колика.
45Болевой синдром различной этиологии, в том числе, головная и зубная боль, послеоперационные боли.
56Лихорадка (как правило,(при температуре выше 38,5 ْ С ) .
67Дисменорея. Применяют при первичной дисменорее для купирования болевого синдрома, связанного с повышением тонуса матки вследствие гиперпродукции простагландина F 2а . Помимо анальгезирующего действия, уменьшают объем кровопотери. Назначают при первом появлении болей 3-х дневным курсом или накануне месячных. При таком кратковременном лечении их побочное действие не развивается.
Противопоказания.
Неопиоидные анальгетики противопоказаны при эрозивно-язвенных поражениях ЖКТ (особенно в стадии обострения), выраженных нарушениях функции печени и почек, костного мозга, цитопениях, индивидуальной непереносимости, беременности.
Предосторожности.
Неопиоидные анальгетики должны с осторожностью назначаться больным бронхиальной астмой, а также людям, у которых раньше регистрировались побочные эффекты при приеме НПВС.
Пожилым больным назначают минимально эффективные дозы короткими курсами.
Побочное действие.
ЖКТ . Диспеп c ические расстройства. Эрозии, язвы желудка и 12-и перстной кишки. Кровотечения и перфорации ЖКТ.
Механизмы ЖКТ токсичности: 1)ингибирование активности циклооксигеназы-1 (ЦОГ -1), контролирующей выработку простагландинов, регулирующих целостность слизистой оболочки ЖКТ (основной механизм).; 2)локальное повреждение неопиоидными анальгетиками слизистой, поскольку большинство их является органическими кислотами.
Блокада ЦОГ- 1 результат системного действия неопиоидных анальгетиков. Обуславливает гастротоксичность при любом пути введения.
Поражение слизистой желудка неопиоидными анальгетиками протекает в 3 стадии: 1) торможение синтеза простагландинов в слизистой; 22) уменьшение опосредованной простагландинами выработки защитной слизи и бикарбонатов; 13) изъязвление;. Возможно также
2) локальное повреждение неопиоидными анальгетиками слизистой, поскольку большинство из них являеются органическими кислотами.
Проблема гастротоксичности неопиоидных анальгетиков осложняется их анальгезирующим действием. На фоне отсутствия боли обнаруживается выраженное изъязвление слизистой желудка.
Почки.
Нефротоксичность. Развивается по двум механизмам. 1. Блокада синтеза простагландина Е 2 и простациклина в почках вызывает сужение сосудов и ухудшение почечного кровотока. Развивается ишемия почек. С, снижается клубочковая фильтрация и диурез. Развиваются нарушения водно-электролитного обмена: (задержка воды, отеки, гипернатриемия, повышение давления крови).
2. Прямое повреждение паренхимы почек с развитием интерстициального нефрита («анальгетическая нефропатия»). Возможно развитие тяжелой почечной недостаточности.
Гематотоксичность . Метамизол и пропифиназон могут вызвать апластическую анемию и агранулоцитоз.
Коагулопатия . Торможение образования протромбина в печени и агрегации тромбоцитов. Результат кровотечение (чаще ЖКТ).
Реакции гиперчувствительности (аллергия) .
Сыпи, отек Квинке, анафилактичекий шок, синдромы Лайела и Стивенса - Джонсаона. Чаще (чаще вызывают метамизол и пропифиназон ).
Бронхоспазм. У больных бронхиальной астмой.
Механизм бронхоспазма:
1) аллергия (повышенная чувствительность);
2) торможение синтеза простагландина Е 2 , который является эндогенным бронходилататором;
3) увеличение синтеза лейкотриенов (бронхоконстрикторы).
Удлинение беременности и замедление родов .
Связано с тем, что простагландины Е 2 и F 2α стимулируют миометрий. Их синтез тормозится.
ыВзаимодействияе.
С непрямыми антикоагулятами и пероральными гипогликемическими средствами. Усилваение действия последних.
Механизм. 1. Вытеснение из центров связывание на альбумине. 2. С гипотензивными и мочегонными. Ослабляют действие.
3. С мочегонными. Нефротоксияность.
Механизм. Рис. 24.5
4. С аминогликозидными антибиотиками и дигоксином. Усиление токсичности последних.
5. С алюминийсодержащие антациды (альмагель , маалокс ) а такжеи холестирамин. Снижение всасывания неопиоидных анальгетиков.
6. С седативными и опиоидными анальгетиками. Усиление обезболивающего действия.
Характеристика отдельных препаратов.
Мефенамовая кислота .
Механизм действия. Ингибирование биосинтеза простагландинов.
Действие . АнальгетикОбладает анальгезирующими свойствами.
Противопоказана Фармакокинетика. Медленно всасывается,. Ччастично метаболизируется в печени. Т½ - 4 часа.
И Применение. Ревматизм : ревматизм, неспецифический инфекционный полиартрит, артралгии, миалгии, невралгии, головная и зубная боль.
Побочные действия . Более выраженное, чем у аспирину . Более токсична. Назначают до 1 недели.
Противопоказание. Детям.
Этофеномат .
Действие. Противовоспалительное и анальгезирующее.
Применение . Бурсит: бурсит, тендовагинит, суставной синдром, миозит, люмбаго, растяжения, вывихи, ушибы.
Метамизол (анальгин ).
Действие. Анальгезирующее, противовоспалительное, жаропонижающее, спазмолитическое действием.
Механизм анальгезирующего действия. Нарушение проведения болевых импульсов в спинном мозге.
Быстро етсяаяя Фармакокинетика. Быстро всасывается. Максимальная концентрация в крови через 1-2 часа, Т½ - 2,5 часа.
Применение :. Головная боли различнобольго генеза (головная, невралгия, радикулит, ревматизм). При сильных болях вводят парентерально.
Побочное действие. Г : угнетение кроветворения (гранулоцитопения, агранулоцитоз), аллергические реакции, анафилактический шок (возможен при в/ввнутривенном введении).
Противопоказания .: Повышенная повышенная чучувствительность, нарушения кроветворения.
Пропифеназон .
Действие . Выраженное анальгезирующее и жаропонижающее. Фармакокинетика. Быстро всасывается из ЖКТ. Максимальная концентрация в крови через 30 минут.
Применение. Входит в состав саридона и пливалгина .
Побочные действия. Безопасен.
Парацетамол .
Один один из основных препаратов для лечения боли легкой и средней тяжести в тех случаях, когда нет необходимости в противовоспалительном эффекте. Слабый ингибитор синтеза простагландинов в периферических тканях.
Действие . И: парацетамол ингибирует биосинтез простагландинов в ЦНС. Развивается жаропонижающее и обезболивающее действие. Слабо влияет на циклооксигеназу в периферических тканях. Поэтому обладает слабой противовоспалительной активностью. Не влияет на функцию тромбоцитов или увеличиваютудлиняет время образования сгустка крови. Лишен многих свойств аспирина .
Применение . ГЭффективен при (головныхая, мышечныхая и послеродовыхая боляхи. При ревматоидных артритах используется как дополнение к противовоспалительной терапии с целью анальгезии.
Парацетамол хороший заменитель обезболивающего и жаропонижающего действия аспирина у больных: 1) с жалобами со стороны ЖКТ, 2) у которых удлинение времени кровотечения не целесообразно, 3) которые не нуждаются в противовоспалительном действии аспирина .
Парацетамол наилучшее обезболивающее и жаропонижающее средство у детей с вирусной инфекцией. [Примечание. Аспирин (вспомним, что аспирин повышает риск возникновения синдрома Рея) ] .
Парацетамол не является антагонистом урикозурического средства пробенецида и, поэтому, не противопоказан больным подагрой.
Побочное действие:. ВПокраснение кожи и незначительные аллергические реакции бывают. Могут наблюдаться минимальные нарушения в содержании лейкоцитов, но они проходят. Повышение активности печеночных ферментов, но без развития желтухи. Эффект обратим после прекращения приема.
Токсичность . Головокружение, возбуждение и нарушение ориентации. Некроз канальцев почек и гипогликемическая кома редкие осложнения длительного лечения большими дозами парацетамола .
В дозах 10 г и более у взрослых может развиваться смертельный некроз печени вследствие истощения запасов глутатиона, расходуемого в реакциях детоксикации парацетамола . Ранние симптомы поражения печени это тошнота, рвота, понос, боли в животе. Лечение. - а цетилцистеин (предшественник глутатиона). Может может спасти жизнь, если его ввести не позднее в течение не более 20 часов после введения сверхдозы парацетамола . [Примечание. Прогноз хуже,Ранние симптомы поражения печени это тошнота, рвота, понос, боли в животе. чем при передозировке аспирина ] .
Гемолитическая анемия и метгемоглобинемия. В отличие от аспирина , парацетамол не вызывает ЖКТ-кровотеченийя.
Противопоказания. Заболевания печени. ю
Кеторолак.
Действие. НПВСМощный анальгетик Нестероидное противовоспалительное средство средней продолжительности действия. Вместо морфина при послеоперационной боли легкой и средней степени тяжести. Только в 2,5 раза уступает морфину .
Побочное действие . Гастротоксичность и повышенная кровоточивость (антиагрегационное действие).
Взаимодействия. С опиоидными анальгетиками. Потенцируется анальгезия. Это позволяет применять их в меньших дозах.
С местными анестетиками. Внутривенное или внутрисуставное введение кеторолака с лидокаином или бупивакаином обеспечивает лучшее обезболивание, чем раздельное.
Предосторожности . Кеторолак нельзя применять перед длительными операциями с высоким риском кровотечений, а также для обезболивания родов, купирования боли при инфаркте миокарда.
22. Сравнительная характеристика опиоидных и неопиоидных анальгетиков (рис. 10.9).
Эти средства избирательно снижают, подавляют болевую чувствительность, не влияя существенно на другие виды чувствительности и не нарушая сознания (анальгезия - утрата болевой чувствительности; an - отрицание, algos - боль). Издавна врачи старались избавить больного от боли. Гиппократ 400 лет до н. э. писал: "... удаление боли есть труд божественный". Исходя из фармакодинамики соответствующих препаратов, современные обезболивающие средства подразделяют на 2 большие группы:
I-я - наркотические анальгетики или группа морфина. Данная группа средств характеризуется следующими моментами (условиями):
1) обладают сильной анальгезизирующей активностью, позволяющей использвать их как выскокоэффективные болеутоляющие средства;
2) эти средства могут вызвать наркоманию, то есть пристрастие, лекарственную зависимость связанную с особм их влиянием на ЦНС, а также развитие болезненного состояния (абстиненции) у лиц с развившейся зависимостью;
3) при передозировке у больного развивается глубокий сон, переходящий последовательно в наркоз, кому и, наконец, заканчивающийся остановкой деятельности дыхательного центра. Поэтому они и получили свое название - наркотические анальгетики.
II-я группа средств - это ненаркотические анальгетики, классическими представителями которых являются: аспирин или ацетилсалициловая кислота. Препаратов здесь много, но все они не вызывают привыкания, т. к. обладают иными механизмами действия.
Разберем I-ю группу средств, а именно препараты группы морфина или наркотические анальгетики.
Наркотические анальгетики оказывают выраженное угнетающее влияние на центральную нервную систему. В отличии от средств, угнетающих ЦНС неизбирательно, оно проявляется анальгетическим, умеренно снотворным, противокашлевым действием, угнетающим центры дыхания. Кроме того, большинство наркотических анальгетиков вызывает лекарственную (психическую и физическую) зависимость.
Наиболее ярким представителем данной группы средств, из-за которого эта группа и получила свое название, является МОРФИН.
Morphini hydrochloridum (табл. по 0, 01; амп. 1% - 1 мл). Алколоид морфин выделяют из опия (греч. - opos - сок), который является застывшим, высохшим соком недозревших коробочек снотворного мака (Papaver somniferum). Родина мака - Малая Азия, Китай, Индия, Египет. Морфин свое название получил от имени древнегреческого бога сновидений Морфея, являющегося, согласно легенде, сыном бога сна Гипноса.
Морфина в опии содержится 10-11%, что составляет почти половину доли всех имеющихся в нем алкалоидов (20 алкалоидов). Применяются в медицине давно (5000 лет назад как: обезболивающее, противопоносное средство). Несмотря на осуществленный в 1952 году химиками синтез морфина, его до сих пор получают из опия, что дешевле и легче.
По химической структуре все фармакологически активные алкалоиды опия относятся либо к производным ФЕНАНТРЕНА, либо к производным ИЗОХИНОЛИНА. К алкалоидам фенантренового ряда относят: морфин, кодеин, тебаин и др. Именно алкалоиды фенантрена характеризуются выраженным угнетающим действием на ЦНС (анальгетическое, противокашлевое, снотворное и др.).
Для производных изохинолина свойственно прямое спазмолитическое действие на гладкие мышцы. Типичным изохинолиновым производным является папаверин, который никаким действием на ЦНС не обладает, но влияет на гладкую мускулатуру, особенно в состоянии ее спазма. Папаверин выступает в данном случае как спазмолитик.
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА МОРФИНА
1. Действие морфина на ЦНС
1) Морфин прежде всего оказывает анальгетическое действие или обезболивающее, при этом анальгезирующее действие оказывают дозы, существенно не изменяющие функции ЦНС.
Анальгезия, вызываемая морфином, не сопровождается смазанностью речи, нарушениями координации движений, не ослабляются осязание, виброчувствительность, слух. Болеутоляющий эффект является для морфина основным. В современной медицине это одно из самых сильных обезболивающих средств. Эффект разивается через несколько минут после иньекции. Чаще морфин вводят в/м, п/к, но можно и в/в. Действие длится 4-6 часов.
Как известно, боль складывается из 2-х компонентов:
а) восприятие боли, зависящее от порога болевой чувствительности человека;
б) психическая, эмоциональная реакция на боль.
В этой связи важно то, что морфин резко угнетает оба компонента боли. Он повышает, во-первых, порог болевой чувствительности, снижая, таким образом, восприятие боли. Анальгетическое действие морфина сопровождается чувством благополучия (эйфории).
Во-вторых, морфин изменяет эмоциональную реакцию на боль. В терапевтических дозах он может даже не полностью устранять ощущения боли, но больные воспринимают ее как нечто постороннее.
Как и каким образом осуществляет указанные эффекты морфин?
МЕХАНИЗМ ДЕЙСТВИЯ НАРКОТИЧЕСКИХ АНАЛЬГЕТИКОВ.
В 1975 году Hughes и Kosterlitz в нервной системе у человека и животных были открыты специфические "опиатные" рецепторы нескольких типов, с которыми взаимодействуют наркотические анальгетики.
В настоящее время выделяют 5 типов этих опиатных рецепторов: мю, дельта, каппа, сигма, эпсилон.
Именно с указанными опиатными рецепторами взаимодействуют в норме различные эндогенные (вырабатываемые в самом организме) пептиды, обладающие высокой анальгетической активностью. Эндогенные пептиды обладают очень высоким сродством (аффинитетом) к указанным опиатным рецепторам. Последние, как стало известно, расположены и функционируют в различных отделах ЦНС и в периферических тканях. В связи с тем, что эндогенные пептиды обладают высоким сродством, их в литературе еще называют по отношению к опиатным рецепторам ЛИГАНДАМИ, то есть (от лат. - ligo - связываю) непосредственно связывающиеся с рецепторами.
Эндогенных лигандов несколько, они все являются олиго-пептидами, содержащими разное количество аминокислот и объединенными названием "ЭНДОРФИНЫ" (то есть эндогенные морфины). Пептиды, в состав которых входит пять аминокислот, называют энкефалинами (метионин-энкефалин, лизин-энкефалин). В настоящее время это целый класс из 10-15 веществ, имеющих в составе своей молекулы от 5 до 31 аминокислоты.
Энкефалин, по Hughes, Kosterlitz - это "вещества в голове".
Фармакологические эффекты энкефалинов:
Выброс гормонов гипофиза;
Изменение памяти;
Регулирование дыхания;
Модулирование иммуннного ответа;
Обезболивание;
Состояние, подобное кататонии;
Судорожные припадки;
Регуляция температуры тела;
Контроль за аппетитом;
Функции размножения;
Сексуальное поведение;
Реакции на стресс;
Снижение АД.
ОСНОВНЫЕ БИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ЭНДОГЕННЫХ ОПИАТОВ
Основным эффектом, ролью, биологической функцией эндорфинов является торможение освобождения "нейромедиаторов боли" из центральных окончаний афферентных немиелинизированнных С-волокон (в том числе и норадреналина, и ацетилхолина, допамина).
Как известно, этими медиаторами боли могут быть, прежде всего, вещество Р (пептид из аминокислот), холецистокинин, соматостатин, брадикинин, серотонин, гистамин, простагландин. Болевые импульсы распространяются по С- и А -волокнам (А-дельта волокна) и поступают в задние рога спинного мозга.
При возникновении болевых ощущений в норме стимулируется особая система энкефалинергических нейронов, так называемая антиноцицептивная (антиболевая) система, выделяются нейропептиды, что оказывает тормозное действие на болевую систему (ноцицептивную) нейронов. Конечным результатом действия эндогенных пептидов на опиатные рецепторы является повышение порога болевой чувствительности.
Эндогенные пептиды очень активны, они в сотни раз активнее морфина. В настоящее время они выделены в чистом виде, но в очень небольших количествах, являются очень дорогими, пока в основном используют их в экспериментах. Но уже есть и в практике результаты. Синтезирован, например, отечественный пептид ДАЛАРГИН. Получены первые результаты, причем уже в клинике.
В случае недостаточности антиноцецептивной системы (антиболевой энкефалинергической), а это бывает при чрезмерно выраженном или длительном повреждающем воздействии, болевые ощущения приходится подавлять с помощью болеутоляющих средств - анальгетиков. Оказалось, что местом действия как эндогенных пептидов, так и экзогенных наркотических средств, являются одни и те же структуры, а именно опиатные рецепторы ноцицептивной (болевой) системы. В этом плане морфин и его аналоги являются агонистами опиатных рецепторов. Отдельные эндо- и экзогенные морфины воздействуют на разные опиатные рецепторы.
В частности, морфин действует преимущественно на мю-рецепторы, энкефалины на дельта-рецепторы и т. д. ("отвечающие" за обезболивание, угнетение дыхания, снижение частоты ССС, обездвижение).
Таким образом, наркотические аналгетики, в частности морфин, играя роль эндогенных опиатных пептидов, являясь по-существу имитаторами действия эндогенных лигандов (эндорфинов и энкефалинов), повышают активность антиноцицептивной системы и усиливают тормозное ее влияние на систему боли.
Помимо эндорфинов, в этой антиноцицептивной системе функционируют серотонин и глицин, являющиеся синергистами морфина. Воздействуя преимущественно на мю-рецепторы, морфин и другие препараты этой группы преимущественно подавляют ноющую, тянущую боль, связанную с суммированием ноцицептивной импульсации, поступающей из спинного мозга по неспецифическому пути к неспецифическим ядрам таламуса, нарушая ее распространение к верхней лобной, теменной извилинам коры большого мозга (то есть восприятие боли), а также к другим его отделам, в частности, к гипоталамусу, миндалевидному комплексу, в которых формируются вегетативная, гормональная, эмоциональная реакции на боль.
Подавляя эту боль, препараты тормозят эмоциональную реакцию на нее, в результате чего наркотические анальгетики предупреждают нарушения функции сердчено-сосудистой системы, возникновение страха, страдания, связанные с болью. Сильные анальгетики (фентанил) способны подавить проведение возбуждения и по специфическому ноцицептивному пути.
Возбуждая энкефалиновые (опиатные) рецепторы в других структурах головного мозга, эндорфины и наркотические анальгетики оказывают влияние на сон, бодроствование, эмоции, половое поведендие, судорожные и эпилептические реакции, вегетативные функции. Оказалось, что в реализации эффектов эндорфинов и морфиноподобных препаратов участвуют практически все известные системы нейромедиаторов.
Отсюда и различные другие фармакологические эффекты морфина и его препаратов. Так, 2-ой эффект морфина, успокаивающее и снотворное действие. Седативный эффект морфина выражен очень четко. Морфей - сын бога сна. Седативный эффект морфина заключается в развитии сонливости, некоторого затемнения сознания, нарушении способности логического мышления. От сна, вызванного морфином, больные легко пробуждаются. Сочетание морфина со снотворными или другими седативными средствами делает угнетение ЦНС более выраженным.
3-ий эффект - влияние морфина на настроение. Здесь влияние двоякое. У некоторых больных, а чаще у здоровых лиц после однократного введения морфина возникает чувство дисфории, беспокойства, отрицательных эмоций, нет удовольствия, снижение настроения. Как правило, это возникает у здоровых лиц, у которых нет показаний к применению морфина.
При повторном введении морфина, особенно при наличии показаний к использованию морфина, обычно развивается явление эйфории: возникает повышение настроения с чувством блаженства, легкости, положительных эмоций, приятности по всему телу. На фоне возникающей сонливости, сниженной физической активности, развивается затруднение концентрации внимания, возникает чувство безразличия к окружающему миру.
Мысли и суждения человека утрачивают логическую последовательность, воображение приобретает фантастичность, возникают яркие красочные картины, видения (мир грез, "кайф"). Утрачивается способность заниматься искусством, наукой, творчеством.
Возникновение перечисленных психотропных эффектов связано с тем, что морфин, как и другие анальгетики данной группы, прямо взаимодействуют с опиатными рецепторами, локализованными в коре большого мозга, гипоталамусе, гиппокампе, миндалевидном комплексе.
Желание испытать это состояние еще раз и является причиной возникновения психической зависимости человека от препарата. Таким образом, именно эйфория ответственна за развитие наркомании. Эйфория может наступить даже после одной иньекции.
4-ый фармакологический эффект морфина связан с его воздействием на гипоталамус. Морфин тормозит центр терморегуляции, что может приводить к резкому снижению температуры тела при отравлениях морфином. Кроме того, с влиянием морфина на гипоталамус связано также и то, что он, как и все наркотические анальгетики, стимулирует освобождение антидиуретического гормона, что приводит к задержке мочи. Кроме того, он стимулирует освобождение пролактина и соматотропина, однако задерживает освобождение лютеинизирующего гормона. Под влиянием морфина снижается аппетит.
5-ый эффект - морфин, как и все другие препараты данной группы, оказывает выраженное влияние на центры продолговатого мозга. Это действие неоднозначно, так как ряд центров он возбуждает, а ряд угнетает.
Угнетение дыхательного центра наиболее легко возникает у детей. Угнетение дыхательного центра связано со снижением его чувствительности к углекислому газу.
Морфин угнетает центральные звенья кашлевого рефлекса и обладает выраженной противокашлевой ативностью.
Наркотические анальгетики, как и морфин, могут способствовать стимуляции нейронов хеморецепторной триггерной (пусковой) зоны дна IY желудочка, вызывая тошноту и рвоту. Сам рвотный центр морфин в больших дозах угнетает, поэтому повторное введение морфина не вызывает рвоту. В этой связи применение рвотных средств при отравлении морфином бесполезно.
6-ой эффект - влияние морфина и его препаратов на сосуды. Терапевтические дозы оказывают незначительное воздействие на АД и сердце, токсические могут вызвать гипотензию. Но морфин вызывает расширение периферических кровеносных сосудов, особенно капилляров, частично за счет прямого действия и частично за счет высвобождения гистамина. Таким образом, он может вызывать покраснение кожи, повышение ее температуры, отек, зуд, потливость.
ВЛИЯНИЕ МОРФИНА НА ЖКТ И ДРУГИЕ ГЛАДКОМЫШЕЧНЫЕ ОРГАНЫ
Влияние наркотических анальгетиков (морфина) на ЖКТ относят в основном за счет повышения ими активности нейронов центра n. vagus, и в меньшей степени за счет прямого влияния на нервные элементы стенки желудочно-кишечного тракта. В этой связи морфин вызывает сильный спазм гладкой мускулатуры кишечника, имоцекального и анального сфинктеров и одновременно снижает двигательную активность, уменьшая перистальтику (ЖКТ). Спазмогенное действие морфина наиболее выражено в области двенадцатиперстной кишки и толстого кишечника. Секреция слюны, соляной кислоты желудочного сока и секреторная активность слизистой оболочки кишечника уменьшаются. Замедляется прохождение каловых масс, возрастает всасывание воды из них, что ведет к запорам (морфинная обстипация - повышение тонуса всех 3-х групп мышц). Морфин и его аналоги повышают тонус желчного пузыря, способствуют развитию спазма сфинктера Одди. Поэтому, хотя аналгетический эффект облегчает состояние больного при желчных коликах, течение самого патологического процесса усугубляется.
ВЛИЯНИЕ МОРФИНА НА ДРУГИЕ ГЛАДКОМЫШЕЧНЫЕ ОБРАЗОВАНИЯ
Морфин повышает тонус матки и мочевого пузыря, мочеточников, что сопровождается "мочевой поспешностью". В то же время, сокращается висцеральный сфинктер, что при недостаточной реакции на позывы из мочевого пузыря ведет к задержке мочи.
Морфин повышает тонус бронхов и бронхиол.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ МОРФИНА
1) Острые боли, угрожающие развитием болевого шока. Примеры: тяжелая травма (переломы трубчатых костей, ожог), облегчение послеоперационного периода. В этом случае морфин используется как обезболивающее, противошоковое средство. С этой же целью морфин используют при инфаркте миокарда, эмболии легочной артерии, остром перикардите, спонтанном пневмотораксе. Для облегчения внезапно появившейся боли морфин вводят в/в, что быстро уменьшает риск развития шока.
Кроме того, морфин как анальгетическое средство используют при коликах, например, кишечных, почечных, печеночных и т. д. Однако четко нужно помнить, что в данном случае морфин вводят вместе со спазмолитиком атропином, и только тогда, когда врач точно уверен в правильности диагноза.
2) Хронические боли у безнадежных умирающих больных с гуман ной целью (пример: хосписы - больницы для безнадежных онкологических больных; прием по часам). Вообще-то хронические боли являются противопоказанием к использованию морфина. Только у безнадежных, умирающих опухоленосителей, обреченных введение морфина является обязательным.
3) Как средство премедикации во время наркоза, до наркоза, то есть в анестезиологии.
4) Как противокашлевое средство при кашле, угрожающем жизни больного. По данному показанию морфин назначают например, при обширных операциях, травмах грудной клетки.
5) При острой левожелудочковой недостаточности, то есть при сердечной астме. В данном случае эффект обусловлен снижением возбудимости ЦНС и патологической одышки. Он вызывает расширение периферических сосудов, вследствие чего происходит перераспределение крови из системы легочных артерий в расширенные периферические сосуды. Это сопровождается уменьшением кровотока и снижением давления в легочной артерии и ЦВД. Таким образом снижается работа сердца.
6) При остром отеке легких.
ПОБОЧНЫЕ ЭФФЕКТЫ МОРФИНА
Широта фармакологических эффектов морфина обусловливает и его многочисленные побочные реакции. Это, прежде всего, дисфория, запор, сухость во рту, затуманенность мышления, головокружение, тошнота и рвота, угнетение дыхания, головная боль, повышенная утомляемость, парестезии, брадикардия. Иногда встречаются непереносимость в виде тремора и бреда, а также аллергических реакций.
ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ МОРФИНА
Абсолютных нет, но есть целая группа относительных противопоказаний:
1) ранний детский возраст (до 3-х лет) - опасность угнетения дыхания;
2) у беременных женщин (особенно в конце беременности, во время родов);
3) при самых различных видах дыхательной недостаточности (эмфизема легких, при бронхиальной астме, при кифосколиозе, ожирении);
4) при тяжелых травмах головы (повышение внутричерепного давления; в этом случае морфин еще более повышая внутричерепное давление, вызывает рвоту; рвота, в свою очередь, повышает внутричерепное давление и так формируется порочный круг).
В нашей стране создан на базе морфина очень мощный анальгетик с длительным действием, - МОРФИЛОНГ. Он представляет собой новое лекарственное средство, содержащее морфина гидрохлорид и узкофракционированный поливинилпирролидон. Морфилонг в результате приобретает большую продолжительность действия (22-24 часа его болеутоляющий эффект) и большую интенсивность эффекта. Менее выражены побочные эффекты. В этом его преимущество перед морфином (по продолжительности в 4-6 раз превышает продолжительность действия морфина). Используют в качестве болеутоляющего пролонгированного средства:
1) в послеоперационном периоде;
2) при резко выраженном болевом синдроме.
ОМНОПОН (Omnoponum в амп. по 1 мл - 1% и 2% раствор). Омнопон представляет собой новогаленовый препарат опия в виде смеси 5-ти алкалоидов опия. Он содержит 48-50% морфина и 32-35% других алкалоидов как фенантренового, так и изохинолинового ряда (папаверин). В этой связи омнопон обладает меньшим спазмогенным действием. В принципе фармакодинамика омнопона аналогична таковой морфина. ОДнако используют омнопон все равно вместе с атропином. Показания к применению практически те же.
Помимо морфина, омнопона в медицинской практике нашли применение многие синтетические и полусинтетические препараты. Эти препараты были созданы с 2-мя целями:
1) чтобы избавиться от плантаций мака;
2) чтобы не формировалось у больных пристрастие. Но эта цель не удалась, так как у всех наркотических анальгетиков общие механизмы действия (через опиатные рецепторы).
Значительный интерес представляет ПРОМЕДОЛ, являющийся синтетическим препаратом, производным пиперидина.
Promedolum (табл. - 0, 025; амп. по 1 мл - 1% и 2% раствор). По обезболивающей активности уступает морфину в 2-4 раза. Продолжительность действия 3-4 часа. Реже вызывает тошноту и рвоту, в меньшей степени угнетает дыхательный центр. В отличие от морфина промедол снижает тонус мочеточников и бронхов, расслабляет шейку матки и немного усиливает сокращения стенки матки. В связи с этим промедолу отдается предпочтение при коликах. Кроме того, он может применяться во время родов (по показаниям, так как в меньшей степени, чем морфин, угнетает дыхание плода, а также расслабляет шейку матки).
В 1978 году появился синтетический анальгетик - МОРАДОЛ, являющийся по химической структуре дериватом фенантрена. Аналогичным синтетическим препаратом является ТРАМАЛ. МОРАДОЛ (буторфанол тартрат) при в/м и в/в введении обеспечивает высокую степень аналгезирующей эффективности, при этом аналгезия наступает быстрее, чем при введении морфина (через 30-60 минут, морфин - через 60 минут). Действие длится 3-4 часа. Вместе с тем, у него существенно меньше побочных эффектов и главное очень низкий риск развития физической зависимости даже при длительном использовании, так как морадол редко вызывает эйфорию (действует приемущественно на другие опиатные рецепторы-дельта). Кроме того, ограниченно угнетает дыхание, даже в больших дозах. Используют: по тем же показаниям, что и морфин, но в случае с длительной необходимостью применения. В терапевтических дозах не угнетает дыхательный центр, безопасно для матери и плода.
Другой синтетический представитель производных пиперидин-фенантрена ФЕНТАНИЛ. Фентанил обладает очень высокой анальгетической активностью, превосходит по активности морфин (в 100-400 раз). Отличительной особенностью фентанила является кратковременность вызываемого им обезболивания (20-30 минут). Эффект развивается через 1-3 минуты. Поэтому фентанил применяют для нейролептанальгезии совместно с нейролептиком дроперидолом (таломонал).
Такой вид анальгезии используют тогда, когда больной должен быть в сознании, например, при инфаркте миокарда. Сама форма обезболивания очень удобна, так как больной не реагирует на болевое раздражение (анальгезирующий эффект) и с полным безразличием относится ко всему происходящему (нейролептический эффект, складывающийся из суперседативного и сильного транквилизирующего).
Особняком стоит алкалоид опия КОДЕИН (Codeinum в табл. по 0, 015). Как анальгетик значительно слабее морфина. Имеет более слабое сродство к опиатным рецепторам. Противокашлевое действие кодеина слабее, чем у морфина, однако вполне достаточное для практики.
Достоинства кодеина:
1) в отличие от морфина хорошо всасывается при приеме внутрь;
2) кодеин меньше угнетает дыхание;
3) меньше вызывает сонливость;
4) обладает меньшей спазмогенной активностью;
5) к кодеину медленнее развивается зависимость.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ КОДЕИНА:
1) при сухом, саднящем, непродуктивном кашле;
2) второй этап борьбы с хронической болью у онкобольного (ВОЗ), согласно трехступенчатой схемы. Кодеин (50-150 мг через 5 часов) плюс ненаркотический анальгетик, плюс вспомогательные средства (глюкокортикоиды, антидепрессанты, противосудорожные, психотропные и др.).
ОСТРОЕ ОТРАВЛЕНИЕ МОРФИНОМ И МОРФИНОПОДОБНЫМИ ПРЕПАРАТАМИ
Острое отравление морфином может произойти при передозировке препарата, а также при случайном приеме больших доз у больных с привыканием. Кроме того, морфин может быть использован с суицидальной целью. Для взрослых летальная доза составляет 250 мг.
При остром отравлении морфином клиническая картина характерна. Состояние больного очень тяжелое. Развивается вначале сон, переходящий в стадию наркоза, далее комы, ведущей к параличу дыхательного центра.
Клиническая картина складывается прежде всего из угнетения дыхания, его урежения. Кожа бледная, холодная, цианотичная. Отмечается понижение температуры тела и мочеотделения, в конце отравления - снижение АД. Развивается брадикардия, резкое сужение зрачка (точечный размер зрачка), в конце от гипоксии зрачок расширяется. Смерть наступае вследствие угнетения дыхания или шока, отека легких и вторичной инфекции.
ЛЕЧЕНИЕ больных с острым отравлением морфином строится на тех же принципах, что и лечение острой интоксикации барбитуратами. Меры помощи выделяют специфические и неспецифические.
СПЕЦИФИЧЕСКИЕ МЕРЫ ПОМОЩИ связаны с введением специфических антагонистов морфина. Наилучший антагонист - это НАЛОКСОН (наркан). У нас в стране налоксона практически нет, а потому чаще используют частичный антагонист - НАЛОРФИН.
Налоксон и налорфин устраняют влияние морфина и его препаратов на опиатные рецепторы и восстанавливают нормальную функцию ЦНС.
Налорфин, частичный антагонист морфина, в чистом виде (монопрепарат) действует как морфин (вызывает анальгетический эффект, но слабее, угнетает дыхание, дает брадикардию, суживает зрачки). Но на фоне веденного морфина налорфин проявляет себя как его антагонист. Налорфин обычно применяют в/в в дозе от 3 до 5 мг, при необходимости повторяя ин"екции через 30 минут. Эффект его буквально возникает на "кончике иглы" - в течение первой минуты введения. При передозировке этих средств у отравленного морфином может быстро развиться синдром отмены.
НЕСПЕЦИФИЧЕСКИЕ МЕРЫ ПОМОЩИ связаны с удалением невсосавшегося яда. Причем промывание желудка нужно делать даже при парентеральном введении морфина, так как происходит частичное его выделение слизистой ЖКТ в просвет кишечника. Необходимо согревание больного, если возникают судороги, используют противосудорожные.
При глубоком угнетении дыхания производят искусственную вентиляцию легких.
ХРОНИЧЕСКОЕ ОТРАВЛЕНИЕ МОРФИНОМ, как правило, связано с развитием к нему зависимости. Развитие пристрастия, наркомании закономерно сопровождается повторным введением наркотических анальгетиков. Различают физическую и психическую зависимость.
Проявлением сформировавшейся ФИЗИЧЕСКОЙ ЗАВИСИМОСТИ от наркотических анальгетиков является возникновение синдрома отмены или абстиненции при прекращении повторного введения морфина. Абстинентный синдром слагается из ряда характерных признаков: через 6-10-12 часов после последней ин"екции морфина у морфиниста возникают ринорея, слезотечение, страшная зевота, озноб, появляется гусиная кожа, гипервентиляция, гипертермия, мидриаз, мышечные боли, рвота, диарея, тахикардия, слабость, потливость, расстройства сна, галлюцинации, тревожность, беспокойство, агрессивность. Эти симптомы продолжаются в течение 2-3 суток. Для предупреждения или ликвидации этих явлений наркоман готов пойти на все, даже на преступление. Постоянный прием препарата приводит человека к физической и психической деградации.
Механизм развития абстиненции связывают с тем, что наркотические анальгетики, активируя опиатные рецепторы по принципу обратной связи (как в эндокринологии), тормозят освобождение, а может быть и синтез эндогенных опиатных пептидов, постепенно заменяя их активность. В результате отмены анальгетиков возникает недостаточность и вводимого ранее анальгетика и эндогенного пептида. Развивается синдром абстиненции.
Ранее физической зависимости развивается психическая зависимость. Основой возникновения психической зависимости являются эйфория, седативный эффект и индифферентное отношение к беспокоящим человека воздействия внешней среды. Кроме того, повторное введение морфина вызывает очень приятные для морфиниста ощущения в брюшной полости, ощущения необычного тепла в эпигастральной области и нижней части живота, напоминающие таковые при интенсивном оргазме.
Помимо психической и физической зависимости имеется 3-ий признак наркомании - развитие толерантности, устойчивости, привыкания. В этой связи наркоман все время вынужден повышать дозу анальгетика.
Лечение зависимости к морфину принципиально не отличается от лечения зависимости к алкоголю или барбитуратам. Лечение наркоманов осуществляют в специальных учреждениях, но результаты пока не обнадеживают (единицы процентов). Часты развитие синдрома лишения (абстиненции), рецидивы пристрастия.
Нет ни одного специального средства. Используют общеукрепляющие, витамины. Легче профилактировать наркоманию, чем лечить. Опасность развития наркомании и является главной причиной ограничения применения данных препаратов в медицине. Из аптек их отпускают только по специальным рецептам, препараты хранятся по списку "А".
НЕНАРКОТИЧЕСКИЕ АНАЛЬГЕТИКИ - это обезболивающие, аналгизирующие средства, не оказывающие существенного влияния на ЦНС, не вызывающие наркомании и наркоза. Другими словами, в отличие от наркотических анальгетиков они не обладают седативным и снотворным эффектом; эйфория, привыкание и лекарственная зависимость при их применении не возникают.
В настоящее время синтезирована большая группа препараов, среди которых выделяют так называемые:
1) старые или классические ненаркотические анальгетики
2) новые, более современные и в большей мере обладающие противовоспалительным действием - так называемые нестероидные противовоспалительные средства - НПВС.
По химическому строению старые или классические ненаркотические анальгетики делятся на 3 основные группы:
1) производные салициловой кислоты (орто-оксибензойной кислоты) - салицилаты:
а) Кислота ацетилсалициловая - (аспирин, Acidum acetylsalicylicum);
б) натрия салицилат (Natrii salicylas).
Еще препараты этой группы: салициламид, метилсалицилат, а также дифлунизал, бенортан, тосибен.
2) производные пиразолона:
а) амидопирин (Amidopyrinum, в табл. по 0, 25) - снят с производства как монопрепарат, используется в комбинированных средствах;
б) анальгин (Analginum, в табл. по 0, 5; амп. по 1; 2 мл - 25% и 50% раствор);
в) бутадион (Butadionum, в табл. по 0, 15);
3) производные анилина:
а) фенацетин (Phenacetinum - в комбинированных таблетках);
б) парацетамол (Paracetamolum, в табл. по 0, 2).
Ненаркотические анальгетики обладают 3-мя основными фармакологическими эффектами.
1) Анальгезирующим или обезболивающим воздействием. Анальгезирующая активность ненаркотических анальгетиков проявляется при определенных видах болевых ощущений: главным образом при невралгических, мышечных, суставных болях, а также при головной и зубной боли.
При сильной боли, связанной с травмами, полостными оперативными вмешательствами, злокачественными образованиями они практически неэффективны.
2) Жаропонижающим или антипиретическим действием, проявляющимся при лихорадочных состояниях.
3) Противовоспалительным, действием, выраженным в разной степени у различных соединений этой группы.
Начнем с салицилатов. Основным препаратом этой группы является кислота ацетилсалициловая или АСПИРИН (Acidum acetylsalicylicum в табл. по 0, 1 - детская; 0, 25; 0, 5) (АА).
Салицилаты известны давно, им уже более 130 лет, они явились первыми препаратами, оказывающими специфическое противовоспалительное действие, сочтающееся с болеутоляющим и жаропонижающим эффектом. Полный синтез ацетилсалициловой кислоты был осуществлен в 1869 году. Салицилаты с тех пор получили широкое распространение в медицинской практике.
Салицилатам, в том числе АА (аспирину), присущи 3 основных фармэффекта.
1) Обезболивающий или анальгетический эффект. Этот эффект выражен несколько в меньшей степени, особенно при висцеральной боли, чем у морфина. АА кислота оказывается эффективным препаратом при следующих видах боли: при головной боли; зубной боли; боли, исходящей из мышечной и нервной тканей (миалгии, невралгии), при суставной боли (артралгии), а также при болях, исходящих из малого таза.
Особенно выражен анальгетический эффект ненаркотических анальгетиков, в частности салицилатов, при воспалении.
2) Вторым эффектом АА, является жаропонижающий (антипиретический). Этот эффект заключается в снижении лихорадочной, но не нормальной температуры тела. Обычно в качестве жаропонижающих препаратов салицилаты показаны начиная с температуры 38, 5-39 градусов, то есть при температуре, нарушающей общее состояние больного. Это положение особенно касается детей.
При более низких цифрах температуры тела салицилаты в качестве жаропонижающих не рекомендуются, так как лихорадка - это одно из проявлений защитной реакции организма на инфекцию.
3) Третий эффект салицилатов, а значит и АА - это противовоспалительный. Противовоспалительный эффект проявляется в случае наличия воспаления в соединительной ткани, то есть при различных диссеминированных системных заболеваниях ткани или коллагенозах (ревматизм, ревматоидный артрит, болезнь Бехтерева, артралгии, системная красная волчанка).
Начинается противовоспалительный эффект АА после достижения в тканях постоянного уровня салицилатов, а это происходит через 1-2 дня. У больного уменьшаются интенсивность болевой реакции, снижаются экссудативные явления, что клинически проявляется уменьшением припухлости, отечности. Обычно эффект сохраняется в период применения препарата. Уменьшение явлений воспаления, связанных с ограничением (ингибированием) салицилатами экссудативной и пролиферативной фаз воспаления, является причинным элементом болеутоляющего эффекта, то есть противовоспалительный эффект салицилатов усиливает и их анальгетическое действие.
Следует сказать, что у салицилатов все 3 перечисленных фармакологические эффекта по степени выраженности примерно равны.
Помимо перечисленных эффектов для салицилатов характерно также антиагрегационное действие в отношении тромбоцитов крови, а при длительном приеме салицилаты оказывают также десенсебилизирующее действие.
МЕХАНИЗМ ДЕЙСТВИЯ САЛИЦИЛАТОВ
Действие салицилатов связывают с ингибированием (торможением)синтеза простагландинов различных классов. Эти высокоактивные соединения были открыты в 1930 году шведскими учеными. Простагландины в норме в тканях присутствуют в следовых количествах, однако уже при незначительных воздействиях (токсические вещества, некоторые гормоны) их концентрация в тканях резко возрастает. В своей основе простагландины - циклические жирные кислоты с 20-ю атомами углерода в цепочке. Они возникают из свободных жирных кислот, прежде всего из арахидоновой кислоты, попадающих в организм с пищей. Образуются они и из линолевой и линоленовой кислот после их превращения в арахидоновую кислоту. Эти ненасыщенные кислоты входят в состав фосфолипидов. Из фосфолипидов они освобождаются под действием фосфолипазы 2 или фосфолипазы А, после чего становятся субстратом биосинтеза простагландинов. В активации синтеза простагландинов принимает участие ионы кальция.
Простагландины - это клеточные, локальные гормоны.
Первым этапом биосинтеза простагландинов (PG) является окисление арахидоновой кислоты, осуществляемое комплексом PG-циклогеназы-пероксидазы, связанного с микросомальными мембранами. Возникает круговая структура PGG-2, которая под действием пероксидазы переходит в PGH-2. Из полученных продуктов - циклических эндопероксидов - под влиянием PG-изомеразы образуются "классические" простагландины - PGD-2 и PGE-2 (двойка в индексе означает наличие двух двойных связей в цепи; буквы означают вид и положение боковых радикалов циклопентанового кольца).
Под влиянием PG-редуктазы образуется PGF-2 .
Обнаружены ферменты, катализирующие синтез других PG; имеющих особые биологические свойства: PG-I-изомераза, -оксоциклаза, катализирующая образование простациклина (PG I-2) и PG-тромбоксан -А-изомераза, катализирующая синтез тромбоксана А-2 (ТхА-2).
Снижение, подавление синтеза простагландинов под действием салицилатов связывают прежде всего с ингибированием ферментов синтеза PG, а именно ингибированием циклооксигеназ (ЦОГ). Последнее и ведет к снижению синтеза из арахидоновой кислоты провоспалительных простагландинов (особенно PGE-2), потенцирующих активность медиаторов воспаления - гистамина, серотонина, брадикинина. Простагландины, как известно, вызывают гиперальгезию, то есть повышают чувствительность болевых рецепторов к химическим и механическим стимулам.
Таким образом, салицилаты, угнетая синтез простагландинов (PGE-2, PGF-2, PGI-2), предупреждают развитие гиперальгезии. Порог чувствительности к болевым стимулам при этом повышается. Анальгетический эффект наиболее выражен при воспалении. В этих условиях в очаге воспаления происходят освобождение и взаимодействие простагландинов и других "медиаторов воспаления". Простагландины вызывают расширение артериол в очаге воспаления и гиперемию, PGF-2 и ТхА-2 - сужение венул - стаз, те и другие простагландины повышают проницаемость сосудистой стенки, способствуя экссудации жидкости и элементов белой крови, усиливают влияние на сосудистую стенку и других медиаторов воспаления. ТхА-2 способствует образованию тромбоцитарных тромбов, эндоперекиси инициируют свободнорадикальные реакции, повреждающие ткани. Таким образом, Pg способствуют реализации всех фаз воспаления: альтерации, экссудации, пролиферации.
Подавление ненаркотическими анальгетиками, в частности, салицилатами, участия медиаторов воспаления в развитии патологического процесса приводит к утилизации арахидоновой кислоты по липоксигеназному пути и к повышенному образованию лейкотриенов (ЛТД-4, ЛТС-4), в том числе медленно реагирующей субстанции анафилаксии, вызывающей сужение сосудов и ограничение экссудации. Угнетением синтеза простагландинов салицилатами об"ясняется их способность подавлять боль, снижать воспалительную реакцию, а также лихорадочную температуру тела. Жаропонижающий эффект салицилатов заключается в снижении лихорадочной, но не нормальной температуры тела. Лихорадка - одно из проявлений защитной реакции организма на инфекцию. Лихорадка является следствием повышения концентрации в церебральной жидкости PgE-2, что проявляется возрастанием теплопродукции и уменьшением теплоотдачи. Салицилаты, тормозя образование ПГЕ-2, восстанавливают нормальную активность нейронов центра терморегуляции. В итоге увеличивается теплоотдача путем излучения тепла с поверхности кожи и испарения обильных количеств пота. Теплообразование при этом практически не изменяется. Гипотермический эффект салицилатов достаточно отчетлив только при условии их применения на фоне лихорадки. При нормотермии они практически не изменяют температуру тела.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ салицилатов и ацетилсалициловой кислоты (Аспирина)
1) АА применяют в качестве анальгетического средства при невралгиях, миалгиях, артралгиях (суставных болях). Обычно ацетилсалициловая кислота используется для симптоматического лечения ноющей и хронической болей. Препарат эффективен при болях многих типов (при неглубоких, умеренной интенсивности послеоперационных и послеродовых болях, а также при болях, вызванных ранением мягких тканей, при тромбофлебитах поверхностных вен, при головной боли, при дисменорее, альгоменорее).
2) Как жаропонижающее средство при лихорадке, например, ревматической этиологии, при лихорадке инфекционно-воспалительного генеза. Назначение салицилатов с целью снижения температуры тела целесообразно только при очень высокой температуре, которая сказывается неблагоприятно на состоянии больного (39 и больше градусов); т. е. при фебрильной лихорадке.
3) В качестве противовоспалительного средства для лечения больных с воспалительными процессами, в частности при артрите и миозите, используется главным образом ацетилсалициловая кислота. Она уменьшает воспалительную реакцию, но не прерывает ее.
4) В качестве противоревматического средства, при коллагенозах (ревматизм, ревматоидный артрит, СКВ и др.), т. е. при системных диффузных заболеваниях соединительной ткани. В данном случае используются все эффекты, включая десенсибилизирующее действие.
При использовании в высоких дозах салицилаты в течение 24-48 часов резко уменьшают признаки воспаления. Уменьшаются боль, припухлость, неподвижность, повышенная локальная температура, покраснение сустава.
5) В качестве противоагрегирующего средства для профилактики образования пластиночно-фибриновых тромбов. С этой целью аспирин используют в небольших дозах, примерно 150-300 мг/сутки. Ежедневный прием таких доз препарата хорошо зарекомендовал себя для профилактики и лечения внутрисосудистого свертывания крови, для профилактики инфаркта миокарда.
6) Небольшие дозы АСК (600-900 мг) - при профилактическом использовании предупреждают симптомы непереносимости пищевых продуктов. Кроме того АА эффективна при диарее, а также при лучевой болезни.
ПОБОЧНЫЕ ЭФФЕКТЫ
1) Наиболее частым осложнением при применении АСК является раздражение слизистой оболочки желудка (следствие подавления синтеза цитопротекторных простагландинов, в частности PGI-2 простациклина), развитие эрозий, иногда с кровотечением. Двоякая природа данного осложнения: АА - кислота, значит сама раздражает слизистую; угнетение синтеза простагландинов в слизистой, - простациклина, второй способствующий фактор.
У больного салицилаты вызывают диспепсию, тошноту, рвоту, а при длительном применении - могут оказать ульцерогенный эффект.
2) Частым осложнением при приеме салицилатов являются геморрагии (кровоизлияния и кровотечения), являющиеся следствием ингибирования салицилатами агрегации тромбоцитов и антагонизма по отношению к витамину К, необходимому для активации протромбина, проконвертина, IX и X факторов свертывания крови, а также для поддержания нормальной структуры сосудистой стенки. Поэтому при применении салицилатов не только нарушается свертывание крови, но возрастает и ломкость сосудов. Для предупреждения или устранения названного осложнения применяют препараты витамина К. Наиболее часто - викасол, но лучше назначить фитоменадион - аналог витамина К, быстрее всасывающегося, более эффективного и менее токсичного.
3) В больших дозах АА вызывает церебральные симптомы, проявляющиеся шумом в ушах, звоном в ушах, ослаблением слуха, беспокойством, а в более тяжелом случае - галлюцинациями, потерей сознания, судорогами, нарушением дыхания.
4) У лиц, страдающих бронхиальной астмой или обструктивными бронхитами, салицилаты, могут вызывать учащение приступов бронхоспазмов (что является следствием подавления синтеза спазмолитических простагландинов и преимущественного образования лейкотриенов, в том числе медленно реагирующей субстанции анафилаксии из их общего предшественника - арахидоновой кислоты).
5) У отдельных больных могут быть гипогликемические состояния - следствие подавления синтеза ПГЕ-2 и устранения этим его тормозящего влияния на освобождение инсулина из бета-клеток островковой ткани поджелудочной железы.
6) При использовании АА в конце беременности роды могут задерживаться на 3-10 дней. У новорожденных, матери которых по показаниям принимали в конце беременности салицилаты (АА), могут развиваться тяжелые сосудистые заболевания легких. Кроме того, салицилаты (АА), принимаемые во время беременности, могут нарушать ход нормального органогенеза, в частности приводить к незаращению боталового протока (вследствие ингибирования синтеза простагландинов, необходимых для нормального органогенеза).
7) Редко (1: 500), но встречаются аллергические реакции на салицилаты. Непереносимость может проявляться кожными сыпями, крапивницей, зудом, ангионевротическим шоком, тромбоцитопенической пурпурой.
Салициловая кислота - ингредиент многих веществ, в том числе фруктов (яблоки, виноград, апельсины, персики, сливы), входит в состав некоторых сортов мыла, ароматизирующих средств и напитков (особенно березового сока).
Из салицилатов, помимо АА, находит применение НАТРИЯ САЛИЦИЛАТ - этот препарат дает анальгетический эффект, составляющий лишь 60% от такового Аспирина; еще слабее его анальгетический и противовоспалительный эффекты, поэтому его применяют относительно редко. Используют в основном при системных диффузных заболеваниях тканей, при коллагенозах (РА, ревматизм). Аналогичный препарат - метилсалицилат.
Вторая группа ненаркотических анальгетиков - производные пиразолона. К этой группе средств относятся АМИДОПИРИН, БУТАДИОН, а также АНАЛЬГИН.
АМИДОПИРИН (ПИРАМИДОН) (Amidopyrinum порошок; табл. 0, 25). Pyros - огонь. Является мощным анальгетиком и жаропонижающим средством.
Препарат полностью и быстро абсорбируется из кишечника и почти полностью метаболизируется в организме. Однако в связи с высокой токсичностью, в частности выраженным угнетающим влиянием на кроветворение, амидопирин практически не применяют в клинике; исключен из применения как самостоятельное средство и входит лишь в состав некоторых комбинированных препаратов.
АНАЛЬГИН (Analginum; порошок; в табл. по 0, 5; в амп. по 1 и 2 мл - 25% и 50% раствор). Анальгин химически и фармакологически сходен с амидопирином. Анальгин хорошо растворим в воде, поэтому может вводиться и парентерально. Также как и у амидопирина, у данного преепарата анальгетическое действие выражено больше, чем жаропонижающий, а особенно противовоспалительный эффекты.
Применяют анальгин для кратковременного получения анальгетического и жаропонижающего эффектов при невралгиях, миозитах, головной боли, зубной боли. В данном случае используют, как правило, таблетированную форму. В более выраженных случаях, когда надо быстро оказать эффект, используют ин"екции анальгина. При этом анальгин быстро снижает повышенную температуру тела. Назначают анальгин как жаропонижающее только в случае фебрильной лихорадки, когда препарат является первейшим средством скорой помощи. Вводят внутримышечно. Ребенку, надо хорошо помнить, нельзя вводить 1 мл и более, так как может быть литическое падение температуры, что приведет к температурному коллапсу. Ребенку вводят 0, 3-0, 4 мл. Как правило в этом случае к раствору анальгина добавляют димед
рол. Лечение анальгином связано с риском развития осложнений (прежде всего со стороны крови) и поэтому не оправдано его применение в качестве анальгетика и жаропонижающего, когда в равной мере эффективны салицилаты или другие средства.
БАРАЛГИН (Baralginum) - разработан в ФРГ. Очень близкий к анальгину препарат. В таблетированной форме поступает из Болгарии как СПАЗМОЛГОН. Баралгин состоит из анальгина, к которому добавлено еще 2 синтетических вещества (одно из которых обладает папавериноподобным действием, второе слабым ганглиоблокирующим действием). Отсюда понятно, что баралгин показан, прежде всего, при почечной, печеночной, кишечной коликах. Используют его также при спазмах сосудов головного мозга, при головной боли, при мигрени. Выпускают как в таблетках, так и в иньекционной форме.
В настоящее время на лекарственный рынок России поступает целая серия комбинированных препаратов, содержащих анальгин (Максиган, Спазмалгин, Спазган, Вералган и др.)
БУТАДИОН (Butadionum; в табл. по 0, 15). Считают, что бутадион по анальгетической активности примерно равен анальгину, а по противовоспалительной активности существенно выше его. Его и используют поэтому как противовоспалительный препарат. По данному показанию бутадион назначают при поражениях внесуставных тканей (бурситы, тендиниты, синовииты) ревматического и неревматического происхождения. Показан при анкилозирующем спондилите, ревматоидном артрите, остеоартрите.
Максимальная концентрация бутадиона в крови, также как и других производных пиразолона, достигается примерно через 2 часа. Препарат активно связывается с белками плазмы (на 98%). Длительное лечение бутадионом приводит к стимулированию печеночных микросомальных ферментов. Благодаря этому, иногда бутадион в малых дозах используют (0, 005 г/кг в сутки) у детей при гипербилирубинемии. Бутадион снижает реабсорбцию уратов в конечных канальцах, что способствует выведению из организма этих солей этих солей. В этой связи используют при подагре.
Препарат токсичен, отсюда побочные эффекты:
1) как и все производные пиразолона, при длительном использовании может вызвать анорексию, ощущения тяжести в эпигастрии, изжогу, тошноту, рвоту, диарею, образование пептических язв. Может вызвать гепатит, поэтому назначают лишь в течение 5-7 дней;
2) как и все пиразолоновые препараты, бутадион угнетает кроветворение (лейкопения, анемия, тромбоцитопения) до агранулодитоза;
3) при лечении бутадионом может развиваться отечность, так как он задерживает в организме ионы натрия, а значит и воду (снижает натрийурез); это может приводить к застойной недостаточности сердца или даже отеку легких.
РЕОПИРИН (Rheopyrinum)- препарат, представляющий сочетание амидопирина и бутадиона, обладает выраженной противовоспалительной и аналгетической активностью. Используется только как противовоспалительное средство при артритах, ревматических поражениях, люмбаго, аднекситах, параметритах, невралгиях. Кроме того, он, способствуя выведению из организма солей уратов, назначается при подагре. Выпускается как в таблетированной, так и в иньекционной лекарственных формах (Gedeon Rihter).
В последнее время синтезирована группа новых анальгетиков, которые получили название нестероидных противовоспалительных средств - НПВС.
ПРОИЗВОДНЫЕ АНИЛИНА (или более точно - парааминофенола).
Здесь следует указать на два препарата: фенацетин и парацетамол.
Парацетамол как активное аналгезирующее средство и антипиретическое вещество открыто в 1893 году фон Мерингом. В 1995 году было высказано предположение, что парацетамол является метаболитом фенацетина, а в 1948 году Броуди и Аксельрод доказали роль парацетамола как основного метаболита фенацетина. В наше время парацетамол получил широкое распространение как жаропонижающее и анальгезирующее средство на этапе доврачебной фармакологической помощи больному. В этой связи парацетамол является одним из характерных препаратов ОТС-рынка (OTC - jver the counter) т. е. препаратов, продаваемых без рецепта врача. Одной из первых фармакологических компаний, официально представляющей препараты ОТС, и в частности парацетамол (панадол в различных лекарственных формах), является компания "Стерлинг хелз". Несмотря на то, что в настоящее время препарат парацетамол выпускается многими фармацевтическими фирмами под различными названиями (Ацетаминофен, Watsou, USA; Долипран, США-Франция; Миралган, Югославия; Калпол, Wellcome Англия; Дофалган, Франция и пр.), требуются определенные условия для получения чистого продукта. В противном случае лекарственное средство будет содержать фенацетин и 4-р-аминофенол. Именно эти токсические составляющие и не позволяли парацетамолу длительное время занять достойное место в лекарственном арсенале врачей. Западными фирмами, в частности компанией "Sterling Health", парацетамол (панадол) производится в условиях GMP и содержит действующее вещество высокой степени очистки.
МЕХАНИЗМ ДЕЙСТВИЯ ПАРАЦЕТАМОЛА.
Установлено, что парацетамол является слабым ингибитором простагландинового биосинтеза, причем блокирующее действие его на синтез простагландинов - медиаторов боли и температурной реакции - происходит в большей степени в ЦНС, чем на периферии. Этим и объясняется наличие выраженного болеутоляющего и антипиретического действия парацетамола и очень слабого противовоспалительного эффекта. Парацетамол практически не связывается с белками плазмы, легко проникает через гематоэнцефалический барьер, практически равномерно распределяетсяв в головном мозге. Препарат начинает быстрое жаропонижающее и аналгетическое действие примерно через 20-30 минут и продолжает действовать в течение 4 часов. Период полного выведения препарата составляет в среднем 4, 5 часа.
Препарат приемущественно выводится почками (98%), основная часть введенной дозы биотрансформируется в печени. В связи с тем, что парацетамол практически не оказывает влияние на слизистую оболочку желудка, т. е. не вызывает ульцерегенного эффекта. Этим же объясняется отсутствие бронхоспазма при использовании парацетамола даже у лиц, страдающих бронхиальной астмой. Препарат не воздействует, в отличие от аспирина, на систему кроветворения и свертывающую систему крови.
Указанные приемущества, а также большая широта терапевтического действия парацетамола, позволили ему в настоящее время занять достойное место среди других ненаркотических аналгетиков. Препараты, содержащие парацетамол, используются по следующим показаниям:
1) Болевой синдром малой и средней интенсивности различного генеза (головная боль, зубная боль, невралгия, миалгия, боль при травмах, ожогах).
2) Лихорадка фебрильная при инфекционно-воспалительных заболеваниях. Наиболее хорош в качестве жаропонижающего средства в детской практике, в педиатрии.
Иногда производные анилина (фенацетин, например) сочетают в одной таблетке с другими ненаркотическими аналгетиками, получая, таким образом, комбинированные средства. Чаще всего комбинируют фенацетин с АА и кодеином. Известны следующие комбинированные препараты: асфен, седалгин, цитрамон, пиркофен, панадеин, солпадеин.
Побочные эффекты немногочисленны и в большей мере обусловлены введением фенацетина, чем парацетамола. Сообщения о серьезных неблагоприятных реакциях на парацетамол встречаются редко и связаны они, как правило, либо с передозировкой лекарства (более 4, 0 в день), либо с длительным (более 4-х дней) их использованием. Описано всего несколько случаев тромбоцитопении и гемолитической анемии, связанных с приемом лекарства. Наиболее же часто сообщалось о развитии метгемоглобинемии при использовании фенацетина, а также о гепатотоксическом эффекте.
Как правило, современные ненаркотические анальгетики, обладают прежде всего выраженным противовоспалительным эффектом, поэтому их называют чаще всего НПВС.
Это химические соединения различных групп, главным образом соли различных кислот:
а) производные уксусной кислоты: индометацин, сулиндак, ибуфенак, софенак, пранопрофен;
б) производные пропионовой кислоты: ибупрофен, напроксен, кетопрофен, сургам и др.;
в) производные антраниловой кислоты: флуфенамовая кислота, мефенановая кислота, вольтарен;
г) производные никотиновой кислоты: нифлумовая кислота, клониксин;
д) оксикамы (энолиновые кислоты): пироксикам, изоксикам, судоксикам.
Индометацин (Indometacinum; капсулы и драже по 0, 025; суппозитарии - 0, 05) - это нестероидное противовоспалительное средство (НПВС), являющееся производным индолуксусной кислоты (индола). Обладает противовоспалительной, анальгезирующей и жаропонижающей активностью. Это один из самых сильных НПВС, является эталонным НПВС. НПВС - в отличие от салицилатов, вызывают обратимое ингибирование синтетазы простагландинов (ЦОГ).
Используют его противовоспалительный эффект при экссудативных формах воспаления, ревматизме, диссеминированных (системных) заболеваниях соединительной ткани (СКВ, склеродермия, узелковый периартрит, дерматомиозит). Препарат наиболее хорош при воспалительном процессе, сопровождающемся дегенеративными изменениями в суставах позвоночника, при деформирующем остеоартрозе, при псориатической артропатии. Используют при хроническом гломерулонефрите. Очень эффективен при острых атаках подагры, анальгетический эффект длится в течение 2 часов.
У недоношенных детей используют (1-2 раза) для закрытия функционирующего артериального боталлова протока.
Токсичен, поэтому в 25-50% случаев возникают выраженные побочные эффекты (церебральные: головная боль, головокружения, звон в ушах, спутанность сознания, расплывчатость зрительных восприятий, депрессии; со стороны ЖКТ: язвы, тошнота, рвота, диспепсия; кожа: сыпи; кровь: дискразия; задержка ионов натрия; гепатотоксичен). Детям до 14 лет - не рекомендуют.
Следующий НПВС - ИБУПРОФЕН (Ibuprofenum; в табл. по 0, 2) - синтезирован в 1976 году в Англии. Ибупрофен производное фенилпропионовой кислоты. По противовоспалительной активности, анальгетическому и жаропонижающему эффекту близок к салицилатам и даже активнее. Хорошо всасывается из ЖКТ. Лучше переносится больными, чем АА. При приеме внутрь ниже частота побочных реакций. Однако также раздражает ЖКТ (до язвы). Кроме того, при аллергии к пеницилину - больные будут чувствительны и к бруфену (ибупрофен), особенно больные СКВ.
На 92-99% связывается с белками плазмы. Медленно проникает в полость суставов, но задерживается в синовиальной ткани, создавая в ней большие концентрации, чем в плазме крови и медленно исчезая из нее после отмены. Быстро выводится из организма (T 1/2 = 2-2, 5 часа), а потому необходимо частое введение препарата (3-4 раза в день - первую дозу до еды, а остальные - после еды, чтобы удлинить эффект).
Показан при: лечении больных с РА, деформирующем остеоартрозом, анкилозирующим спондилитом, с ревматизмом. Наибольший эффект дает в начальной стадии болезни. Кроме того, ибупрофен используют как сильное жаропонижающее средство.
Близкий препарат к бруфену - НАПРОКСЕН (напросин; табл. по 0, 25) - производное нафтилпропионовой кислоты. Быстро всасывается из ЖКТ, максимальная концентрация в крови - через 2 часа. На 97-98% связан с белками плазмы. Хорошо проникает в ткани и синовиальную жидкость. Обладает хорошим анальгезирующим эффектом. Противовоспалительный эффект приблизительно как у бутадиона (даже выше). Жаропонижающий эффект выше, чем у аспирина, бутадиона. Отличается длительным действием, поэтому его назначают лишь 2 раза в сутки. Хорошо переносится больными.
Применяют его:
1) как жаропонижающее средство; в этом плане он более эффективнее аспирина;
2) как противовоспалительное и анальгезирующее средство при РА, хронических ревматических заболеваниях, при миозитах.
Нежелательные реакции редки, реализуются в форме диспепсических явлений (изжога, боли в животе), головной боли, потливости, аллергических реакций.
Следующий современный НПВС - СУРГАМ или тиопрофеновая кислота (табл. по 0, 1 и 0, 3)- производное пропионовой кислоты. Обладает аналгетическим и противовоспалительным эффектами. Отмечено и жаропонижающее действие препарата. Показания и побочные эффекты те же.
ДИКЛОФЕНАК-НАТРИЙ (вольтарен, ортофен) - производное фенилуксусной кислоты. Это сегодня одно из самых активных противовоспалительных средств, по силе действия примерно равен индометацину. Кроме того, обладает выраженным анальгетическим, а также и жаропонижающим влиянием. По противовоспалительному и анальгетическому эффекту активнее аспирина, бутадиона, ибупрофена.
Хорошо всасывается в ЖКТ, при приеме через рот максимальная концентрация в крови происходит через 2-4 часа. Интенсивно подвергается пресистемной элиминации, и только 60% принятой дозы попадает в систему кровообращения. На 99% связывается с белками плазмы. Быстро проникает в синовиальную жидкость.
Обладает низкой токсичностью, но значительной широтой терапестического действия. Хорошо переносится, иногда лишь вызывая диспепсические и аллергически реакции.
Показан при воспалении любой локализации и этиологии, но преимущественно его используют при ревматизме, РА и других заболеваниях соединительной ткани (при болезни Бехтерева).
ПИРОКСИКАМ (изоксикам, судоксикам) - новый нестероидный противовоспалительный препарат, отличающийся от других НПВС, производное оксикамов.
Удовлетворительно всасывается из ЖКТ. Максимальная концентрация в крови возникает через 2-3 часа. При приеме внутрь он хоршо абсорбируется, период полужизни его около 38-45 часов (это при кратковременном приеме, а при длительном применении - до 70 часов), поэтому он может быть использован один раз в сутки.
ПОБОЧНЫЕ ЭФФЕКТЫ: диспепсия, изредка геморрагии.
Пироксикам ингибирует образование интерлейкина-1, который стимулирует пролиферацию синовиальных клеток и продукцию ими нейтральных протеолитических ферментов (коллагеназы, эластазы) и простагландина E. ИЛ-1 активирует пролиферацию T-лимфоцитов, фибробластов и синовиальных клеток.
В плазме крови на 99% связан с белками. У больных ревматоидным артритом хорошо проникает в синовиальную жидкость. Дозы от 10 до 20 мг (1 или 2 таблетки) вызывают анальгетический (через 30 минут после приема) и жаропонижающий эффекты, а более высокие дозы (20-40 мг) - противовоспалительный (к концу 1 недели постоянного приема). В отличие от аспирина он меньше раздражает ЖКТ.
Препарат используют при РА, анкилозирующем спондилите, остеоартрите и при обострении подагры.
Все названные выше средства, за исключением салицилатов, имеют более выраженное противовоспалительное действие, чем другие средства.
Они хорошо подавляют экссудативное воспаление и сопровождающий его болевой синдром и существенно менее активно воздействуют на альтеративную и пролиферативную фазы.
Эти препараты лучше переносятся больными, чем аспирин и салицилаты, индометацин, бутадион. Данные препараты именно поэтому стали в основном использоваться как противовоспалительные средства. Отсюда они получили и название - НПВС (нестероидные противовоспалительные средства). Однако, кроме этих новых НПВС, к нестероидным ПВС по большому счету относят сейчас и старые средства - ненаркотические анальгетики.
Все новые НПВС менее токсичны, чем салицилаты и индометацин.
На деструктивные процессы в хрящевой и костной тканях НПВС не только не оказывают тормозящего влияния, но в ряде случаев могут даже их провоцировать. Они нарушают способность хондроцитов синтезировать ингибиторы протеаз (коллагеназы, эластазы) и этим усиливают повреждение хряща и костей. Ингибируя синтез простагландинов, НПВС тормозят синтез гликопротеинов, гликозаминогликанов, коллагена и других протеинов, необходимых для регенерации хрящей. К счастью, ухудшение наблюдается лишь у некоторых больных, у большинства же ограничение воспаления может предотвратить дальнейшее развитие патологического процесса.
АНАЛЬГЕЗИ́РУЮЩИЕ СРЕ́ДСТВА (анальгетики), лекарственные препараты, ослабляющие или устраняющие чувство боли. Анальгезирующее (болеутоляющее) действие оказывают препараты различных фармакологических групп. Наиболее выражено оно у наркотических, опиоидных А. с., которые взаимодействуют с опиоидными рецепторами. Их используют в анестезиологии гл. обр. для общей анестезии и послеоперационного обезболивания; при травмах и заболеваниях с выраженным болевым синдромом (злокачественные новообразования, инфаркт миокарда и др.). Основные представители этой группы А. с. – морфин, фентанил (ремифентанил), омнопон, промедол, тримеперидин, просидол, буторфанол, морадол, стадол, налбуфин, трамадол. Наркотические А. с. обладают сильной анальгезирующей активностью, могут вызывать лекарственную зависимость, абстинентный синдром , при передозировке развивается глубокий сон, переходящий в стадию наркоза, затем комы, ведущей к параличу дыхательного центра.
Бупренорфин (полусинтетическое производное алкалоида тебаина) по анальгетической активности в 20–50 раз превосходит морфин; назначают для купирования интенсивных болей после небольших полостных операций; благодаря таблетированной форме незаменим для неотложной медицины при массовых травматических поражениях.
Универсальным антагонистом опиоидных А. с. является наксолон, который блокирует их связывание или вытесняет их из опиоидных рецепторов всех типов. Его применяют для быстрого прекращения действия опиоидов, в т. ч. при их передозировке (посленаркозное угнетение дыхания, острое отравление опиоидами и др.).
К ненаркотическим А. с. относятся производные пиразолона (амидопирин, анальгин, антипирин, баралгин, бутадион, реопирин), анилина (антифебрин, парацетамол, фенацетин), салициловой кислоты (ацетилсалициловая кислота, натрия салицилат, салициламид, дифлунизал, тосибен). По болеутоляющей активности они значительно уступают наркотическим А. с., обладают жаропонижающим действием при лихорадочных состояниях. Выраженным противовоспалительным действием обладают соединения различных групп, гл. обр. соли различных кислот: производные уксусной кислоты (индометацин, ибуфенак, сулиндак, софенак, пранопрофен); пропионовой кислоты (ибупрофен, кетопрофен, напроксен и др.); антраниловой кислоты (вольтарен и др.); никотиновой кислоты (клониксин); оксикамы (пироксикам). Кроме того, они эффективны лишь при некоторых видах болей (невралгической, головной, зубной, мышечной, суставной). Ненаркотические А. с. не оказывают снотворного действия, не влияют на дыхательный и кашлевой центры, на условно-рефлекторную деятельность, не вызывают эйфории и лекарственной зависимости.