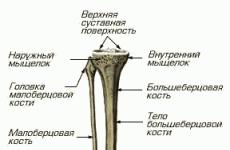
Прогрессирующая мультифокальная лейкоэнцефалопатия симптомы. Почему невозможно вылечить лейкоэнцефалопатию головного мозга: особенности течения и причин заболевания Симптомы пмл
Лекарственных препаратов, способных остановить развитие заболевания, в настоящее время не существует.
Описание
Лейкоэнцефалопатия – заболевание, характеризующееся стойким разрушением в головном мозге белого вещества. Болезнь развивается быстро и практически всегда приводит к летальному исходу.
Патология впервые описана Людвигом Бинсвангером в 1964 г., поэтому иногда ее называют болезнью Бинсвангера.
Причины
Принято выделять 3 основные причины, приводящие к лейконэнцефалопатии. Это гипоксия, стабильно высокое давление и вирусы. Провоцируют ее возникновение следующие заболевания и состояния:
- эндокринные нарушения;
- гипертония;
- атеросклероз;
- злокачественные опухоли;
- туберкулез;
- ВИЧ и СПИД;
- патологии позвоночника;
- генетический фактор;
- родовая травма;
- прием препаратов, снижающих иммунную реакцию организма.
Провоцирующее действие вредоносных факторов ведет к демиелинизации пучков нервных волокон. Белое вещество уменьшается в объеме, размягчается, изменяет структуру. В нем появляются кровоизлияния, очаги поражения, кисты.
Часто демиелинизацию вызывают полиомавирусы. В неактивном состоянии они присутствуют в жизни человека постоянно, сохраняясь в почках, костном мозге, селезенке. Ослабление иммунитета приводит к активизации вирусов. Лейкоциты переносят их в центральную нервную систему, где они находят благоприятную среду в мозге, поселяются в нем и разрушают его.
Обычно необратимым изменениям подвергается только белое вещество. Однако есть данные и о том, что, вероятно, перивентрикулярный вид лейкоэнцефалопатии ведет также к поражению серого вещества.
Классификация
Определение основной причины патологии и характера ее течения позволяет выделять несколько типов лейкоэнцефалопатии.
Дисциркуляторная
Основной причиной появления и развития мелкоочаговой лейкоэнцефалопатии сосудистого генеза является поражение сосудов мозга, вызванное гипертонией, травмами, появлением атеросклеротических бляшек, эндокринными заболеваниями, болезнями позвоночника. Кровообращение нарушается из-за сгущения крови и закупорки сосудов. Ухудшающим состояние фактором является алкоголизм и ожирение. Считается, что болезнь развивается при наличии отягчающих наследственных факторов.
Данную патологию называют также прогрессирующей сосудистой лейкоэнцефалопатией. Сначала появляются небольшие очаги поражения сосудов, потом они увеличиваются в размерах, вызывая ухудшение состояния больного. С течением времени нарастают признаки патологии, заметные окружающим. Ухудшается память, снижается интеллект, возникают психоэмоциональные расстройства.
Больной жалуется на тошноту, головную боль, постоянную усталость. Сосудистая мелкоочаговая энцефалопатия характеризуется скачками давления. Человек не может глотать, с трудом пережевывает пищу. Появляется тремор, отличающий болезнь Паркинсона. Утрачивается способность контролировать процессы мочеиспускания и дефекации.
Очаговая энцефалопатия сосудистого генеза регистрируется в основном у мужчин после 55 лет. Ранее данное нарушение было включено в список МКБ, но в дальнейшем его исключили.
Прогрессирующая мультифокальная
Главной особенностью этого типа нарушения считается появление большого количества очагов повреждения. Вызывают воспаление полиомавирус человека 2 (JC polyomavirus). Он обнаруживается у 80% жителей Земли. В скрытом состоянии живет в организме несколько лет, но при ослаблении иммунитета активируется и, попадая в ЦНС, вызывает воспаление.
Провоцирующими заболевание факторами являются СПИД, ВИЧ-инфицирование, длительное применение иммунодепрессантов и лекарств, предназначенных для лечения онкологических заболеваний. Прогрессирующая мультифокальная энцефалопатия диагностируется у половины пациентов со СПИДом и 5% людей с ВИЧ-инфекцией.

Поражение часто имеет асимметричный характер. Признаками ПМЛ являются параличи, парезы, ригидность мышц, тремор, напоминающий болезнь Паркинсона. Лицо приобретает вид маски. Возможна потеря зрения. Проявляются тяжелые когнитивные нарушения, снижение внимания.
Мультифокальная лейкоэнцефалопатия не лечится. Для улучшения состояния больного убирают препараты, подавляющие иммунитет. Если заболевание вызвано пересадкой органа, он подлежит удалению.
Перивентрикулярная
Лейкопатию головного мозга у ребенка вызывает гипоксия, возникшая при родах. Инструментальные методы диагностики позволяют увидеть участки гибели ткани, преимущественно рядом с мозговыми желудочками. Перивентрикулярные волокна несут ответственность за двигательную активность, и их поражение ведет к детскому церебральному параличу. Очаги поражения возникают симметрично, в особо тяжелых случаях обнаруживаются во всех центральных зонах мозга. Поражение характеризуется прохождением 3 стадий:
- возникновение;
- развитие, приводящее к структурным изменениям;
- образование кисты или рубца.
Перивентрикулярная лейкоэнцефалопатия характеризуется 3 степенями заболевания. Легкая степень характеризуется незначительной выраженностью симптомов. Обычно они проходят через неделю после рождения. Для средней степени характерно повышение внутричерепного давления, возникают судороги. При тяжелой ребенок находится в коме.
Симптомы появляются не сразу, некоторые из них можно заметить только через 6 месяцев после рождения ребенка. Чаще всего обращают на себя внимание парезы и парализация. Наблюдается косоглазие, заторможенность, гиперактивность.
Лечение включает массаж, физиопроцедуры, специальные комплексы упражнений.
Лейкоэнцефалопатия с исчезающим белым веществом
Основной причиной этого заболевания являются мутации генов, подавляющие белковый синтез. Чаще всего появляется у детей, преимущественно в возрасте от двух до шести лет. К провоцирующим факторам относят сильное психическое напряжение, вызванное травмой или тяжелой болезнью.
Органические поражения головного мозга имеют общее название — энцефалопатия. Аномальный процесс сопровождается дистрофическими изменениями мозговой ткани.
Один из видов патологии носит название «прогрессирующая мультифокальная лейкоэнцефалопатия» и может закончиться смертью пациента.
Для того чтобы понимать, что такое лейкоэнцефалопатия, следует рассмотреть причины ее возникновения, классификацию и основные методы лечения.
 Заболевание, в результате которого под воздействием различных факторов поражается белое вещество мозга, называется лейкоэнцефалопатией головного мозга. Очаговые разрушения мозговой ткани происходят из-за неправильной циркуляции крови в сосудах головы, заражения человека вирусом. Развитию болезни способствует наследственная предрасположенность.
Заболевание, в результате которого под воздействием различных факторов поражается белое вещество мозга, называется лейкоэнцефалопатией головного мозга. Очаговые разрушения мозговой ткани происходят из-за неправильной циркуляции крови в сосудах головы, заражения человека вирусом. Развитию болезни способствует наследственная предрасположенность.
Последствия заболевания тяжелые: развивается слабоумие, существенно снижается зрение, появляются судорожные припадки. Летальный исход регистрируется в большинстве случаев.
В зависимости от места поражения головного мозга, выделено несколько видов лейкоэнцефалопатии.
Дисциркуляторная энцефалопатия
Это заболевание развивается из-за поражения мелких артерий и артериол в мозговой ткани. Неправильный кровоток в сосудах мозга приводит к разрушению белого вещества мозговой ткани.
Дистрофические изменения могут происходить вследствие различных причин: нарушения кровообращения, патологии сосудов, черепно-мозговые травмы. Основным фактором, приводящим к деструкции мозговой ткани, является постоянная гипертензия, наличие атеросклеротических отложений на васкулярных стенках.
Другое название патологии — прогрессирующая сосудистая лейкоэнцефалопатия. Со временем мелкие очаги поражения белого вещества мозга разрастаются, в связи с чем состояние больного ухудшается. Наблюдаются следующие симптомы:
- ухудшение памяти, умственных способностей;
- развитие слабоумия;
- появление признаков синдрома паркинсонизма;
- расстройства вестибулярного аппарата: головокружения, тошнота;
- трудности с приемом пищи: медленное жевание еды, проблемы с глотанием;
- перепады артериального давления.
При развитии процесса больной становится неспособен контролировать процессы дефекации и мочеиспускания.
Мелкоочаговая лейкоэнцефалопатия сосудистого генеза вначале слабо выражена. Развитию деструкции мозговой ткани сопутствуют расстройства психики, хроническое переутомление, нарушения памяти, головокружение.
Прогрессивная мультифокальная лейкоэнцефалопатия
Для этого вида патологии характерно появление множественных очагов, где наблюдается поражение мозга. Прогрессирующая мультифокальная лейкоэнцефалопатия (кратко ПМЛ) вызывается полиомавирусом человека 2, заражение которым обычно происходит в детском возрасте.
Несмотря на то что это вирус можно обнаружить у 80% населения, мультифокальное поражение мозга – довольно редкое заболевание.
Прогрессирующая многоочаговая лейкоэнцефалопатия развивается на фоне практически полной утраты иммунитета, поэтому ей чаще всего подвержены больные СПИДом, люди, перенесшие иммуноподавляющую терапию, страдающие новообразованиями лимфатической системы.
Пациенты, в анамнезе которых присутствует атеросклероз, часто проходят курс лечение препаратами, вызывающими иммунодефицит.
Поэтому риск возникновения ПМЛ у больных, страдающих атеросклерозом, очень высокий.
Начинается прогрессирующая многоочаговая лейкоэнцефалопатия остро, прогрессирует стремительно, ее признаки:
- нарушения речи и зрения;
- значительное расстройство моторики рук;
- сильные головные боли;
- парезы конечностей с правой или левой стороны тела;
- нарушения чувствительности.
При прогрессировании заболевания происходит утрата памяти и ухудшение умственных способностей.
Специфическое медикаментозное лечение мультифокального поражения мозговой ткани не найдено. В случаях, если поражение вызвано иммуносупрессивной терапией, ее прекращают.
Если заболевание стало следствием трансплантации органа, его могут удалить. Все методы лечения направлены на восстановление защитных функций организма.
К сожалению, если не удается улучшить функционирование иммунной системы, прогноз неблагоприятный. На вопрос о том, сколько живут при таком виде патологии, можно ответить, что очень мало. Смерть может наступить в течение 2 лет с момента постановки диагноза, если лечение не дает результатов.
Перивентрикулярная лейкомаляция
 При этой форме энцефалопатии поражение мозга происходит в результате появления в подкорковых структурах очагов некроза, чаще всего вокруг желудочков. Оно является результатом гипоксии, диагноз «перивентрикулярная лейкоэнцефалопатия» часто ставят новорожденным, пережившим кислородное голодание из-за сложных родов.
При этой форме энцефалопатии поражение мозга происходит в результате появления в подкорковых структурах очагов некроза, чаще всего вокруг желудочков. Оно является результатом гипоксии, диагноз «перивентрикулярная лейкоэнцефалопатия» часто ставят новорожденным, пережившим кислородное голодание из-за сложных родов.
Перивентрикулярные зоны белого вещества отвечают за движение, поэтому некроз их отдельных участков приводит к возникновению ДЦП. Подробно перивентрикулярная лейкомаляция была исследована советским ученым В. В. Власюком. Он не только исследовал патогенез, этиологию, стадии поражения мозга.
В. В. Власюк пришел к выводу о хронической форме болезни, с течением времени к пораженным участкам присоединяются новые.
Мелкоочаговые некрозы (инфаркты) присутствуют в белом веществе и чаще всего расположены симметрично в мозговых полушариях. В тяжелых случаях поражения могут распространяться на центральные отделы мозга.
Некрозы проходят несколько стадий:
- развитие;
- постепенное изменение структуры;
- формирование рубца или кисты.

Выделено несколько степеней проявления лейкомаляции.
Такие как:
- легкая. Симптомы наблюдаются до недели с момента рождения, выражены в легкой форме;
- средняя. Признаки сохраняются в течение 10 дней, могут возникать судороги, наблюдается повышенное внутричерепное давление;
- тяжелая. Сохраняется очень длительное время, ребенок впадает в кому.

Симптомы перивентрикулярной лейкомаляции различны:
- парезы;
- параличи;
- появление косоглазия;
- задержка развития;
- гиперактивность или, наоборот, угнетение нервной системы;
- пониженный тонус мышц.
Иногда неврологические нарушения в первые месяцы жизни ребенка не выражены и проявляются только через полгода. По прошествии времени появляются симптомы нарушения деятельности нервной системы, может наблюдаться судорожный синдром.
Лечение перивентрикулярной лейкоэнцефалопатии проводится с использованием медикаментозных препаратов. Важную роль играют физпроцедуры, массаж, лечебная гимнастика. Таким пациентам требуется повышенное внимание, обязательны систематические прогулки на свежем воздухе, игры, общение со сверстниками.
Лейкоэнцефалопатия с исчезающим белым веществом
 Этот вид поражения вызван генными мутациями в хромосоме, которые подавляют синтез белка. Заболеванию подвержены все возрастные категории, но классическая форма болезни возникает у детей от 2-6 лет.
Этот вид поражения вызван генными мутациями в хромосоме, которые подавляют синтез белка. Заболеванию подвержены все возрастные категории, но классическая форма болезни возникает у детей от 2-6 лет.
Толчком для ее начала становится пережитый стресс: тяжелая инфекция, травмы, перегревание и т. д. Впоследствии у ребенка обнаруживается тяжелая гипотония, ослабление мышц, он может впасть в кому, даже умереть.

Во взрослом возрасте патология может проявиться после 16 лет следующими симптомами:
- психоз;
- слабоумие;
- депрессия.
Частым признаком такого вида энцефалопатии у взрослых женщин являются нарушения функционирования яичников. В крови регистрируется повышенное содержание гонадотропинов и пониженное — эстрогенов и прогестерона.
Страдающие данным видом патологии испытывают трудности в учебе, у них наблюдаются неврологические расстройства, мышечная слабость и нарушения мелкой моторики рук.
Медикаментозное лечение, которое бы непосредственно устраняло генные нарушения, отсутствует. Для предупреждения появления приступов рекомендуется избегать травм головы, запрещается перегреваться, если возникает температура, следует обязательно применять жаропонижающие препараты.
Методы диагностики
Прежде чем будет поставлен диагноз, следует пройти полное обследование. Для этого нужно, чтобы специалист исследовал головной мозг с помощью специальной аппаратуры. Применяются следующие методы диагностики:
- магнитно-резонансная томография;
- компьютерная томография;
- электроэнцефалография;
- доплерография.
Возможно проведение исследования с помощью инвазивных методов изучения мозговой ткани. К ним относятся биопсия и люмбальная пункция. Забор материала может привести к осложнениям, так как связан с непосредственным проникновением в ткани мозга. Люмбальная пункция проводится, когда необходим забор спинномозговой жидкости.
При подозрении на заражение вирусом или наличие генных мутаций могут назначить ПЦР-диагностику (метод полимеразной цепной реакции). Для этого в лаборатории исследуют ДНК больного, выделенную из его крови. Точность диагноза при этом довольно высокая и составляет около 90%.
Терапия
Лечение энцефалопатии, связанной с поражением белого вещества мозга, направлено на устранение причин, его вызвавших. Терапия включает прием медикаментозных препаратов и применение нелекарственных методов.
Для лечения заболеваний сосудов, вызвавших энцефалопатию, применяются средства, направленные на восстановление их нормального функционирования. Они призваны нормализовать кровоток в мозговых тканях, устранить проницаемость васкулярных стенок. При необходимости назначаются средства, разжижающие кровь.
Показан прием ноотропных препаратов, стимулирующих деятельность головного мозга. Рекомендован прием витаминов, иммуностимулирующих медикаментов. Нелекарственные методы включают:
- лечебную гимнастику;
- массаж;
- физиотерапию;
- иглоукалывание.
Возможна работа с логопедами, психологами, мануальными терапевтами. Можно увеличить продолжительность жизни пациента, это зависит от интенсивности терапии, общего состояния здоровья больного. Но полностью излечить патологию невозможно.
Заключение
 Рассказывая, почему возникает лейкоэнцефалопатия головного мозга, что это такое и каковы ее последствия, прежде всего нужно упомянуть о сложности ее диагностики, лечения. Деструкция белого вещества мозга приводит к серьезным последствиям, вплоть до смерти.
Рассказывая, почему возникает лейкоэнцефалопатия головного мозга, что это такое и каковы ее последствия, прежде всего нужно упомянуть о сложности ее диагностики, лечения. Деструкция белого вещества мозга приводит к серьезным последствиям, вплоть до смерти.
При генетических патологиях, вызывающих разрушение мозговой ткани, необходим регулярный контроль здоровья пациента. Специальных препаратов для исправления дефектных генов не существует.
В большинстве случаев заболевание заканчивается смертью. Можно лишь замедлить прогрессирование болезни путем повышения иммунитета организма и устранения внешних обстоятельств, усугубляющих поражение мозга.
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ) - это тяжелое демиелинизирующее заболевание ЦНС. Возбудителем этого заболевания является вирус JC из группы ДНК-содержащих полиомавирусов, который распространен по всему миру.
Свое название вирус получил по инициалам больного по имени Джон Каннингхэм (John Cunningham), от которого этот простой ДНК-вирус был впервые выделен в 1971 г.
Вопреки распространенному заблуждению, вирус JC никак не связан с синдромом Крейтцфельда-Якоба .
Поскольку доля лиц, имеющих антитела к этому вирусу, среди населения достигает 80%, предполагается возможность скрытой пожизненной инфекции.
По-видимому, вирус в основном сохраняется в почках и костях. Реактивация вируса с развитием симптомов инфекции происходит только при нарушении клеточного иммунитета.
В наибольшей степени страдает белое вещество полушарий головного мозга, но возможно также поражение мозжечка и серого вещества.
ПМЛ - классическая оппортунистическая инфекция. Нередко у больных отмечается тяжелый иммунодефицит, однако для развития ПМЛ он не обязателен. В отличие от ЦМВ-инфекции и инфекции, вызванной атипичными микобактериями, ПМЛ не всегда служит признаком терминальной стадии ВИЧ-инфекции.
Хотя, как правило, ПМЛ развивается при количестве лимфоцитов CD4 менее 100 мкл –1 , она возможна и при количестве лимфоцитов CD4 более 200 мкл –1 .
Диагностика
- МРТ. При МРТ обычно выявляются очаги повышенной интенсивности сигнала на T2-взвешенных изображениях и последовательности FLAIR; эти очаги имеют сниженную интенсивность на T1-взвшенных изображениях, как правило, не усиливаются гадолинием и не вызывают масс-эффект.
Восстановление иммунитета на фоне АРТ может привести к выраженному воспалительному компоненту с существенным усилением контрастирования. Поражения серого вещества не типичны, поскольку это лейкоэнцефалопатия. Также следует отметить, что очаги почти всегда располагаются асимметрично.
Во многих случаях МРТ позволяет отличить ПМЛ от церебрального токсоплазмоза и лимфомы. Однако классические - обширные, затрагивающие все полушарие - очаги поражения, которые обычно описываются в литературе, обнаруживаются не всегда. Развитие ПМЛ начинается с маленького очага, поэтому наличие одного или нескольких маленьких очагов, расположенных вдали друг от друга, не позволяет исключить диагноз. ПМЛ может развиться в любой части головного мозга, типичной локализации нет. Очаги нередко обнаруживаются в теменной и затылочной областях или перивентрикулярно, однако могут обнаруживаться и в мозжечке. Важно, чтобы МР-томограммы обязательно посмотрел специалист по лучевой диагностике (или врач-клиницист), имеющий опыт в диагностике ПМЛ. Но даже в этом случае ПМЛ бывает трудно отличить от инфекции, вызванной вирусом герпеса человека 6-го типа, и ВИЧ-лейкоэнцефалопатии.
Таким образом, клиническая картина и данные, полученные с помощью лучевых методов диагностики, не позволяют поставить точный диагноз.
- Для уточнения диагноза необходимо выполнить исследование СМЖ. Как правило, если нет сопутствующих инфекций, то в СМЖ отсутствуют признаки неспецифического воспаления, хотя общий уровень белка часто немного повышен. Цитоз обнаруживается редко, и, если он достигает 100/3, диагноз ПМЛ маловероятен.
- У всех больных нужно исследовать СМЖ на вирус JC. Чувствительность новых методик на основе ПЦР составляет около 80%, а специфичность - более 90%. Образец СМЖ для исследования нужно направить в лабораторию, имеющую опыт выявления вируса JC. При характерных клинической картине и результатах, полученных с помощью лучевых методов диагностики, в сочетании с положительным результатом ПЦР на вирус JC диагноз ПМЛ можно установить с достаточной степенью вероятности. В этих случаях выполнять биопсию головного мозга сегодня не рекомендуется. Тем не менее, отрицательный результат ПЦР не исключает ПМЛ. Уровень вирусной нагрузки JC в СМЖ может колебаться в значительной степени и не коррелировать с распространенностью поражений К сожалению, ПЦР на вирус JC в настоящее время стала менее информативной, поскольку на фоне АРТ концентрация вируса в СМЖ у многих пациентов очень низкая или даже неопределимая.
- Некоторым больным может потребоваться проведение стереотаксической биопсии головного мозга.
Лечение
Специфического лечения ПМЛ не существует. Рекомендуется своевременное назначение
«ОБЗОР Инфекция головного мозга вирусом JC A. K. Bag, J. K. Cur, РЕЗЮМЕ: С тех пор как инфекция головного мозга вирусом JC была P. R. Chapman, описана впервые, в...»
Инфекция головного мозга вирусом JC
РЕЗЮМЕ: С тех пор как инфекция головного мозга вирусом JC была
описана впервые, в эпидемиологии, патогенезе, симптомах и данных
лучевой диагностики произошли значительные изменения. Самое частое
проявление инфекции - прогрессирующая мультифокальная
лейкоэнцефалопатия (ПМЛ). Недавно описаны и другие проявления -
вызванная вирусом JC энцефалопатия (JC-Э), нейропатия зернистых
клеток мозжечка (JC-НЗК) и менингит (JC-М). Хотя основным предрасполагающим фактором реактивации вируса является СПИД, признаки инфекции головного мозга вследствие реактивации вируса все чаще встречаются в отсутствие ВИЧ-инфекции, в том числе на фоне ревматических, гематологических и онкологических заболеваний; при терапии моноклональными антителами; у реципиентов после трансплантации; при первичных иммунодефицитах; а иногда даже в отсутствие иммунодефицита. У ВИЧ-положительных пациентов с ПМЛ, получающих антиретровирусную терапию, после восстановления иммунитета возможно развитие ВСВИ. Этот синдром может иметь очень тяжелые последствия, и его необходимо диагностировать как можно быстрее. Лучевая диагностика играет ключевую роль в диагностике инфекции, оценке эффективности лечения, при наблюдении за прогрессированием заболевания и прогнозе. Данная статья представляет собой обзор современных взглядов на эпидемиологию, патогенез, клиническую картину и все аспекты лучевой диагностики при инфекции головного мозга вирусом JC.
СОКРАЩЕНИЯ: ВААРТ = высокоактивная антиретровирусная терапия; ВИЧ = вирус иммунодефицита человека; вПМЛ = воспалительная ПМЛ; ВСВИ = воспалительный синдром восстановления иммунитета; ИКД = измеряемый коэффициент диффузии;
кПМЛ = классическая ПМЛ; КПН = коэффициент передачи намагниченности; Кр = креатин; НАА = N-ацетиласпартат; НВСВИ = нейро-ВСВИ; ПМЛ = прогрессирующая мультифокальная лейкоэнцефалопатия; ПМЛ-ВСВИ = ПМЛ, связанная с ВСВИ; ПЦР = полимеразная цепная реакция; РС = рассеянный склероз; СКВ = системная красная волчанка; СМЖ - спинномозговая жидкость; ЦНС = центральная нервная система;
FLAIR = методика FLAIR (обеспечивающая подавление сигнала свободной воды); JC-М = менингит, вызванный вирусом JC; JC-НЗК = нейропатия зернистых клеток мозжечка, вызванная вирусом JC; JC-Э = энцефалопатия, вызванная вирусом JC.
Вирус JC, относящийся к семейству полиомавирусов, впервые был выделен в 1971 г. из головного мозга больного лимфогранулематозом1, хотя само заболевание было описано Astrom et al в 1958 г.2. Вызываемая вирусом демиелинизирующая энцефалопатия позднее получила название прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ). До 1980-х гг. ПМЛ считалась крайне редкой оппортунистической инфекцией. Пандемия ВИЧинфекции привела к появлению новой группы пациентов с иммунодефицитом, и распространенность ПМЛ резко выросла. В настоящее время иммунодефицит, вызванный ВИЧ - самый частый фактор, предрасполагающий к клинически выраженной инфекции вирусом JC. Рост распространенности ПМЛ вследствие ВИЧ-инфекции стал причиной интенсивных исследований, посвященных инфекции, вызванной вирусом JC, что улучшило наши представления о меняющейся эпидемиологии и постоянно расширяющемся спектре ее патологических проявлений. Также теперь известно, что картина заболевания по данным лучевой диагностики является более разнообразной и сложной, чем считалось ранее, а новейшие методы терапии ВИЧ-инфекции и ПМЛ оказывают на нее существенное Отделение рентгенологии, кафедра нейрорентгенологии, университет Алабамы при медицинском центре Бирмингема, Бирмингем, Алабама.
Корреспонденцию направлять Asim K. Bag, MD, кафедра нейрорентгенологии, отделение рентгенологии, университет Алабамы при медицинском центре Бирмингема, 619 19th St S, WP-150, Birmingham, AL-35249-6830; e-mail: [email protected] Указывает на свободный доступ к статье для всех желающих по адресу www.ajnr.org DOI 10.3174/ajnr.A2035 влияние. Данная статья представляет собой обзор проявлений инфекции вирусом JC, в том числе ПМЛ, с упором на все большее разнообразие картины лучевой диагностики.
Эпидемиология: группы риска Сейчас стало ясно, что понятие ПМЛ уже не соответствует своему определению. Инфекция вирусом JC уже не является оппортунистической инфекцией, связанной только с ВИЧинфекцией и лимфопролиферативными заболеваниями. Хотя примерно 80% случаев ПМЛ вызваны ВИЧ, она все чаще встречается в отсутствие ВИЧ-инфекции3.
Вирус JC - очень распространенный патоген; в качестве основных путей передачи предлагались как воздушно-капельный, так и алиментарный, вследствие употребления зараженной вирусом воды4,5. Первичная инфекция, скорее всего, бессимптомна; у 85% взрослого населения есть антитела к вирусу, что указывает на предшествующее заражение и, возможно, латентную инфекцию6. Как правило, для реактивации вируса требуется тяжелая недостаточность клеточного иммунитета (T-лимфоцитов)6. Подавление клеточного иммунитета при ВИЧ-инфекции - наиболее частая причина реактивации вируса JC: ВИЧинфицированные составляют примерно 80% пациентов с ПМЛ. Реже причиной развития ПМЛ становятся гемобластозы (13%), трансплантация внутренних органов (5%) и аутоиммунные заболевания, при которых назначают иммуномодуляторы (3%)6.
Эпидемиологическое описание инфекции вирусом JC основывается на ПМЛ, поскольку это наиболее частое проявление инфекции.
ПМЛ на фоне ВИЧ-инфекции В настоящее время иммунодефицит, вызванный инфекцией ВИЧ-1/СПИДом - наиболее частое состояние, провоцирующее реактивацию вируса JC и развитие ПМЛ. Относительно ПМЛ на фоне инфекции ВИЧ-2 есть лишь отдельные сообщения7,8, что может быть связано с различиями в региональной распространенности ВИЧ-2: он значительно чаще встречается в Африке, чем в развитых странах Европы и Северной Америки7. Чтобы подтвердить диагноз ПМЛ, требуются сложные современные технологии, не всегда доступные в большинстве развивающихся стран, и поэтому частота ПМЛ может быть искусственно заниженной.
Основой лечения ВИЧ-инфекции сегодня стала ВААРТ, благодаря которой продолжительность жизни больных заметно выросла. ВААРТ привела к значительному снижению частоты ПМЛ9. До ее внедрения ПМЛ развивалась у 3–7% пациентов с ВИЧ-1, и на ее долю приходилось до 18% поражений ЦНС со смертельным исходом10,11. Частота ПМЛ снизилась с 0,7 на 100 человек за год наблюдений в 1994 г. до 0,07 в 2001–2002 гг.11. В отличие от многих других оппортунистических инфекций ЦНС, инфекция вирусом JC развивается на ранних стадиях СПИДа при числе лимфоцитов CD4 200 мкл–1 и может развиться на фоне ВААРТ12. Годичная выживаемость у ВИЧ-инфицированных с ПМЛ также значительно выросла, с 0–30% до появления ВААРТ до 38–62% на ее фоне13,14. Однако согласно исследованию, проведенному в 2005 г., ПМЛ все еще является второй про распространенности (14%) причиной смерти от СПИДа, уступая только неходжкинской лимфоме14.
ПМЛ при гемобластозах и злокачественных опухолях Впервые ПМЛ была описана в 1958 г. у пациентов с хроническим лимфолейкозом и лимфогранулематозом2. Масштабный обзор Garcia-Suarez et al15 охватывает все описанные в период с 1958 по 2004 гг. случаи ПМЛ на фоне лимфопролиферативных заболеваний. В частности, описано развитие ПМЛ на фоне хронического лимфолейкоза, лимфогранулематоза, неходжкинской лимфомы, макроглобулинемии Вальденстрема, множественной миеломы и грибовидного микоза. Основными факторами риска ПМЛ в этих случаях являются лимфогранулематоз в отсутствие лечения, терапия структурными аналогами пуринов и трансплантация стволовых клеток.
ПМЛ после трансплантации внутренних органов Трансплантация органов, при которой иммунитет подавляется искусственно, нередко становится причиной ПМЛ. Медиана времени до развития заболевания составляет 17 мес, при трансплантации почки несколько дольше, поскольку в этих случаях иммуносупрессию проводят не так агрессивно16. ПМЛ описана также после трансплантации стволовых клеток - как аутологичной, так и аллогенной17.
ПМЛ при ревматических заболеваниях В недавнем обзоре Calabrese et al18 рассмотрены 37 случаев ПМЛ на фоне ревматических заболеваний. Все пациенты до развития ПМЛ получали те или иные иммунодепрессанты.
Чаще всего (65%) ПМЛ развивалась на фоне СКВ, а также на фоне ревматоидного артрита, гранулематоза Вегенера, дерматомиозита, полимиозита и системной склеродермии. Есть также сообщения о ПМЛ у пациентов с синдромом Шегрена19 и саркоидозом20, не получавших иммунодепрессантов, в обоих случаях - на фоне лимфопении. До конца не ясно, что спровоцировало ПМЛ в этих случаях, лимфопения или ревматическое заболевание.
ПМЛ при терапии моноклональными антителами В последние годы моноклональные антитела применяются при лечении самых разных иммунных заболеваний. Некоторые из них подавляют иммунитет, что предрасполагает к развитию ПМЛ. В медицинской литературе широко обсуждается связь между ПМЛ и применением натализумаба (моноклональное антитело против 4-интегрина, относящегося к семейству молекул адгезии; применяется главным образом при лечении РС и болезни Крона)21-23. Другие моноклональные антитела, с применением которых связывают развитие ПМЛ – эфализумаб24 (моноклональное антитело к CD11a, применяется главным образом при лечении псориаза) и ритуксимаб25 (моноклональное антитело к CD20, применяется при лечении различных заболеваний). Описано 57 случаев ПМЛ у пациентов, получавших ритуксимаб при гемобластозах (главным образом при неходжкинских лимфомах (n = 50), ревматоидном артрите (n = 1), СКВ (n = 2) и аутоиммунных гематологических заболеваниях (n =4))26,27.
ПМЛ при идиопатическом иммунодефиците ПМЛ описана также у пациентов с первичным иммунодефицитом - чаще всего с идиопатической CD4-лимфоцитопенией28-30, а также с вариабельным неклассифицируемым иммунодефицитом31,32.
ПМЛ при минимальных нарушениях иммунитета или в их отсутствие До недавнего времени считалось, что ПМЛ не может развиться в отсутствие тяжелого угнетения клеточного иммунитета. Однако сейчас описаны случаи ПМЛ на фоне менее выраженного иммунодефицита, например, при циррозе печени, ХПН, псориазе, дерматомиозите и даже при беременности6. Кроме того, неоднократно описаны случаи ПМЛ в отсутствие какого-либо иммунодефицита. Крайне важно, чтобы нейрорентгенологи знали о подобных изменениях в эпидемиологии ПМЛ, JC-Э, JC-М и JC-НЗК. JC-Э и JC-НЗК на сегодняшний день описаны только на фоне ВИЧ-инфекции и СПИДа. Интересно отметить, что все случаи JC-М наблюдались в отсутствие ВИЧ-инфекции, в том числе на фоне СКВ и даже при нормальном иммунитете (подробнее описано в разделе «Патогенез»).
Патогенез Вирус JC - ДНК-содержащий двухцепочечный кольцевой вирус, принадлежащий к семейству полиомавирусов. Это небольшой вирус, обладающий икосаэдральной симметрией.
Капсид вируса содержит три вирусных белка: VP1, VP2, and VP3, из них преобладающим является VP1, который может образовывать вирусоподобные частицы, вызывающие иммунный ответ организма33,34.
Патогенез ПМЛ имеет три стадии. Первая - первичная бессимптомная инфекция. Вторая - стойкая латентная вирусная инфекция мочеполовой системы, костного мозга и, возможно, селезенки35.Наличие вируса в костном мозге и его выделение с мочой часто наблюдается при бессимптомном носительстве у людей с нормальным иммунитетом36,37. Есть также предположения, что вирус может персистировать в ЦНС. Третья, последняя стадия инфекции - реактивация вируса и его распространение в организме с предположительно гематогенным путем попадания в ЦНС35. Как именно это происходит и когда, точно не установлено, но гематогенный путь наиболее вероятен; это может происходить на стадии первичной инфекции, на стадии персистенции в периферических тканях, либо при реактивации вируса, на фоне нарушенного клеточного иммунитета38.
На стадии носительства участок вирусной ДНК между ранними и поздними вирусными генами содержит стабильную регуляторную последовательность. При снижении клеточного иммунитета происходит перестройка этой последовательности, приводящая к реактивации вируса, что вызывает инфекцию олигодендроцитов с последующим их лизисом39. Риск ПМЛ особенно высок при сниженном или подавленном клеточном иммунитете (в отличие от случаев, когда нарушен гуморальный иммунитет). Эффекторами клеточного иммунитета являются T-лимфоциты CD8 (иначе цитотоксические T-лимфоциты). Они уничтожают инфицированные вирусами клетки, если узнают должным образом процессированные вирусные эпитопы (вирусные белки или их части, которые распознаются иммунной системой организма). Наличие в крови или СМЖ цитотоксических T-лимфоцитов, специфичных в отношении вируса JC, снижает риск развития заболевания и улучшает прогноз. Таким образом, цитотоксические T-лимфоциты играют ключевую роль в иммунном ответе против вируса40. Четкая связь заболевания с ВИЧ-инфекцией и случаи ПМЛ в отсутствие ВИЧ, на фоне идиопатической CD4-лимфоцитопении, указывают на то, что Tлимфоциты CD4 также играют важную роль в борьбе с инфекцией, вызванной вирусом JC41.
Гуморальный же иммунитет от инфекции вирусом не защищает.
Насколько важна сохранность иммунитета, видно из того, что ПМЛ часто развивается при иммунодефицитах различной этиологии, а также из случаев ее ремиссии с началом ВААРТ42,43. Ремиссия заболевания часто совпадает с ростом числа лимфоцитов CD4 и цитотоксических T-лимфоцитов в крови и СМЖ44–46.
Клинические синдромы при инфекции ЦНС, вызванной вирусом JC До недавнего времени ПМЛ была единственным известным проявлением инфекции ЦНС, вызванной вирусом JC, с неспецифической клинической картиной, но характерными гистологическими признаками и данными лучевой диагностики.
При восстановлении иммунитета под действием ВААРТ у некоторых пациентов возможны резкие изменения в клинической картине, гистологии и данных лучевой диагностики. Эти изменения имеют очень важное клиническое значение, и их следует дифференцировать от классической картины ПМЛ. Кроме того, недавно описаны три новых проявления инфекции. Для более четкого представления все синдромы, связанные с инфекцией вирусом JC, представлены ниже (таблица 1).
кПМЛ Симптомы ПМЛ неспецифичны. Примерно у 25% пациентов ПМЛ становится первым диагностическим критерием СПИДа47. При кПМЛ первыми появляются очаговые неврологические симптомы, характер которых зависит от локализации очагов инфекции.
Чаще всего наблюдаются гемипарезы или гемипарестезии. При поражении затылочных долей головного мозга или зрительной лучистости возможны нарушения зрения; при поражении теменной доли доминантного полушария - нарушения речи; при поражении мозжечка - атаксия или дисметрия и т. п.35. Первоначальные симптомы постепенно нарастают, в зависимости от того, какие области мозга поражаются следующими. Примерно у 20% пациентов со временем развиваются эпилептические припадки48. Возможны также нарушения когнитивной функции. В некоторых случаях на основании одной только клинической картины трудно отличить ПМЛ от ВИЧ-энцефалопатии.
С гистологической точки зрения основным признаком является демиелинизация.
Первоначальные очаги демиелинизации увеличиваются и сливаются. В далеко зашедших случаях возможен некроз с образованием полостей38. Характерный гистологический признак - инфекция олигодендроцитов с их последующим лизисом; олигодендроциты набухшие, с увеличенными базофильными ядрами, содержащими эозинофильные включения, дают положительную реакцию при иммуногистохимическом окрашивании на белки и ДНК вируса JC38. Инфицированные олигодендроциты выявляются в основном растущему краю очага49. При набухании олигодендроцитов межклеточное пространство сокращается, чем объясняются ограничения диффузии по краям очагов при диффузионновзвешенной МРТ. Вирус JC поражает также астроциты, которые тоже резко увеличиваются в размере и имеют большое количество набухших отростков. В таких увеличенных астроцитах выявляются вирусные белки и/или гены. Иногда они содержат многодольчатые гиперхромные ядра, напоминая опухолевые клетки; патологи называют такие клетки «причудливыми астроцитами»50. Еще одна характерная гистологическая черта ПМЛ - очень слабо выраженное воспаление или его отсутствие50. В очень редких случаях наблюдаются кровоизлияния в очагах поражения51.
вПМЛ Как уже было сказано выше, кПМЛ характеризуется отсутствием воспалительных изменений в ткани головного мозга. В редких случаях реактивация вируса и развитие ПМЛ сопровождаются выраженной воспалительной реакцией. Характерна диффузная или очаговая периваскулярная лимфоцитарная инфильтрация, главным образом Tлимфоцитами CD3, моноцитами или макрофагами, B-лимфоцитами, T-лимфоцитами CD4 и плазматическими клетками52–54. Рентгенологически очаги воспаления характеризуются накоплением контраста и/или смещением структур мозга с вазогенным отеком.
Обычно вПМЛ развивается в двух случаях. Чаще всего она наблюдается на фоне ВСВИ у ВИЧ-инфицированных после ВААРТ (см. раздел «ВСВИ и НВСВИ»). Как можно ожидать, при вПМЛ на фоне ВСВИ неврологические симптомы ПМЛ обычно выражены сильнее. В редких случаях вПМЛ встречается у ВИЧ-инфицированных в отсутствие ВААРТ, а также в отсутствие ВИЧ-инфекции52. При в ПМЛ в отсутствие ВИЧ-инфекции прогноз хуже52.
– – –
JC-НЗК Задняя черепная ямка часто поражается как при кПМЛ, так и при вПМЛ. Очаги инфекции обычно затрагивают средние ножки мозжечка и мост, либо полушария мозжечка. Еще одно проявление инфекции вирусом JC, затрагивающее мозжечок - JC-НЗК55, при котором поражаются только зернистые клетки мозжечка, но не олигодендроциты. Поэтому классической картины ПМЛ, с изменениями олигодендроцитов и астроцитов, в данном случае нет. Характерны изолированные мозжечковые симптомы, в т. ч. атаксия и дизартрия.
Полагают, что такая тропность вируса к зернистым клеткам мозжечка связана с уникальной мутацией гена VP1 вируса56.
JC-М При симптомах вирусного менингита анализ СМЖ на наличие ДНК или антигенов вируса JC обычно не проводят. Blake et al57 в 1992 г. впервые описали инфекцию вирусом JC, сопровождавшуюся менингоэнцефалитом, у девочки с нормальным иммунитетом. В поддержку их гипотезы свидетельствовал увеличенный титр IgG и IgM антител к вирусу. В крупном исследовании58 ДНК вируса выявили в СМЖ у 2 из 89 пациентов (19 с ВИЧинфекцией и 70 без нее) с подозрением на менингит58. Оба пациента, у которых была найдена вирусная ДНК, не имели ВИЧ-инфекции. Авторы делают вывод, что при обследовании пациентов с менингитом или энцефалитом необходим анализ на наличие вирусов BK и JC. Viallard et al59 описали пациента, длительно страдающего СКВ, с острым менингитом и отсутствием энцефалита или ПМЛ в анамнезе. При всестороннем обследовании единственным обнаруженным в СМЖ патогеном оказался вирус JC. Авторы заключают, что если у больного СКВ подозревается инфекция ЦНС, дифференциальный диагноз должен включать инфекцию вирусом JC. Нужно немедленно провести анализ СМЖ на наличие вируса посредством ПЦР, чтобы своевременно начать антивирусную терапию.
JC-Э JC-Э60 - недавно описанная форма инфекции ЦНС вирусом JC с проявлениями энцефалита.
Wuthrich et al60 описали пациента с нарушениями высшей нервной деятельности, но без очаговых неврологических нарушений. При гистологическом исследовании было обнаружено преимущественное поражение пирамидных клеток и астроцитов в сером веществе и на границе между серым и белым веществом, с очагами некроза. Авторы выявили обширное поражение пирамидных клеток и, используя двойное иммуногистохимическое окрашивание, показали наличие белков вируса JC в их ядрах, аксонах и дендритах. Хотя на поздней стадии, по данным МРТ, поражается белое вещество, поражение олигодендроцитов было незначительным, и «типичной» для ПМЛ демиелинизации не найдено.
ВСВИ и НВСВИ ВСВИ - парадоксальное ухудшение клинической картины у ВИЧ-инфицированных, получающих ВААРТ. Диагностика часто затруднена, возможности лечения ограничены;
прогноз может быть различным61. Диагноз ВСВИ обоснован при наличии следующих критериев62: ВИЧ-инфицированный на ВААРТ, со снижением уровня РНК ВИЧ-1 и увеличением количества лимфоцитов CD4 от исходных показателей, с симптомами, указывающими на воспаление, а не на ранее или вновь выявленную оппортунистическую инфекцию либо побочное действие препаратов. Когда речь идет о поражении ЦНС, иногда используется термин НВСВИ.
Риск ВСВИ особенно высок у тех, кто впервые получает антиретровирусные препараты63,64.
Среди других факторов риска - длительность и тяжесть иммунодефицита, полиморфизм в генах цитокинов65, высокая вирусная нагрузка перед началом лечения и скорость восстановления иммунитета66. При сравнении различных схем ВААРТ различий в риске ВСВИ не выявлено63. Однако начало ВААРТ вскоре после выявления оппортунистической инфекции может быть прогностическим фактором ВСВИ67.
ВСВИ может развиться на любой из двух стадий восстановления иммунитета после начала ВААРТ68. Первый период наибольшего риска приходится на начальные недели терапии, когда рост числа T-лимфоцитов CD4 в значительной мере обусловлен перераспределением сохранившихся клеток памяти. Вторая фаза восстановления иммунитета характеризуется пролиферацией девственных T-лимфоцитов, обычно 4 – 6 нед спустя, но ВСВИ может развиться и через 4 года после начала ВААРТ69.
Восстановление специфического иммунного ответа под действием ВААРТ способствует распознанию антигенов вируса JC как при уже имеющейся ПМЛ (третья стадия заболевания), так и при персистирующей инфекции (вторая стадия)70. Хотя гистологические критерии еще не разработаны, при ВСВИ часты воспалительные инфильтраты, состоящие из T-лимфоцитов CD8. Вне ЦНС ВСВИ чаще всего вызывается микобактериальными инфекциями71,72, но что касается ЦНС, наиболее частый патоген – вирус JC. Реже выявляются криптококки73,74, вирус простого герпеса и цитомегаловирус68. В редких случаях причиной ВСВИ могут стать аутоиммунные заболевания или новообразования 73.
ПМЛ, связанная с ВСВИ, наблюдается у 18% ВИЧ-инфицированных с ПМЛ75. Как уже говорилось, ПМЛ и ВСВИ с началом ВААРТ могут развиться независимо друг от друга, или же у пациентов с ранее выявленной ПМЛ возможно ухудшение неврологических симптомов вследствие развития ВСВИ после начала ВААРТ76. Хотя демографических различий между этими двумя группами пациентов нет, у второй группы ВСВИ развивается быстрее – вероятно, вследствие более обширной площади очагов поражения77. Большинство случаев ПМЛ, связанной с ВСВИ, характеризуется умеренными симптомами и незначительными признаками воспаления ЦНС.
Типичные гистопатологические признаки ПМЛ, связанной с ВСВИ – гиперплазия серого и белого вещества с глиозом, астроциты с атипичными гиперхромными ядрами, наличие макрофагов, умеренное периваскулярное воспаление, что объясняет накопление контраста при МРТ с контрастированием (в отличие от кПМЛ). Накопление контраста может считаться косвенным маркером ПМЛ, связанной с ВСВИ, однако наблюдается лишь у 56% пациентов77. Следовательно, отсутствие накопления контраста в очагах, характерных для ПМЛ, не может быть основанием для исключения диагноза. К сожалению, на сегодняшний день биохимические маркеры, позволяющие подтвердить развитие ВСВИ, не разработаны.
Таблица 2. Диагностические критерии ПМЛ Диагноз Типичная Типичная ДНК Типичная гистологическая клиническая картина при вируса в картина с наличием вирусной картина лучевой СМЖ ДНК или белков диагностике Подтвержденная + + + ПМЛ Подтвержденная + + - + ПМЛ Предполагаемая + + - ПМЛ Примечание.
+ – присутствует; - – отсутствует.
Как ни парадоксально, ПМЛ, связанную с ВСВИ, лечат назначением глюкокортикоидных препаратов и кратким перерывом в антиретровирусной терапии. При должном лечении глюкокортикоидами исход обычно благоприятный77.
Диагностика Ранняя диагностика ПМЛ и других инфекций ЦНС, вызванных вирусом JC, крайне важна вследствие недавнего расширения группы риска. Несмотря на наличие высокочувствительных тестов для выявления вирусной ДНК и специфичность картины при МРТ, для подтверждения диагноза требуется биопсия головного мозга с гистологическим исследованием. Классические гистологические изменения при кПМЛ и вПМЛ описаны выше. Чувствительность и специфичность биопсии составляет 64–96% и 100%78, соответственно; побочные эффекты наблюдаются в 2,9% случаев, осложнения развиваются в 8,4% случаев79.
Если биопсию провести невозможно (например, у ослабленных пациентов, если пациент не дает согласия, при труднодоступных очагах поражения), диагноз ПМЛ ставится по результатам МРТ головного мозга или при выявлении вирусной ДНК в СМЖ посредством ПЦР.
До внедрения ВААРТ ПЦР была очень чувствительным и специфичным методом диагностики ПМЛ (чувствительность 72–92%, специфичность 92–100%)80. Однако в последнее время достаточно часты отрицательные результаты ПЦР у пациентов со СПИДом при характерных для ПМЛ симптомах и данных МРТ. Возможно, восстановление иммунитета при антиретровирусной терапии приводит к подавлению репликации вируса и снижению концентрации вирусной ДНК в СМЖ42. В результате чувствительность выявления ДНК вируса JC с помощью ПЦР упала до 58%81,82.
С появлением ВААРТ очень важной составляющей диагностики ПМЛ стала лучевая диагностика. Собственно говоря, по новейшим диагностическим критериям, классификация ПМЛ как «подтвержденной» базируется на клинической картине и данных МРТ в сочетании с положительными результатами либо биопсии головного мозга, либо ПЦР (таблица 2)38.
При симптомах и данных МРТ, согласующихся с ПМЛ, и либо наличии вирусной ДНК в СМЖ, либо типичной гистологической картине и наличии вирусной ДНК или белков по данным иммуногистохимического окрашивания ставится диагноз «подтвержденной ПМЛ»
(таблица 2). При типичных симптомах и данных МРТ, но в отсутствие данных о наличии вируса (биопсия или люмбальная пункция не проводились, либо вирусная ДНК в СМЖ не выявлена) ставят диагноз «предполагаемой ПМЛ».
Диагноз JC-НЗК и JC-Э подтверждают путем выявления вирусной ДНК или белков в инфицированных нейронах при двойном иммуногистохимическом окрашивании.
Лучевая диагностика Лучевая диагностика играет ключевую роль в диагностике инфекции вирусом JC и в последующем наблюдении за пациентом. И врачи, и пациенты часто не хотят прибегать к такой инвазивной процедуре, как биопсия головного мозга. Кроме того, ВААРТ снижает диагностическую чувствительность ПЦР СМЖ. Учитывая, что продолжительность жизни у таких пациентов при лечении увеличивается, разбираться в данных лучевой диагностики очень важно.
кПМЛ В конце 1980-х гг. было опубликовано несколько статей, посвященных применению КТ и МРТ при ПМЛ у отдельных пациентов или небольших групп83–86. На КТ обычно выявлялись очаги пониженной плотности в белом веществе (иногда множественные), без смещения структур мозга. Поражения задней черепной ямки с помощью КТ оценить сложно из-за наложения костных структур.
МРТ МРТ является методом выбора при диагностике ПМЛ87. Результаты стандартных методик МРТ изложены в соответствии с распределением и характеристикой очагов поражения.
Распределение очагов поражения Whiteman et al49 в 1993 г. впервые дали систематическое описание картины, наблюдаемой при КТ или МРТ головного мозга у больных ПМЛ, с корреляцией между клиническими и патологическими признаками. Как правило, ПМЛ характеризуется сливным, двусторонним, но при этом асимметричным, супратенториальным поражением белого вещества. Однако поражение может быть односторонним, и может выявляться только один очаг49,88.
Поражения ЦНС можно классифицировать следующим образом.
Поражения белого вещества Супратенториальные. Поскольку вирус JC обладает тропностью к олигодендроцитам, поражаться может любая область мозга. Чаще всего встречается асимметричное многоочаговое двустороннее сливное супратенториальное поражение белого вещества49,88.
Однако может обнаруживаться единственный очаг поражения, расположенный в подкорковых ассоциативных волокнах89,90; в таких случаях ПМЛ иногда ошибочно принимают за инсульт91. Чаще всего поражается теменная доля, затем лобная.
Супратенториальные очаги поражения, как правило, захватывают подкорковое белое вещество и имеют неровные края92. Могут поражаться также семиовальный центр и перивентрикулярное белое вещество. Сообщалось, что поражение белого вещества начинается в подкорковом слое, где наиболее кровоток интенсивен, а затем распространяется в более глубокие отделы семиовального центра и перивентрикулярных областей93. Реже поражаются внутренняя капсула, наружная капсула и мозолистое тело. На рисунке 1 приведена типичная картина кПМЛ при супратенториальном поражении.
Инфратенториальные. Следующим по частоте поражается белое вещество затылочной ямки49,88, как правило, средняя ножка мозжечка и прилегающие области варолиева моста и мозжечка. Во внутреннем клиническом разборе, проводившемся в нашей клинике, у всех 9 пациентов с поражением затылочной ямки была затронута преимущественно средняя ножка мозжечка вместе с прилегающими областями мозжечка и варолиева моста. Очаги поражения в варолиевом мосту могут распространяться на средний и/или продолговатый мозг. Изолированные поражения белого вещества мозжечка или изолированные поражения продолговатого мозга встречаются реже. На рисунке 2 приведена типичная картина кПМЛ при инфратенториальном поражении.
Спинной мозг. Спинной мозг при ПМЛ поражается крайне редко. Известны лишь отдельные протоколы вскрытия, в которых описаны такие поражения94,95.
Рисунок 1. Типичная картина супратенториального поражения правой лобной доли при кПМЛ у ВИЧ-инфицированного.
A. При проведении диффузионно-взвешенной МРТ видно типичное снижение диффузии вдоль растущего края очага кзади (показано стрелками) и отсутствие снижения диффузии в центре. B. На карте ИКД значения ИКД низки у заднего растущего края очага (показано стрелкой) и высоки в центре очага. C. Очаг поражения обычно затрагивает подкорковые ассоциативные волокна, и (в сравнении с серым веществом) интенсивность сигнала на T1-взвешенном изображении снижена. Обратите внимание, что смещения структур мозга нет (очаг среднего размера). D. На T1-взвешенном изображении после введения контраста накопления контраста нет. E. На FLAIR-изображении интенсивность сигнала в большей части очага повышена. Обратите внимание на снижение интенсивности сигнала в передней части очага (показано стрелкой) вследствие образования внутри кисты. F. На T2-взвешенном изображении вся пораженная область характеризуется увеличенной интенсивностью сигнала. Обратите внимание, что передняя поверхность коры рядом с очагом (показано стрелкой) затронута сравнительно мало. G. Оценка перфузии.
Кровенаполнение в области очага ниже (показано стрелкой), чем в белом веществе с противоположной стороны.
Как и в случае головного мозга, поражение обычно ограничено белым веществом. У Takeda S. et al94 описано поражение передних и задних столбов всех 26 сегментов спинного мозга на фоне лимфоцитопении. На сегодня, насколько нам известно, нет работ, где приводились бы результаты МРТ при ПМЛ спинного мозга.
Поражения серого вещества При ПМЛ может поражаться и серое вещество. Чаще всего страдает таламус, второе место занимают базальные ядра49,88. Поражение серого вещества почти всегда сопутствует поражению белого вещества. В очень редких случаях очаги поражения при ПМЛ могут захватывать только серое вещество96,97.
Локализация очагов Супратенториальные поражения, как правило, ограничены подкорковыми ассоциативными волокнами и окружены здоровой тканью коры мозга93. Такая локализация очагов поражения считается характерным признаком ПМЛ и используется, чтобы отличить ее от ВИЧэнцефалопатии и других поражений белого вещества93. В отличие от других поражений белого вещества, при ПМЛ обычно не затрагиваются перивентрикулярные области или глубокие слои белого вещества. Однако они могут вовлекаться в патологический процесс по мере прогрессирования заболевания.
Инфратенториальные поражения обычно локализуются в средней ножке мозжечка, часто захватывая прилегающие области варолиева моста и/или мозжечка. На поздних стадиях патологический процесс может распространиться на средний и продолговатый мозг.
– – –
Данные МРТ при ПМЛ у больных РС Выше уже кратко упоминалось, что ПМЛ может развиться на фоне РС при терапии натализумабом. У таких больных отличить недавно появившийся очаг ПМЛ от очага демиелинизации, характерного для РС, крайне трудно. Рекомендации по МРТ-диагностике очагов ПМЛ у больных РС были предложены Yousry et al99.
Согласно им, диагноз ПМЛ считается подтвержденным, если соблюдаются три нижеследующих критерия:
1) Есть ухудшение клинической картины.
2) Типичная картина при МРТ.
3) В СМЖ обнаружена ДНК вируса JC.
Признаки, указывающие скорее на ПМЛ, чем на РС (согласно Yousry et al99):
1) Диффузное поражение подкоркового белого вещества, а не перивентрикулярных отделов;
часто поражается задняя черепная ямка.
2) Неправильной формы нечеткий край очага, ограниченный белым веществом.
3) Постоянный рост очага, ограниченного белым веществом.
4) Даже в крупных очагах нет смещения структур мозга.
5) Диффузное увеличение интенсивности сигнала на T2-взвешенных изображениях; в недавно вовлеченных в патологический процесс областях интенсивность сигнала выше.
6) На T1-взвешенных изображениях интенсивность сигнала вначале нормальная или сниженная, со временем уменьшается; интенсивность сигнала никогда не возвращается к норме.
7) Накопления контраста, как правило, нет даже в крупных очагах.
Атипичные случаи В редких случаях очаги поражения могут распространяться из одной доли в другую через мозолистое тело, имитируя лимфому или глиобластому88,100.
Диффузионно-взвешенная томография При диффузионно-взвешенной МРТ картина ПМЛ зависит от стадии заболевания101. Новые, активно растущие очаги имеют ободок понижения диффузии по растущему краю и отсутствие снижения диффузии в центре очага (рисунки 1A, B)101,102. Обычно ободок незамкнут и указывает на активный инфекционный процесс38. Гистологически у этого края очага обнаруживаются укрупненные разбухшие олигодендроциты, увеличенные «причудливые астроциты» с многочисленными увеличенными отростками, и инфильтрация макрофагами с пенистой цитоплазмой38,49,101. Увеличение размера клеток ведет к сокращению межклеточного пространства, где максимально броуновское движение молекул воды. Снижение диффузии по краю очага может быть обусловлено сокращением межклеточного пространства103 – 105 или же просто увеличенным размером клеток вследствие удержания воды во внутриклеточном пространстве106. В старых «зарубцевавшихся» очагах, после лечения или в центральной части крупного очага, свобода диффузии повышена вследствие нарушений клеточной архитектоники, увеличения межклеточного пространства в результате гибели олигодендроцитов, деятельности макрофагов, репаративных процессов, стимулируемых астроцитами101,107.
Важную роль при диагностике ПМЛ играет также диффузионно-тензорная томография.
Фракционная анизотропия, отражающая упорядоченность структуры белого вещества, при ПМЛ снижается, что указывает на нарушения этой упорядоченности. Фракционная анизотропия может снижаться уже на ранних стадиях заболевания, когда при обычной и диффузионно-взвешенной МРТ еще никаких изменений не выявляется107. Диффузионнотензорная томография выявила также нарушения клеточной структуры в центральной части крупного сливного очага поражения108.
Метод с использованием переноса намагниченности Dousset et al109,110 отметили, что вследствие выраженной демиелинизации КПН в очагах ПМЛ очень низок (22%) по сравнению с КПН белого вещества у здоровых добровольцев (47%).
При ПМЛ высота пика НАА по сравнению с высотой пика на противоположной стороне намного ниже, как в абсолютном выражении, так и относительно высоты пика Кр120. Это может отражать гибель нейронов в очагах ПМЛ113. Высота холинового пика увеличена, что, возможно, отражает разрушение миелина113,120. Высота пика мио-инозитола может оставаться нормальной или значительно вырасти по сравнению с высотой пика на противоположной стороне. Уровень мио-инозитола зависит от стадии заболевания. На ранней стадии, в период активного роста очага он повышен, а на поздних стадиях постепенно снижается до нормы120. Увеличение соотношения мио-инозитол/Кр, которое указывает на местную изолированную пролиферацию клеток глии, вызванную воспалением, недавно предложено в качестве прогностического маркера ПМЛ. При активных очагах поражения значительно повышенное соотношение мио-инозитол/Кр коррелирует с увеличением продолжительности жизни, вероятно, вследствие более выраженного воспаления, что замедляет прогрессирование ПМЛ115.
Можно предположить, что высота пика мио-инозитола может расти также при ПМЛ-ВСВИ, поскольку при этом наблюдается сильное воспаление. На сегодня, насколько нам известно, работ, посвященных картине магнитно-резонансной спектроскопии при ПМЛ-ВСВИ, нет.
Оценка перфузии При гистологическом исследовании очаги ПМЛ не васкуляризованы. Мы проводили оценку перфузии только у двух пациентов с кПМЛ. Как и ожидалось, в обоих случаях кровенаполнение в области очагов поражения было меньше, в сравнении с нормальным белым веществом мозга с противоположной стороны (рисунок 1).
Ангиография При ангиографии очаги ПМЛ по большей части не выявляются из-за слабого воспаления или его отсутствия. Однако Nelson et al121 описали затеки контрастного вещества и наличие артериовенозных шунтов у 4 из 6 своих пациентов; гистологические исследования показали, что это обусловлено повышенной плотностью капилляров и «стойкими воспалительными изменениями». Авторы сделали вывод, что повышенная плотность мелких сосудов – следствие ангиогенеза, а не ускоренного прохождения контраста из-за изменения тонуса капилляров под воздействием воспалительных кининов. Однако последний механизм представляется более вероятным объяснением этих нарушений, поскольку у всех 4 пациентов на поперечных изображениях выявлены признаки вПМЛ (т. е. либо смещение структур мозга, либо накопление контраста).
Сцинтиграфия Поскольку в очагах поражения при кПМЛ нет воспаления, и они не являются новообразованиями, при сцинтиграфии они не выявляются. Iranzo et al122 не обнаружили захвата изотопов у 6 пациентов с характерной для ПМЛ картиной по МРТ. В исследовании Lee et al123 у 1 из 3 пациентов с ПМЛ не обнаружено захвата изотопа при сцинтиграфии с таллием-201 и галлием-67. Однако у двух других пациентов наблюдался захват обоих изотопов. Хотя результаты МРТ и гистологического исследования этих двух пациентов в статье не упомянуты, вероятно, у них была вПМЛ. У Port et al124 описан случай ПМЛ, при котором наблюдались захват таллия-201, накопление контраста на МРТ и множественные инфильтраты, состоящие из макрофагов, при гистологическом исследовании. Хотя термин «вПМЛ» в то время еще не был введен, авторы сделали вывод, что захват таллия-201 в данном случае обусловлен «воспалительной реакцией».
Теоретически во всех случаях кПМЛ результаты сцинтиграфии должны быть отрицательными, а во всех случаях вПМЛ – положительными. Чтобы доказать это предположение, необходимы систематические исследования.
Признаки прогрессирования заболевания Увеличение размера очагов ПМЛ и их слияние друг с другом, усиление атрофии коркового вещества и постепенное снижение интенсивности сигнала на T1-взвешенных изображениях говорят о прогрессировании заболевания и указывают на плохой прогноз88. На рисунке 6 можно видеть типичное прогрессирование заболевания даже несмотря на ВААРТ. На поздней стадии наблюдаются диффузная корковая атрофия и поражение белого вещества (рисунок 7). Дополнительным фактором может служить присоединение ВИЧэнцефалопатии.
Можно ли с помощью МРТ следить за ходом лечения?
Согласно Thurnher et al92, по интенсивности сигнала на FLAIR-изображениях можно отличить тех, у кого лечение дает результат, от тех, у кого оно неэффективно; снижение интенсивности сигнала на T1-взвешенных и FLAIR-изображениях со временем указывает на лейкомаляцию и сопутствующую атрофию в старых очагах ПМЛ (рисунок 6, нижний ряд). С другой стороны, повышение интенсивности сигнала на FLAIR-изображениях и снижение интенсивности сигнала на T1-взвешенных изображениях указывает на прогрессирование заболевания и является плохим прогностическим признаком109. В одном случае (Usiskin et al108) описано восстановление анизотропии белого вещества в ходе ВААРТ при доказанной ПМЛ (показано при диффузионно-взвешенной МРТ с высоким фактором диффузии b).
Может ли МРТ использоваться для прогнозирования исхода?
В крупной серии клинических наблюдений, посвященной гистологически доказанным случаям ПМЛ, Post et al88 не нашли корреляции между размерами очагов, их локализацией, интенсивностью сигнала, степенью атрофии мозгового вещества или наличием гидроцефалии, и выживаемостью. Однако наблюдалась выраженная корреляция между риском смерти и наличием смещения структур мозга при первом МРТ. Кроме того, риск смерти был вдвое выше, если в патологический процесс было вовлечено серое вещество базальных ядер. В данном исследовании продолжительность жизни была больше у пациентов с множественными дискретными очагами, по сравнению с теми, у кого имелись крупные сливные очаги поражения. В исследовании, где сравнивались пациенты с короткой и более длительной продолжительностью жизни, Thurnher et al92 отметили, что более обширное поражение мозга было связано с большей продолжительностью жизни.
Благоприятным прогностическим признаком является также повышенное соотношение миоинозитол/Кр115.
вПМЛ Картина вПМЛ на МРТ практически не отличается от картины кПМЛ, за исключением накопления контраста на периферии очага и/или смещения структур мозга, обусловленных воспалением. В редких случаях накопление контраста настолько незначительно, что на обычном T1-взвешенном изображении в последовательности «спиновое эхо» не выявляется, и его можно заметить лишь при использовании метода с использованием переноса намагниченности. Из-за воспалительного инфильтрата такие очаги могут активно захватывать изотопы при сцинтиграфии.
JC-НЗК Для JC-НЗК55 характерно изолированное поражение внутреннего слоя зернистых клеток мозжечка без вовлечения в патологический процесс белого вещества. На ранней стадии заболевания специфические признаки на МРТ отсутствуют. На более поздних стадиях наблюдается изолированная атрофия мозжечка с повышенной интенсивностью сигнала на T2-взвешенных изображениях.
JC-М Специфические признаки на МРТ отсутствуют.
JC-Э В отличие от ПМЛ очаги поражения при JC-Э первоначально выявляются только в сером веществе полушарий; по мере прогрессирования заболевания в процесс вовлекается подкорковое белое вещество. Как и при кПМЛ, накопления контраста в очагах нет58.
Лечение Специфического лечения при инфекции вирусом JC не существует. Для ВИЧинфицированных наилучшим методом является оптимизация ВААРТ. ВААРТ в 50–60% случаев может привести к стабилизации клинической картины и картины по МРТ38. В отсутствие ВИЧ-инфекции методом выбора является устранение, насколько это возможно, причины иммунодефицита (прием глюкокортикоидов, ингибиторов кальциневрина у реципиентов после трансплантации, натализумаба и т. п.)125. В различных клинических исследованиях изучена эффективность ряда препаратов – например, цитарабина, цидофовира и топотекана – в отношении вируса JC. Все они либо были неэффективны, либо наряду с некоторой эффективностью демонстрировали высокую токсичность 38. В случаях ПМЛВСВИ при ухудшении состояния, вызванном воспалением, назначают глюкокортикоиды 38.
Трансфер на борт судна. Суббота Балтра После обеда – Китайская Шляпа. Остров Сомбреро Чино образован из вулканической породы и имеет форму китайской шляпы, в честь которой он и назв...» СЕРВИСА» Лист 1 из 57 ...» Документация пользователя Санкт-Петербург, 2011 г. www.dyn.ru СОДЕРЖАНИЕ 1. ВВЕДЕНИЕ 1.1. Общие сведения 1.2. Области применения 1.3. Возможности системы 1.4. Особенности сист...»
2017 www.сайт - «Бесплатная электронная библиотека - разные матриалы»
Материалы этого сайта размещены для ознакомления, все права принадлежат их авторам.
Если Вы не согласны с тем, что Ваш материал размещён на этом сайте, пожалуйста, напишите нам , мы в течении 1-2 рабочих дней удалим его.
Лейкоэнцефалопатия головного мозга — эта патология, при которой наблюдается поражение белого вещества, вызывающее слабоумие. Выделяют несколько нозологических форм, вызываемых различными причинами. Общим для них является наличие лейкоэнцефалопатии.
Спровоцировать заболевание могут:
- вирусы;
- сосудистые патологии;
- недостаточное снабжение головного мозга кислородом.
Другие названия заболевания: энцефалопатия, болезнь Бинсвангера. Впервые патология была описана в конце XIX веке немецким психиатром Отто Бинсвангером, который назвал ее в свою честь. Из этой статьи вы узнайте, что это такое, каковы причины болезни, как она проявляется, диагностируется и лечится.
Классификация
Различают несколько видов лейкоэнцефалопатии.
Мелкоочаговая
Это лейкоэнцефалопатия сосудистого генеза, которая представляет собой хроническую патологию, развивающуюся на фоне высокого давления. Другие названия: прогрессирующая сосудистая лейкоэнцефалопатия, субкортикальная атеросклеротическая энцефалопатия.

Одинаковые клинические проявления с мелкоочаговой лейкоэнцефалопатией имеет дисциркуляторная энцефалопатия — медленно прогрессирующее диффузное поражение сосудов головного мозга. Раньше эта болезнь была включена в МКБ-10, сейчас она в ней отсутствует.
Чаще всего мелкоочаговую лейкоэнцефалопатию диагностируют у мужчин старше 55 лет, у которых имеется генетическая предрасположенность к развитию этого заболевания.
В группу риска входят пациенты, страдающие такими патологиями, как:
- атеросклероз (холестериновые бляшки закупоривают просвет сосудов, в результате наблюдается нарушение кровоснабжения головного мозга);
- сахарный диабет (при этой патологии кровь сгущается, замедляется ее течение);
- врожденные и приобретенные патологии позвоночника, при которых наблюдается ухудшения кровоснабжения мозга;
- ожирение;
- алкоголизм;
- никотиновая зависимость.
Также к развитию патологии приводят погрешности в диете и гиподинамичный образ жизни.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Это самая опасная форма развития заболевания, которая нередко становится причиной летального исхода. Патология имеет вирусную природу.
Ее возбудителем является полиомавирус человека 2. Этот вирус наблюдается у 80% человеческой популяции, но заболевание развивается у пациентов с первичным и вторичным иммунодефицитом. У них вирусы, попадая в организм, еще сильнее ослабляют иммунную систему.
Прогрессирующая многоочаговая лейкоэнцефалопатия диагностируется у 5% ВИЧ-положительных пациентов и у половины больных СПИДом. Раньше прогрессирующая мультифокальная лейкоэнцефалопатия встречалось еще чаще, но благодаря ВААРТ распространенность этой формы снизилась. Клиническая картина патологии полиморфна .
Заболевание проявляется такими симптомами, как:

- периферические парезы и параличи;
- односторонняя гемианопсия;
- синдром оглушения сознания;
- дефект личности;
- поражение ЧМН;
- экстрапирамидные синдромы.
Нарушения со стороны ЦНС могут существенно варьировать от небольшой дисфункции до тяжелой степени слабоумия. Могут наблюдаться нарушения речи, полная потеря зрения. Зачастую у пациентов развиваются тяжелые нарушения со стороны опорно-двигательного аппарата, которые становятся причиной потери работоспособности и инвалидизации.
В группу риска входят следующие категории граждан:
- пациенты с ВИЧ и СПИДом;
- получающие лечение моноклональными антителами (их назначают при аутоиммунных заболеваниях, онкологических болезнях);
- перенесшие пересадку внутренних органов и принимающие иммунодепрессанты с целью предупредить их отторжение;
- страдающие злокачественной гранулемой.
Перивентрикулярная (очаговая) форма
Развивается в результате хронического кислородного голодания и нарушения кровоснабжения головного мозга. Ишемические участки расположены не только в белом, но и сером веществе.
Обычно патологические очаги локализованы в мозжечке, мозговом стволе и лобной части коры больших полушарий. Все эти структуры мозга отвечают за движение, поэтому при развитии такой формы патологии наблюдаются двигательные расстройства.
Это форма лейкоэнцефалопатии развивается у детей, у которых есть патологии, сопровождающиеся гипоксией при родоразрешении и в течение нескольких дней после появления на свет. Также данную патологию называют “перивентрикулярная лейкомаляция”, как правило, она провоцирует ДЦП.
Лейкоэнцефалопатия с исчезающим белым веществом
Она диагностируется у детей. Первые симптомы патологии наблюдаются у пациентов в возрасте от 2 до 6 лет. Появляется она из-за генной мутации.
У пациентов отмечается:

- нарушение координации движения связанное с поражением мозжечка;
- парез рук и ног;
- ухудшение памяти, снижение умственной работоспособности и другие когнитивные нарушения;
- атрофия зрительного нерва;
- эпилептические приступы.
У детей до года наблюдается проблемы со вскармливанием, рвота, высокая температура, психическое отставание, чрезмерная возбудимость, повышенный тонус мышц рук и ног, судороги, ночное апноэ, кома.
Клиническая картина
Обычно признаки лейкоэнцефалопатии нарастают постепенно. В начале болезни пациент может быть рассеянным, неловким, безразличным к происходящему. Он становится слезливым, с трудом произносит сложные слова, у него падает умственная работоспособность.
Со временем присоединяются проблемы со сном, повышается мышечный тонус, больной становится раздражительным, у него наблюдается непроизвольное движение глаз, появляется шум в ушах.
Если не начать лечить лейкоэнцефалопатию на этой стадии, но она прогрессирует: возникают психоневроз, выраженное слабоумие и судороги.
Главными симптомами заболевания являются следующие отклонения:
- двигательные расстройства, которые проявляются нарушением координации движения, слабостью в руках и ногах;
- может быть односторонний паралич рук или ног;
- речевые и зрительные расстройства (скотома, гемианопсия);
- онемение различных частей тела;
- нарушение глотания;
- недержание мочи;
- эпилептический приступ;
- ослабление интеллекта и небольшое слабоумие;
- тошнота;
- головные боли.
Все признаки поражения нервной системы прогрессируют очень быстро. У пациента может отмечаться ложный бульбарный паралич, а также паркинсонический синдром, который проявляется нарушением походки, письма, дрожанием тела.
Почти у каждого пациента наблюдается ослабление памяти и интеллекта, неустойчивость при изменении положения тела или ходьбе.
Обычно люди не понимают, что больны, и поэтому к доктору их зачастую приводят родственники.
Диагностика
Чтобы поставить диагноз «лейкоэнцефалопатия», врач назначит комплексное обследование. Нужны будут:

- осмотр невролога;
- общий анализ крови;
- анализ крови на содержания наркотических, психотропных средств и алкоголя;
- магнитно-резонансная и компьютерная томография, которые позволяют выявить патологические очаги в головном мозге;
- электроэнцефалография головного мозга, которая покажет снижение его активности;
- ультразвуковая допплерография, которая позволяет выявить нарушение циркуляции крови по сосудам;
- ПЦР, позволяющий выявить ДНК-возбудителя в головном мозге;
- биопсия головного мозга;
- спинномозговая пункция, которая показывает повышенную концентрацию белка в спинномозговой жидкости.
В случае если врач подозревает, что в основе лейкоэнцефалопатии лежит вирусная инфекция, он назначает пациенту электронную микроскопию, которая позволит выявить в тканях головного мозга частицы возбудителя.
С помощью иммуноцитохимиеского анализа удается обнаружить антигены микроорганизма. В спинномозговой жидкости при таком течении заболевания наблюдается лимфоцитарный плеоцитоз.
Также помогают в постановке диагноза тесты на психологическое состояние, память, координацию движения.
Дифференциальная диагностика проводится с такими заболеваниями, как:
- токсоплазмоз;
- криптококкоз;
- ВИЧ-деменция;
- лейкодистрофия;
- лимфома центральной нервной системы;
- подострый склерозирующий панэнцефалит;
- рассеянный склероз.
Терапия
Лейкоэнцефалопатия относится к неизлечимым заболеваниям. Но обязательно нужно обращаться в больницу для подбора медикаментозного лечения. Цель терапии — замедлить прогрессирование заболевания и активировать функции головного мозга.
Лечение лейкоэнцефалопатии — комплексное, симптоматическое и этиотропное. В каждом конкретном случае оно подбирается индивидуально .
Врач может прописать следующие медикаменты:

- лекарства, улучшающее мозговое кровообращение (Винпоцетин, Актовегин, Трентал);
- нейрометаболические стимуляторы (Фезам, Пантокальцин, Луцетам, Церебролизин);
- (Стугерон, Курантил, Зилт);
- поливитамины, в состав которых входят витамины группы В, ретинол и токоферол;
- адаптогены, такие как экстракт алоэ, стекловидное тело;
- глюкокортикостероиды, которые помогают купировать воспалительный процесс (Преднизолон, Дексаметазон);
- антидепрессанты (Флуоксетин);
- антикоагулянты, позволяющие снизить риск тромбозов (Гепарин, Варфарин);
- при вирусной природе заболевания назначаются Зовиракс, Циклоферон, Виферон.
Дополнительно показано:
.jpg)
- физиолечение;
- рефлексотерапия;
- аккупунктура;
- дыхательная гимнастика;
- гомеопатия;
- фитотерапия;
- массаж воротниковой зоны;
- мануальная терапия.
Трудность терапии заключается в том, что многие противовирусные и противовоспалительные препараты не проникают через ГЭБ, следовательно, не оказывают воздействия на патологические очаги.
Прогноз при лейкоэнцефалопатии
В настоящее время патология неизлечима и всегда заканчивается летальным исходом. Сколько живут с лейкоэнцефалопатией, зависит от того, была ли вовремя начата противовирусная терапия.
Когда лечение не проводится совсем, продолжительность жизни пациента не превышает полугода с момента выявления нарушения структур мозга.
При проведении антивирусной терапии продолжительность жизни увеличивается до 1-1,5 лет.
Были отмечены случаи острого течения патологии, которые заканчивались гибелью пациента через месяц после ее начала.
Профилактика
Специфической профилактики лейкоэнцефалопатии не существует.
Чтобы снизить риск развития патологии, нужно соблюдать следующие правила:
.jpg)
- укреплять свой иммунитет путем закаливания и приема витаминно-минеральных комплексов;
- нормализовать свой вес;
- вести активный образ жизни;
- регулярно бывать на свежем воздухе;
- отказаться от употребления наркотиков и алкоголя;
- бросит курить;
- избегать случайных половых контактов;
- при случайной интимной близости пользоваться презервативом;
- сбалансировано питаться, в рационе должны преобладать овощи и фрукты;
- научиться правильно справляться со стрессами;
- выделять достаточно времени для отдыха;
- избегать чрезмерных физических нагрузок;
- при выявлении сахарного диабета, атеросклероза, артериальной гипертензии принимать медикаменты, назначенные врачом с целью компенсации болезни.
Все эти меры позволят свести к минимуму риск развития лейкоэнцефалопатии. Если заболевание все-таки возникло, нужно как можно быстрее обратиться за медицинской помощью и начать лечение, которое поможет увеличить продолжительность жизни.