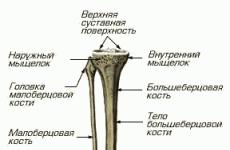
Форма туберкулеза, устойчивая к лекарственным препаратам. Международный студенческий научный вестник Туберкулез устойчивость
Федеральное государственное учреждение «Новосибирский научно-исследовательский институт туберкулеза Министерства здравоохранения и социального развития»
Тема «Лекарственная устойчивость МБТ»
Исполнитель:
Клинический ординатор 1-ого года обучения
Абасов Тарлан Мамед Рагим оглы
Новосибирск2010
Лекарственная резистентность МБТ……………………………………. 3
Механизм и динамика формирования лекарственной устойчивости… 4
Методы диагностики лекарственной устойчивости…………………… 8
Лечение…………………………………………………………………… 10
Профилактика развития лекарственной устойчивости……………….. 22
Список литературы……………………………………………………… 24
Лекарственная резистентность МБТ.
Появление множественной лекарственной устойчивости микобактерий туберкулеза стало серьезной угрозой эффективности противотуберкулезных программ во многих странах мира. В Российской Федерации распространение микобактерий, устойчивых к основным противотуберкулезным препаратам, является одной из главных проблем фтизиатрической службы. В 2007 г в Российской Федерацииу 13% больных с вновь выявленным туберкулезом до лечения была диагностирована множественная лекарственная устойчивость микобактерий. Приобретенная множественная лекарственная устойчивость в ряде регионов страны достигает 50-60% среди повторных случаев лечения туберкулеза. Излечение больных туберкулезом является главным компонентом национальной противотуберкулезной программы. Больной, который излечивается от туберкулеза, обрывает цепочку передачи инфекции. В тех случаях, когда пациенты не получают необходимого лечения и продолжают выделять микобактерий туберкулеза, происходит распространение инфекции в обществе в течение нескольких лет. У большинства больных туберкулезом можно достигнуть излечения, несмотря на наличие лекарственной устойчивости микобактерий туберкулеза (МБТ), сопутствующих заболеваний и развития побочных эффектов от приема лекарственных средств. Своевременно диагностированные больные с МБТ, чувствительными к основным противотуберкулезным препаратам, получают лечение в течение не менее 6 месяцев и практически всегда излечиваются от туберкулеза. Наиболее сложная ситуация возникает, когда у МБТ определяется устойчивость к основным противотуберкулезным препаратам. Больные с множественной лекарственной устойчивостью (МЛУ) микобактерий туберкулеза - те, у которых диагностирована устойчивость МБТ к действию изониазида и рифампицина одновременно, с наличием или без наличия устойчивости к любым другим противотуберкулезным препаратам. Организация диагностики и лечения больных с множественной лекарственной устойчивостью МБТ требует значительных финансовых затрат в лабораторной диагностике, организации специализированного отделения для лечения данной категории больных, покупке противотуберкулезных препаратов второго ряда и лекарственных средств, для купирования побочных эффектов. Больные туберкулезом, выделяющие лекарственно-устойчивые штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих лекарственно-резистентными возбудителями. Чем больше число больных, выделяющих лекарственно-устойчивые МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной лекарственной устойчивостью. По определению экспертов ВОЗ, лекарственно-устойчивый туберкулез – это случай туберкулеза легких с выделением МБТ, устойчивых к одному и более противотуберкулезным препаратам. В последние годы в связи с ухудшением эпидемической ситуации существенно увеличилось число больных, выделяющих МБТ, устойчивые к основным противотуберкулезным препаратам. По данным ЦНИИ туберкулеза РАМН в 2008г. у 50% впервые выявленных и ранее не леченных противотуберкулезными препаратами больных в мокроте определялись лекарственно-устойчивые МБТ, из них у 27,7% имелась устойчивость к 2 основным противотуберкулезным препаратам – изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота выявления лекарственно-устойчивых МБТ возрастает до 95,5%. Феномен лекарственной устойчивости МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является лекарственная устойчивость. В активно размножающейся бактериальной популяции всегда имеется некоторое количество лекарственно-устойчивых мутантов, которые практического значения не имеют, но по мере сокращения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством лекарственно-чувствительных и устойчивых МБТ. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. В клинической практике необходимо исследовать лекарственную чувствительность МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких.
Механизм и динамика формирования лекарственной устойчивости .
Развитие лекарственной устойчивости у МБТ является результатом случайных генетических мутаций. В любой достаточно большой популяции МБТ существуют возникшие естественным путем микобактерии-мутанты. Подвижного фактора устойчивости, подобного плазмидам грамотрицательных палочек, в данном случае нет. Мутации не связаны между собой и происходят с низкой, но предсказуемой частотой в пределах 1-2 делений на 106- 108 МБТ. В Таблице 1 показаны коэффициенты и распространенность мутаций, обусловливающих устойчивость к четырем противотуберкулезным препаратам первого ряда.
Таблица 1. Коэффициенты и распространенность мутаций
|
Препарат |
Коэффициент мутации |
Распространенность мутации |
|
Изониазид |
||
|
Рифампицин |
||
|
Стрептомицин |
||
|
Этамбутол |
Так как мутации не взаимосвязаны, одновременное использование нес-кольких препаратов (полихимиотерапия) предотвращает приобретение устойчивости. Мутировавшие штаммы с устойчивостью к медикаменту А (например к изониазиду), будут уничтожены препаратом Б (например рифампицином), а штаммы, резистентные к медикаменту Б, окажутся уничтоженными лекарственным препаратом А, и так далее. При тяже-лом туберкулезе полости распада могут содержать более чем 108 быст-ро делящихся, активных МБТ. Спонтанное возникновение мутаций, приводящих к сочетанию устойчивости к изониазиду и рифампицину, должно быть редким явлением - примерно 1018. Однако веро-ятность появления лекарственной устойчивости на фоне неадекватной химиотерапии резко увеличивается при первоначальном заражении штаммами с высоким содержанием лекарственно устойчивых МБТ. В связи с этим, больные с полостями распада в легких, где происходит быстрое размножение большого количества МБТ, подвержены более высокому риску приобретения устойчивости.
В клинической практике развитие значительной лекарственной устой-чивости почти во всех случаях является следствием неадекватного ле-чения. Неадекватное лечение, в свою очередь, может быть обусловлено несколькими причинами, в числе которых:
Несоблюдение больным режима лечения
Неправильное назначение схемы химиотерапии
Отсутствие необходимого ассортимента и количества химиопрепаратов
Сопутствующие заболевания, препятствующие созданию адек-ватных концентраций химиопрепаратов как в крови, так и в оча-гах туберкулезного поражения (синдром малабсорбции, фиборозно - склеротические процессы в легких, обструктивные болезни легких и другие)
Организационные просчеты противотуберкулезной программы.
Зачастую, несоблюдение больным режима лечения расценивают как наиболее широко распространенную причину приобретенной лекар-ственной устойчивости. В реаль-ной жизни наиболее вероятными предпосылками возникновения боль-шинства случаев приобретенной лекарственной устойчивости МВТ яв-ляются организационные недостатки многих противотуберкулезных программ, отсутствие медикаментов и врачебные ошибки. Больные, у которых развилась устойчивость к одному препарату, более подвержены дальнейшему приобретению устойчивости (таким образом, могут последовательно появиться устойчивые к нескольким препаратам штаммы МБТ). Больные, у которых развилась лекарственная устойчивость, могут стать источником распространения устойчивых штаммов МБТ, в результате чего у следующих больных, в свою очередь, будет выявлена уже сфор-мировавшаяся или «первичная» лекарственная устойчивость. Термины - первичная, приобретенная, моно-, поли - и множественная лекар-ственная устойчивость - традиционно используют в западной литера-туре и их определения представлены в Таблице 2. Несмотря на это, мно-гие фтизиатры-практики находят данные определения неадекватными. Например, если исследование лекарственной чувствительности не бы-ло произведено в начале лечения, то во многих случаях невозможно от-личить действительно приобретенную устойчивость от первичной, что приводит к бесполезности данных определений. Более того, часто пута-ют термины множественная лекарственная устойчивость и полирезистентность.
Таблица2: Типы лекарственной устойчивости.
|
Определения типов лекарственной устойчивости МБТ |
|
|
Приобретенная лекарственная устойчивость |
Устойчивость, выявленная у больного, получавшего до этого противотуберкулезное лечение в течение по меньшей мере одного месяца. |
|
Первичная лекарственная устойчивость |
Выявление устойчивых штаммов МБТ у больного, который ранее от туберкулеза не лечился, либо получал препараты не более одного месяца |
|
Совокупная лекарственная устойчивость |
Распространенность лекарственной устойчивости среди всех категорий больных туберкулезом, независимо от предшеству-ющего лечения, в данной стране (местности) в данном году. |
|
Монорезистентность |
Устойчивость к одному противотубер-кулезному препарату. |
|
Полирезистентность |
Устойчивость к двум и более противоту-беркулезным препаратам, за исключением случаев одновременной устойчивости к изониазиду и рифампицину. |
|
Множественная лекарственная устойчивость |
Устойчивость, как минимум, к изониазиду и рифампицину. |
Российская Федерация претерпевает широкие социально-экономичес-кие и политические изменения, масштаб и глубина которых вызывает серьёзные последствия для всех слоев общества. Значительный удар был нанесен здоровью населения, что привело к резкому ухудшению ос-новных показателей состояния здоровья. В ходе всесторонних социаль-но-экономических трансформаций противотуберкулезная работа была серьезно подорвана и в настоящее время ситуация с туберкулезом в Российской Федерации достаточно серьезна.
Российская Федерация обладает завидной инфраструктурой противоту-беркулезной службы и долгой историей эффективной борьбы с ТБ. Программа борьбы с ТБ имеет вертикальную структуру с широкой сетью учреждений. Несмотря на это, организационные изменения сис-темы здравоохранения, одновременно с сокращением бюджета, резко снизили способность системы справляться с увеличивающимся количе-ством больных ТБ. Еще в 1990-х годах существовала нехватка противо-туберкулезных препаратов и начиная с середины 1990-х годов, с удвоением количества больных, положение резко ухудшилось.
Проведенные в 1998-99 годах в двух областях Российской Федерации исследования показали, что уровень МЛУ-ТБ в них выше среднего. Так, в Ивановской области 9% впервые выявленных больных и 25.9% ра-нее лечившихся имели МЛУ-ТБ. Аналогичные показатели распростра-ненности МЛУ-ТБ отмечены и в Томской области: 6.5% среди впервые выявленных больных и 26.7% среди ранее лечившихся.
Распространенность ТБ в пенитенциарных учреждениях Российской Федерации остается достаточно высокой, несмотря на значительное снижение за последние 5 лет. В конце 90-х годов смертность от ТБ в местах заключения почти в 30 раз превышала смертность среди осталь-ного населения, а заболеваемость - в 54 раза. Уровень МЛУ-ТБ достигал угрожающих значений. Примерно 10% заключенных имели активный ТБ, и до 20% из них - МЛУ-ТБ.
Стоит отметить, что многочисленные отчеты демон-стрируют удручающие результаты лечения больных с сочетанием МЛУ- ТБ и ВИЧ-инфекции. Быстрое установление диагноза и начало лече-ния больного с комбинированной инфекцией, возможно, снизит урон от таких вспышек заболевания. Можно ожидать, что растущая эпидемия ВИЧ-инфекции в Российской Федерации еще внесет свой вклад в расп-ространение ТБ и МЛУ-ТБ. Неотложный характер ситуации требует незамедлительных действий в эффективном партнерстве с различными международными организаци-ями, включая ВОЗ, Всемирный Банк и неправительственные организа-ции. Учитывая опыт действующих пилотных проектов борьбы с ТБ и привлечение новых ресурсов, можно надеяться, что Российская Феде-рация будет в состоянии решить множество серьезных проблем, стоя-щих перед здравоохранением страны, включая и проблему МЛУ-ТБ.
Полноценная программа DOTS в Томской области реализуется с 1996 года, однако эффективная программа лечения МЛУ-ТБ в Томской об-ласти началась лишь в 2000 году. К этому моменту в гражданском сек-торе насчитывалось более 600, а в пенитенциарном - около 200 боль-ных с МЛУ-ТБ. К концу 2002 года в программу было включено 256 боль-ных, из них более 100 больных в пенитенциарном учреждении г. Томс-ка, ИК № 1. Предварительные результаты продемонстрировали, что по-казатель излечения может превысить 80%. Однако, по прогнозам, да-же если все больные получат соответствующее лечение, понадобится несколько лет для того, чтобы увидеть значительное снижение как ТБ так и МЛУ-ТБ.
Методы диагностики лекарственной устойчивости.
Выявление больных с множественной лекарственной устойчивостью может основываться на разных методиках. Тестирование на питательных средах лекарственной чувствительности микобактерий к противотуберкулезным препаратам остается ключевым фактором выбора стратегии лечения. Схема химиотерапии основывается на результатах теста лекарственной чувствительности. От сроков диагностики МЛУ зависит своевременное назначение противотуберкулезной химиотерапии. Следовательно, для региональной противотуберкулезной программы важно правильно и рационально организовать диагностику устойчивости к основным противотуберкулезным препаратам.Перед началом лечения больных туберкулезом легких мокрота должна быть исследована трехкратно на МБТ методом прямой бактериоскопии и методом посева. Можно проводить исследования двух посевов на твердые среды и одного посева на жидкие питательные среды. В таком случае результат тестирования на устойчивость к препаратам первого ряда будет получен через 3-4 недели. При использовании непрямого метода абсолютных концентраций на твердых средах в большинстве случаев исследования лекарственная устойчивость определяется в течение 8-12 недель. Прямой метод предусматривает непосредственное использование полученного образца мокроты для тестирования лекарственной чувствительности. Если мокроту для прямого метода собирают у больных туберкулезом легких, у которых диагностированы МБТ методом микроскопии, то в таком случае повышаются чувствительность и специфичность метода и ускоряется диагностика МЛУ туберкулеза до 4-8 недель.В России для метода посева на твердые среды организован внешний контроль качества, что позволяет использовать его как стандарт диагностики устойчивости к препаратам первого ряда. Точность результатов тестирования лекарственной чувствительности варьирует в зависимости от лекарственных препаратов. Так, наиболее достоверные результаты отмечаются при тестировании чувствительности к рифампицину и изониазиду, менее надежные к этамбутолу и стрептомицину. Определение чувствительности к препаратам второго ряда необходимо проводить всем больным при выявлении устойчивости к препаратам первого ряда. Тестирование чувствительности к препаратам второго ряда сложнее, чем к некоторым препаратам первого ряда. В настоящее время внешнего контроля качества к определению чувствительности к препаратам второго ряда не существует, поэтому врачи должны понимать, что тестирование указывает на вероятность того, в какой степени данный препарат окажется или не окажется эффективным. Если полученная устойчивость к препаратам второго ряда повторяется два и более раз при исследованиях на твердых средах, вероятность отсутствия эффективности препарата при лечении туберкулеза чрезвычайно высока. Определение устойчивости к препаратам второго ряда позволяет диагностировать широкую и тотальную лекарственную устойчивость. Широкая лекарственная устойчивость - это МЛУ микобактерий туберкулеза, которые также устойчивы к какому-либо препарату из группы фторхинолонов и одному или большему числу инъекционных препаратов (канамицину, амикацину и капреомицину).Быстро внедряющиеся в практику здравоохранения молекулярно-биологические методы диагностики не позволяют пока использовать их как стандарт определения МЛУ вследствие отсутствия внешнего контроля качества и в некоторых методиках высокой специфичности. При улучшении специфичности методов молекулярной диагностики и внедрении внешнего контроля качества эти методы лекарственной чувствительности станут основным стандартом быстрой (1-2 дня) диагностики МЛУ МБТ.
Повышение эффективности лечения туберкулеза, вызванного лекарственно-устойчивыми МБТ, возможно за счет использования ускоренных методов обнаружения лекарственной устойчивости МБТ, что позволяет своевременно изменять режим химиотерапии, отменив препараты, к которым выявлена устойчивость МБТ, и назначить противотуберкулезные средства, к которым чувствительность сохранена. Исследование лекарственной устойчивости МБТ непрямым методом осуществляют после получения культуры МБТ, выделенных от больного, что требует от 30 до 45 суток. Коррекция химиотерапии в таком случае носит отсроченный характер и проводится, как правило, уже на конечном этапе интенсивной фазы химиотерапии. Лекарственную устойчивость МБТ в настоящее время определяют методом абсолютных концентраций, который основан на добавлении в плотную питательную среду Левенштейна–Йенсена стандартных концентраций противотуберкулезных препаратов, которые принято называть предельными. Для изониазида она составляет 1 мкг/мл, рифампицина – 40 мкг/мл, стрептомицина – 10 мкг/мл, этамбутола – 2 мкг/мл, канамицина – 30 мкг/мл, амикацина – 8 мкг/мл, протионамида (этионамида) – 30 мкг/мл, офлоксацина (таривида) – 5 мкг/мл, циклосерина – 30 мкг/мл и пиразинамида – 100 мкг/мл. Определение лекарственной устойчивости МБТ к пиразинамиду проводят на специально приготовленной яичной среде с рН 5,5–5,6. Культура МБТ считается устойчивой, если в пробирке выросло более 20 колоний. Применение прямого метода определения лекарственной устойчивости МБТ возможно при массивном бактериовыделении и осуществляется путем посева исследуемого материала на питательные среды, содержащие противотуберкулезные препараты, без предварительного выделения культуры МБТ. Результаты его учитываются на 21-28-й день, что позволяет раньше провести коррекцию химиотерапии. В последнее время для ускоренного определения лекарственной устойчивости применялся радиометрический метод с использованием автоматической системы BACTEC – 460 TB (Becton Dickinson Diagnostic Systems, Sparks, MD), который позволяет выявлять лекарственную устойчивость МБТ на жидкой среде Middlebrook 7H20 через 8–10 дней.
Лечение.
Выбор схемы химиотерапии осуществляется в соответствии с приказом Минздрава России № 109 от 21.03.03. Существует три вида стратегий лечения больных с множественной лекарственной устойчивостью микобактерий.
Первая стратегия - это стандартизованное лечение. Схема химиотерапии разрабатывается на основе репрезентативных данных о лекарственной устойчивости у различных групп больных (новый случай, рецидив заболевания и др.) в данном регионе. Индивидуализированная стратегия химиотерапии туберкулеза с МЛУ МБТ основывается на результатах тестирования чувствительности к препаратам первого и второго ряда и на предшествующих сведениях о принимавшихся противотуберкулезных препаратах. Эмпирическая стратегия лечения при подборе химиопрепаратов учитывает контакт с больным МЛУ МБТ, до получения собственных результатов лекарственной чувствительности. В настоящее время во многих туберкулезных программах используется стандартизованное или эмпирическое лечение с переходом на индивидуализированную терапию. Схема химиотерапии больных с МЛУ МБТ включает две фазы лечения: интенсивной терапии и продолжения лечения. Химиотерапия должна предусматривать назначение не менее четырех, а чаще всего пяти лекарственных препаратов, к которым сохранена лекарственная чувствительность и имеется убежденность в эффективности лекарств. Лекарственные препараты должны приниматься под непосредственным контролем медицинского или специально подготовленного персонала в течение 6 дней в неделю. Дозы лекарственных средств определяются в зависимости от веса больного. Препараты группы аминогликозидов, полипептидов, фторхинолонов, этамбутол, пиразинамид следует принимать в одной суточной дозе. Препараты второго ряда - протионамид, циклосерин и ПАСК - назначаются дробно на стационарном этапе лечения и однократно при амбулаторном лечении, если больной одномоментно может принять все лекарственные средства. Фаза интенсивной терапии подразумевает использование инъекционного препарата аминогликозидов (канамицина, амикацина или стрептомицина) или полипептида (капреомицина) не менее 6 месяцев лечения до 4-6 отрицательных посевов и заканчивается отменой данного антибиотика. Продолжительность лечения по рекомендациям «Руководства по программному лечению лекарственно-устойчивого туберкулеза» (ВОЗ, 2008) должна составлять 18 месяцев после прекращения бактериовыделения методом прямой бактериоскопии. Учитывая вышеуказанные принципы назначения химиотерапии больных с МЛУ МБТ, необходимо провести отбор лекарственных препаратов для схемы химиотерапии следующим образом:
1. Препараты первого ряда, к которым сохранена чувствительность, должны быть включены в схему химиотерапии. Определение чувствительности к пиразинамиду требует особых методик, которые редко используются в региональных референс-лабораториях, поэтому пиразинамид всегда включается в схему химиотерапии, но не учитывается среди 5 препаратов с известной лекарственной чувствительностью. Этамбутол включается в схему химиотерапии, если к нему сохранена лекарственная чувствительность МБТ.
2. Выбор инъекционного препарата основывается на более высокой эффективности, наличии побочных эффектов и стоимости лекарства. Наиболее эффективным является стрептомицин, если к нему сохранена чувствительность МБТ. Дешевым препаратом является канамицин, который имеет перекрестную устойчивость с амикацином. В сравнении с другими инъекционными препаратами назначение капреомицина предпочтительнее вследствие низкого процентного соотношения количества больных с устойчивостью к данному полипептиду и наличия меньшего количества побочных эффектов. В то же время это один из наиболее дорогостоящих препаратов.
3. Среди фторхинолонов по эффективности и себестоимости наиболее предпочтительным противотуберкулезным препаратом является левофлоксацин. В настоящее время при лечении туберкулеза с МЛУ МБТ при сохраненной чувствительности микобактерий к офлоксацину часто используется данный фторхинолон. Он соответствует параметрам себестоимости и эффективности.
4. Из четвертой группы противотуберкулезных препаратов в лечении используются два или все три бактериостатических препарата: протионамид, циклосерин, ПАСК.
Таким образом, схема химиотерапии для больного с множественной лекарственной устойчивостью часто является стандартизированной. В период фазы интенсивной терапии она состоит из 6 препаратов. На фазе продолжения лечения больные МЛУ МБТ получают схемы химиотерапии без инъекционного препарата не менее 12 месяцев, чтобы общий срок лечения составлял 24 месяца.
В период лечения ежемесячно исследуется мокрота на МВТ- дважды методом прямой бактериоскопии и методом посева. Для мониторинга побочных эффектов противотуберкулезных препаратов ежемесячно в период фазы интенсивной терапии проводят исследование креатинина, калия в сыворотке крови и аудиометрию. Весь период лечения, ежемесячно проводят исследования общего анализа крови, мочи, билирубина, трансаминаз, мочевой кислоты и электрокардиографию. Первое исследование тиреотропного гормона проводят через 6 месяцев лечения и затем повторяют каждые 3 месяца до окончания химиотерапии.
Система регистрации и отчетности больных с МЛУ МВТ необходима для мониторинга предупреждения распространения микобактерий с лекарственной устойчивостью и формирования широкой, тотальной резистентности МВТ. Для мониторинга эффективности лечения используется карта лечения МЛУ МВТ, в которой регистрируется, из какой группы больных был диагностирован туберкулез с МЛУ, бактериовыделение, определение лекарственной чувствительности каждой культуры МВТ и исходы лечения. Информационная система необходима для точной регистрации всех больных с лекарственной устойчивостью микобактерий, поэтому важно регистрировать больных из новых случаев, рецидивов заболевания, из группы - лечение после прерванного курса химиотерапии, после неэффективного первого курса химиотерапии и после неэффективного повторного курса химиотерапии. Важно регистрировать больных ссочетанной ВИЧ-инфекцией и МЛУ МВТ, так как эффективность лечения данной категории больных чрезвычайно низка и требуются неотложные мероприятия по предупреждению распространения туберкулеза среди ВИЧ-инфицированных, а также вируса иммунодефицита среди больных туберкулезом. Результаты лечения больных с МЛУ МВТ определяются через 24 месяца лечения и соответствуют результатам, указанным в приказе Минздрава России № 50 от 13.02.04: эффективный курс химиотерапии, подтвержденный микроскопией, посевом мокроты и клинико-рентгенологическими методами; неэффективный курс химиотерапии, подтвержденный микроскопией, посевом мокроты и клинико-рентгенологическими методами; прерванный курс химиотерапии; смерть от туберкулеза; больной выбыл; диагноз туберкулеза снят.
Важность проблемы диагностики и лечения множественного лекарственно-устойчивого туберкулеза обусловлена не только предупреждением его распространения, но и предотвращением возникновения случаев с широкой и тотальной лекарственной устойчивостью, стратегия лечения которой не будет разработана в ближайшие годы, до появления новых противотуберкулезных препаратов.
Другая не менее важная задача – правильное лечение впервые выявленных больных туберкулезом легких с использованием комбинации из 4–5 основных противотуберкулезных препаратов до получения данных лекарственной устойчивости МБТ. В этих случаях существенно повышается вероятность того, что даже при наличии первичной лекарственной устойчивости МБТ бактериостатическое действие окажут 2 или 3 химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии, при лечении впервые выявленных больных и назначение им в большинстве случаев только 3 химиопрепаратов является грубой врачебной ошибкой, что, в конечном счете, ведет к формированию вторичной лекарственной устойчивости МБТ. Наличие у больного туберкулезом легких лекарственно-резистентных МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и к летальным исходам. Особенно тяжело протекают поражения легких, вызванные полирезистентными МБТ, которые устойчивы как минимум к изониазиду и рифампицину, т.е. к основным и самым активным противотуберкулезным препаратам. Множественная лекарственная устойчивость МБТ является на сегодня наиболее тяжелой формой бактериальной устойчивости, а специфические поражения легких, вызванные такими микобактериями, называются полирезистентным туберкулезом легких. Лекарственная устойчивость МБТ имеет не только клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных обходится намного дороже, чем больных с МБТ, чувствительными к основным химиопрепаратам. Разработка лечения лекарственно-резистентного туберкулеза легких является одним из приоритетных направлений современной фтизиатрии. Для проведения эффективной химиотерапии больных хроническими формами туберкулеза легких с множественной лекарственной устойчивостью МБТ используют комбинации резервных противотуберкулезных препаратов, включающие пиразинамид и этамбутол, к которым медленно и довольно редко формируется вторичная лекарственная устойчивость. Все резервные препараты обладают довольно низкой бактериостатической активностью, поэтому общая длительность химиотерапии у больных с хроническим фиброзно-кавернозным туберкулезом легких и множественной лекарственной устойчивостью МБТ должна составлять не менее 21 мес. При отсутствии эффекта от проводимой химиотерапии резервными противотуберкулезными препаратами возможно применение хирургических методов лечения, наложение лечебного искусственного пневмоторакса или пневмоперитонеума. Оперировать следует после максимально возможного сокращения микобактериальной популяции, что определяется с помощью микроскопии или культурального исследования мокроты. После операции следует продолжать применять тот же режим химиотерапии минимум 18–20 мес. Лечебный искусственный пневмоторакс должен продолжаться у больных полирезистентным туберкулезом легких не менее 12 мес. Повышение эффективности лечения больных с лекарственно-устойчивым туберкулезом легких в значительной степени зависит от своевременной коррекции химиотерапии и применения противотуберкулезных препаратов, к которым сохранена чувствительность. Для лечения больных лекарственно-устойчивым и, особенно, полирезистентным туберкулезом легких необходимо использовать резервные препараты: протионамид (этионамид), амикацин (канамицин), офлоксацин. Эти препараты в отличие от основных (изониазид, рифампицин, пиразинамид, этамбутол, стрептомицин) намного более дорогостоящие, менее эффективные и имеют много побочных эффектов. Они должны быть доступны только для специализированных противотуберкулезных учреждений.
На сегодняшний день во фтизиатрической среде существует вполне обоснованное понимание того, что распространение лекарственной устойчивости является интегральной характеристикой эффективности проводимых противотуберкулезных мероприятий. Причины распространения лекарственной устойчивости относятся к разным уровням эпидемического процесса и управляются на разных уровнях организации лечебно-профилактической деятельности. Мониторинг лекарственной устойчивости микобактерий туберкулеза является важнейшей частью контроля над распространением этого инфекционного заболевания. Это понятие трактуется в довольно широких пределах, однако, собираемые статистические данные о лекарственной устойчивости возбудителя не отражают глубину существующей проблемы. К тому же, отсутствие на сегодняшний день единых принципов организации мониторинга туберкулеза с лекарственной устойчивостью в Российской Федерации ведет к искажению реальной картины и несопоставимости информации, получаемой из разных регионов. С 1999 г. в государственной статистической отчетности введен показатель распространения множественной лекарственной устойчивости (МЛУ) среди впервые выявленных больных. Однако до сегодняшнего дня не установлены правила регистрации и учета таких больных, правила расчета показателей территориальной распространенности туберкулеза с лекарственной устойчивостью, а также не задействованы в необходимом объеме механизмы обеспечения достоверности результатов исследований. В течение последних 15 лет неоднократно исследовалось распространение туберкулеза с лекарственной устойчивостью в различных регионах Российской Федерации. Однако агрегация данных по территориальному принципу или в динамике фактически оказалась невозможной, поскольку нет единых принципов организации мониторинга лекарственной устойчивости возбудителя туберкулеза. Достоверность показателя лекарственной устойчивости возбудителя туберкулеза основывается на соблюдении трех основных принципов: унифицированность используемых понятий и терминов, обеспечение репрезентативности исходных данных для расчета показателей территориальной лекарственной устойчивости и обеспечение достоверности лабораторных данных. Важнейшим понятием при описании инфекционного процесса является устойчивость циркулирующего штамма возбудителя, выделенного у впервые выявленного больного туберкулезом в период диагностики, т.е. до начала лечения. Другим важнейшим понятием является устойчивость возбудителя, приобретаемая в процессе лечения. На практике же активно используется понятие первичной устойчивости. Однако при отсутствии правил учета первичной устойчивости этот показатель не эффективен. Понятие первичной устойчивости стало собирательным: оно включало как реальную первичную устойчивость МБТ у впервые выявленных больных, так и лекарственную устойчивость МБТ у впервые выявленных больных в ходе химиотерапии (по сути – приобретенная лекарственная устойчивость). При отсутствии строгого контроля зачастую на учет как впервые выявленные также брались больные с предшествующей историей противотуберкулезной химиотерапии. Не редко оказывалось, что данные о территориальной распространенности лекарственной чувствительности, собираемые в оргметодотделах, и получаемые в бактериологических лабораториях, существенно не совпадали в силу разного учета больных как впервые выявленных. Иногда в отдельных территориях статистические показатели принимали парадоксальное значение. Например, эффективность лечения больных с МЛУ оказывалась выше, чем показатели для впервые выявленных больных; распространенность МЛУ среди больных с рецидивами была ниже, чем среди впервые выявленных больных. В процессе кураторских визитов и бесед с фтизиатрами выяснялось, что иногда статус МЛУ больного определялся по клиническим результатам (так называемая «клиническая» устойчивость), что является недопустимым для определения эпидемиологических показателей. Таким образом, при формировании показателей распространения лекарственной устойчивости возбудителя туберкулеза необходимо строго использовать понятия, описанные в регламентирующих документах. Существует три группы терминов, используемых при описании распространения лекарственной устойчивости. В первую группу входят понятия для характеристики больных, для которых проводятся тесты на лекарственную устойчивость. К ним относятся пациенты с бактериовыделением, установленным методом посева:
Ранее не леченный больной – впервые выявленный больной, зарегистрированный на лечение, ранее не принимавший противотуберкулезные препараты или принимавший их менее одного месяца.
Ранее леченный больной – пациент, зарегистрированный на повторное лечение, который ранее принимал противотуберкулезные препараты в течение периода, превышающего один месяц.
Для оценки показателей исходов химиотерапии группа ранее леченных больных разбивается на:
Ранее леченный больной с рецидивом туберкулеза и остальные случаи повторного лечения.
Ко второй группе относятся понятия, характеризующие штаммы микобактерий туберкулеза, выделенные от одного больного, по результатам тестов на лекарственную чувствительность:
Лекарственная устойчивость МБТ (ЛУ МБТ) – наличие лекарственно устойчивых штаммов МБТ в выделенной культуре.
Первичная лекарственная устойчивость - устойчивость МБТ у впервые выявленного больного, ранее не леченного или принимавшего противотуберкулезные препараты менее одного месяца (относится к ранее не леченным больным).
Вторичная лекарственная устойчивость - устойчивость МБТ у пациентов после противотуберкулёзной терапии, проводимой в течение месяца и более, на момент регистрации повторного курса химиотерапии (относится к ранее леченным больным).
Комбинированная лекарственная устойчивость – наличие у пациента культуры МБТ, устойчивой к более чем одному противотуберкулезному препарату, за исключением множественной лекарственной устойчивости.
Широкая лекарственная устойчивость (ШЛУ)– наличие у пациента культуры МБТ, устойчивой как минимум к изониазиду, рифампицину, офлоксоцину и одному из внутривенных противотуберкулезных препаратов (каномицин или каприомицин).
Спектр лекарственной устойчивости – характеристика МБТ по устойчивости к каждому из противотуберкулезных препаратов первого и/или второго ряда.
В третью группу терминов входят показатели лекарственной чувствительности популяции микобактерий туберкулеза, циркулирующей на определенной территории. К ним относятся:
Частота первичной лекарственной устойчивости. Показатель рассчитывается как отношение количества впервые выявленных больных туберкулёзом с первичной лекарственной устойчивостью к числу всех впервые выявленных больных, которым проводили исследование на лекарственную чувствительность, и характеризует эпидемиологическое состояние популяции возбудителя туберкулёза.
Частота лекарственной устойчивости среди ранее леченых случаев туберкулеза. Показатель рассчитывается как отношение количества устойчивых культур МБТ к числу штаммов, исследованных на наличие лекарственной устойчивости у больных, зарегистрированных на повторное лечение после неудачного курса химиотерапии или рецидива. По сути является показателем приобретенной устойчивости на момент регистрации больных на повторное лечение.
Частота множественной и широкой лекарственной устойчивости рассчитывается аналогичным образом для отдельных групп больных (впервые выявленных, ранее леченных больных и ранее леченных больных с рецидивами)
Следует отметить, что приведенные термины приняты и используются в международной практике (Всемирной организацией здравоохранения, Международным союзом борьбы с туберкулезом и заболеваниями легких, Комитетом зеленого света и др.), что позволяет получать сопоставимые результаты и находиться в одном формате исследований. Следует обратить внимание на то, что среди всех получаемых лабораторией результатов по лекарственной чувствительности для расчета эпидемиологических показателей учитываются только результаты, полученные из диагностического материала на первом месяце после регистрации больного для лечения. Обычно предполагается, что учет всех собранных данных по территории означает их репрезентативность, но в случае с определением показателей лекарственной чувствительности МБТ это не всегда так.
Во-первых, в силу многоступенчатости процесса получения данных реальные эпидемические процессы отражаются в искаженном виде (эффективность выявления бактериовыделителей в лучших случаях составляет 70%, а часто - менее 50%; охват тестами на лекарственную устойчивость составляет 70-90% всех бактериовыделителей; кроме того, результаты теста на лекарственную чувствительность являются следствием качества лабораторной работы, которое зачастую не контролируется).
Во-вторых, на практике отсутствие данных по бактериовыделению и по лекарственной чувствительности, как правило, отождествляется с отрицательными результатами исследований.
В-третьих, выявление бактериовыделителей по территории субъекта РФ, как правило, идет не равномерно, поэтому представленность таких данных для учета распространенности лекарственной чувствительности может не отражать реальные эпидемиологические процессы. Несоблюдение принципа репрезентативности исходных данных приводит к неестественному разбросу значений показателя распространения туберкулеза с МЛУ в различных субъектах России, как это видно в статистических отчетах за последние годы.
Так, например, разброс распространения МЛУ составлял в 2006 году от 3% (Смоленская, Курская, Амурская области, Краснодарский край) до 80% (Эвенкийский АО). В свете вышесказанного, при расчете территориального показателя необходимо из стихийно получаемой выборки больных сформировать вторичную выборку по принципу равномерной представленности больных из отдельных районов (репрезентативности по районам). На практике это означает следующее. Во-первых, необходимо рассчитать квоты на число включаемых в анализ больных для каждого района (где проводятся бактериологические исследования) на основе показателей заболеваемости в районах и числа выявленных бактериовыделителей. То есть, для расчета территориального показателя лекарственной устойчивости должна формироваться вторичная выборка из всех имеющихся результатов определения лекарственной устойчивости. В районе с наименьшим числом бактериовыделителей в расчет показателей включаются приемлемые результаты всех проведенных исследований. Квоты для остальных районов рассчитываются в соответствии с принципом равномерной представленности больных из всех районов. В этом случае общее число исследований, включаемых в расчет показателей, будет меньше имеющегося числа больных с результатами лекарственной чувствительностью. В выборку для расчета территориального показателя результаты включаются с соблюдением пропорции положительных результатов. Например, пусть в трех районах какого-то региона уровень заболеваемости населения туберкулезом составляет 50, 70 и 100 больных на 100 тыс. населения, при этом район с наибольшей заболеваемостью является самым маленьким. Предположим, в этих районах выявлено 70, 50 и 40 больных, при этом число бактериовыделителей составляет 40, 40 и 20 человек (Табл. 3).
Таблица 3
Пример расчета территориального показателя лекарственной устойчивости среди впервые выявленных больных
|
Заболеваемость (на 100 тыс. населения) |
|||
|
Число выявленных больных |
|||
|
Число бактериовыделителей |
|||
|
Число больных с лекарственной устойчивостью |
|||
|
Всего число тестов |
|||
|
Число положительных тестов |
|||
|
Показатель ЛУ С соблюдением принципа репрезентативности 31,8% Без соблюдения принципа репрезентативности 21% |
|||
Наименьшее число бактериовыделителей выявлено в третьем районе, поэтому расчет квот будет осуществляться на основе соотношений, найденных для третьего района. Так, при уровне заболеваемости 100 учитывается 20 бактериовыделителей, тогда при уровне заболеваемости 50 должно учитываться 10 бактериовыделителей, а при уровне заболеваемости 70 – 14 бактериовыделителей. Среди учитываемых результатов тестов на лекарственную чувствительность доля положительных для каждого региона должна сохраняться. То есть, в первом районе при соотношении положительных и отрицательных результатов теста как 1:7 в квоту войдет 1 положительный и 9 отрицательных результатов. Во втором районе при соотношении положительных и отрицательных результатов теста как 3:16 в квоту войдет 3 положительных и 11 отрицательных результатов. Тогда величина территориального показателя лекарственной чувствительности, полученная с соблюдением принципа репрезентативности данных по районам, будет на треть больше, чем его оценка на основе всех собранных результатов тестов. Такой подход предусматривает ведущую роль оргметодотделов федеральных и территориальных противотуберкулезных учреждений при организации мониторинга показателей распространения лекарственной устойчивости возбудителя туберкулеза. Учет территориальной репрезентативности должен проводиться для оценки показателя у впервые выявленных больных. Целесообразность учета территориальной репрезентативности при оценке показателя ЛУ у ранее леченных больных должен быть предметом отдельного исследования, поскольку приобретенная устойчивость МБT к противотуберкулезным препаратам в большей мере зависит от качества лечения, нежели является характеристикой эпидемиологической ситуации. Для бактериологических лабораторий это также означает дополнительный этап классификации результатов. Следует добавлять маркировку для тех результатов, которые могут быть включены оргметодотделами во вторичную выборку для расчета территориальных показателей лекарственной устойчивости. К ним относятся только те результаты, которые удовлетворяют требованиям обеспечения достоверности лабораторных исследований. Это означает соблюдение следующих правил:
Не включать результаты лекарственной чувствительности при объеме роста МБТ менее 5 КОЕ при первичном посеве, поскольку при таком количестве выросших колоний результаты устойчивости имеют недостаточную точность и большом числе случаев (от 10 до 30% в зависимости от препарата) не совпадают при повторном тесте на лекарственную чувствительность.
Не включать результаты лекарственной чувствительности в случае регистрации критической чувствительности МБТ (когда рост на пробирке с противотуберкулезным препаратом близок к 20 КОЕ), что также ведет к большим ошибкам при повторных тестах на лекарственную чувствительность (до 25%).
Репрезентативность данных означает не только их контролируемое количество, но и соблюдение единого порядка их получения во всех регионах. Сбор исходных данных должен осуществляться в районных туберкулезных диспансерах и микробиологических лабораториях, на базе которых проводится лечение больных. Исследование лекарственной чувствительности МБТ для больных с целью формирования показателей должно осуществляться преимущественно в центральных территориальных (региональных) лабораториях.Там же должна проводиться видовая идентификация культур для всех больных.
Система обеспечения достоверности лабораторных данных является многоуровневой скоординированной системой контроля организационных, лабораторных, статистических методов. Она заключается в контроле качества ведения документации, внутрилабораторном контроле качества исследований, внешнем контроле качества исследований, контроле оценок статистических показателей.В нашей стране контролю качества ведения документации уделяется недостаточно внимания, хотя практика обеспечения качества данных принята во всем мире. Она включает в себя как минимум: проведение регулярной сверки собираемой учетной информации в организационно-методических отделах и бактериологических лабораториях на территориальном уровне; как правило, 1 раз в 2 -4 недели, в зависимости от объема данных; ведение территориального регистра всех больных с МЛУ и ШЛУ; выборочный контроль передаваемых данных, на федеральном и региональном уровнях (выборочный контроль списков больных с МЛУ и ШЛУ, а также некоторой выборки больных с чувствительными и устойчивыми культурами МБТ). Из-за отсутствия твердых требований к качеству лабораторных исследований достоверность их результатов в некоторых случаях невозможно оценить объективно. Согласно официальным данным, более 380 микробиологических лабораторий проводят анализы на чувствительность возбудителя туберкулеза к противотуберкулезным препаратам, но при этом в разных лабораториях применяются методики, результаты которых могут оказаться несопоставимыми между собой. Во многих случаях лабораторные данные о лекарственной чувствительности МБТ получают без соблюдения лабораторных стандартов.Помимо формальных требований к качеству лабораторных исследований необходимо учитывать особенности методик проводимых тестов, объективно не позволяющих достичь требуемой точности исследований (95%). В первую очередь это касается олигобациллярных больных, которых необходимо исключать из расчета территориальных показателей лекарственной устойчивости. По данным обследования лабораторий, проведенного в ходе кураторских визитов и анкетирования, используемые в бактериологических лабораториях критические концентрации препаратов для определения лекарственной чувствительности МБТ вдвое отличались как в одну, так и в другую сторону от рекомендуемых стандартов. Было выяснено, что правила расчетов разведения препаратов для постановки тестов в большинстве лабораторий не соблюдаются, что ведет к искажению результатов. Чтобы не превысить задаваемую ошибку измерения, необходимо:
обеспечение точности результатов тестов на лекарственную чувствительность не менее 95% соответствия результатов тестов к изониазиду и рифампицину и не менее 85% соответствия результатов тестов к этамбутолу и стрептомицину, для чего необходимо обеспечить регулярное участие лаборатории в циклах внешней оценки качества на основе тест-панели аттестованных культур МБТ;
минимизация ошибки лабораторного определения ЛУ МБТ (не более 5% для штаммов МБТ с МЛУ) независимо от используемого метода, для чего следует максимально централизовать исследования на ЛУ МБТ. При этом все лаборатории должны участвовать в циклах внешней оценки качества.
Очевидно, что во всех регионах лабораторные тесты на лекарственную чувствительность МБТ должны проводиться по единой стандартизованной методике и, преимущественно, в головных территориальных лабораториях ПТУ субъектов Федерации. Значимость проблемы качества лабораторных исследований определяется сложностью метода определения лекарственной чувствительности МБТ. От процедуры получения мокроты от больного до заключения бактериологической лаборатории о чувствительности или устойчивости выделенной культуры МБТ выполняется ряд отдельных последовательных процедур. На каждой из них есть своя вероятность ошибки. Накопленная ошибка к моменту получения результата теста в настоящее время составляет около 30%. В лучшем случае при устранении ошибок, зависящих от качества лабораторной работы, накопленная ошибка составит 10%, на самом деле достижимым можно считать уровень ошибки для разных противотуберкулезных препаратов от 12 до 17% (Табл. 4)
Таблица 4
Формирование накопленной ошибки определения лекарственной устойчивости образца от одного больного
|
Процедуры(и источники ошибки) |
Вероятность ошибки, % |
||
|
Реальная ситуация |
Идеальная ситуация |
Достижимая ситуация |
|
|
1 Подготовка диагностического материала (неточность концентраций для деконтаминантов) |
|||
|
2 Использование нестандартных питательных сред (разная высеваемость чувствительных и устойчивых культур) |
|||
|
3 Соблюдение температурного режима (потеря культур) |
|||
|
4 Подготовка пробирок со средами и противо-туберкулезными препаратами (качество сред и реактивов, неточность концентраций) |
|||
|
5 Учет олигобациллярных культур (в пересчете на все культуры) |
|||
|
6 Учет культур с критической чувствительностью (в пересчете на все тесты |
|||
|
Накопленная ошибка (%) |
|||
Рассмотренная ситуация подчеркивает важность проблемы обеспечения высокого качества работы бактериологических лабораторий и постановки ими тестов на лекарственную чувствительность микобактерий. Для обеспечения качества лабораторных данных о лекарственной чувствительности во всех регионах страны, требуется создать гарантированную систему постоянного контроля качества лабораторных исследований для бактериологических лабораторий ПТУ. Контроль качества исследований должен осуществляться на всех уровнях. Все бактериологические лаборатории должны проводить тесты внутренней и внешней оценки качества исследований. Внешняя оценка качества исследований в лабораториях должна проводиться как на основе единой референс-панели штаммов МБТ, так и в форме выборочного контроля культур. При наличии неудовлетворительных результатов внешней оценки качества исследований расчет среднероссийских показателей должен проводиться дважды: с учетом и без учета результатов исследований в субъектах РФ, в которых были такие результаты. Для обеспечения качества лабораторных исследований на федеральном уровне необходима постоянно действующая система внешнего контроля качества, интегрированная в международную систему внешней оценки качества лабораторной диагностики туберкулеза. Сложившаяся на сегодняшний день практика подготовки тест-панели культур МБТ для ФСВОК бактериологами общего профиля, без достаточного опыта во фтизиобактериологии, приводит к определенным системным ошибкам в результате использования иных методик определения лекарственной чувствительности, несоблюдения правил подготовки питательных сред, пересева культур МБТ и т.д. К тому же, курирующие лаборатории лишаются возможности оказывать помощь в этом разделе работ. Таким образом, для обеспечения достоверности оценки показателя распространенности ЛУ МБТ необходимо строгое соблюдение технологии формирования показателя. На сегодняшний день это означает необходимость ряда дополнений в организацию противотуберкулезной службы. Необходимо введение дополнительных функций для оргметодотделов и для бактериологических лабораторий как в головных противотуберкулезных учреждениях, так и федеральных профильных НИИ. Правила сбора репрезентативных данных должны контролироваться оргметодотделами головных противотуберкулезных учреждений субъектов РФ. Разработка и внедрение этих правил должна осуществляться курирующими профильными НИИ. Для координации деятельности отдельных референс-лабораторий нужен специальный единый методический центр по внешней оценке качества исследований. Целесообразно организовать такой методический центр при МЗ РФ. Реализация названных принципов организации мониторинга лекарственной устойчивости возбудителя туберкулеза позволит получить репрезентативные данные распространения лекарственно устойчивых форм МБТ, что позволит определить возможность внедрения современных лечебных технологий, разработать государственную стратегию лечения больных туберкулезом с множественной лекарственной устойчивостью возбудителя, создать предпосылки для использования в борьбе с туберкулезом опыта и возможностей международных организаций.
Профилактика развития лекарственной устойчивости.
Методы предотвращения естественных мутаций, ведущих к формирова-нию лекарственной устойчивости МБТ, неизвестны. Однако продуман-ное и адекватное лечение больных ТБ может свести к минимуму селек-цию устойчивых штаммов МБТ, как у впервые начинающих лечение, так и у пациентов, его уже получавших. Помимо выбора правильной схемы химиотерапии, абсолютно необходимо обеспечить соблюдение режима лечения. И наконец, очень важным является предотвращение распространения МЛУ-ТБ среди тех, кто имеет контакты (или возмож-ность таковых) с больными МЛУ-ТБ.
Диагностика туберкулеза с множественной лекарственной устойчивостью. Единственный способ подтвердить диагноз МЛУ-ТБ - это исследовать лекарственную чувствительность выделенной от пациента культуры микобактерий и доказать ее устойчивость, как минимум, к изониазиду и рифампицину.У всех больных перед началом лечения рекомендуется исследовать чувствительность МБТ к изониазиду, рифампицину, этамбутолу и стрептомицину. Это обеспечит выявление всех больных МЛУ-ТБ. Если есть возможность, то в первичный скрининг можно включить определе-ние чувствительности и к другим препаратам, например канамицину, офлоксацину и этионамиду. При обнаружении МЛУ-ТБ может быть назначено исследование чувствительности ко всем препаратам второго ряда. Если у пациента на фоне лечения продолжается бактериовыделение (по результатам микроскопии или посева мокроты) или наблюдает-ся клинико-рентгенологическое прогрессирование туберкулезного про-цесса, необходимо повторно исследовать лекарственную чувствитель-ность МБТ. Если в каком-либо регионе ресурсы для исследования лекарственной чувствительности ограничены, то более практичным является избира-тельный подход к исследованиям лекарственной чувствительности на основании индивидуальных показаний. В таких случаях, на посев и пос-ледующее исследование устойчивости направляют образцы мокроты только от больных с подозрением на МЛУ-ТБ. Группы пациентов, у которых данный подход может оказаться полез-ным:
Пациенты, ранее лечившиеся по поводу ТБ
Пациенты, имевшие контакт с больным с подтвержденным диагнозом МЛУ-ТБ.
Пациенты, которые имели контакт с больными ТБ, умершими в ходе лечения под непосредственным наблюдением (DOT).
Работники учреждений здравоохранения.
Пациенты, инфицированные ВИЧ
Пациенты, у которых результаты микроскопии мокроты сохра-няются положительными (или вновь становятся положительными) после 4 месяцев лечения.
Пациенты, находившиеся в местах лишения свободы
Достоверные результаты исследования лекарственной чувстви-тельности МБТ являются основой оптимального лечения МЛУ-ТБ. Многие региональные лаборатории имеют возможность исследовать лекарственную чувствительность только к препаратам первого ряда (Н, R, Е, S). Исследование чувствительности к препаратам второго ряда обычно проводят в специализированных центрах или международных референс-лабораториях. Во всех лабораториях необходим регулярный контроль качества результатов.
Список литературы.
Туберкулез (9)
Контрольная работа >> Медицина, здоровьеОрганизовать даже изоляцию больных с лекарственно устойчивыми формами туберкулеза" , - констатировал главный санитарный врач... многообразие методов профилактики, диагностики, лечения и реабилитации при туберкулезе , что предполагает разработку осуществления...
Туберкулез кишечника и Туберкулез брыжеечных лимфатических узлов
Реферат >> Медицина, здоровьеЭто связано с наличием лекарственно -устойчивых мутантов микобактерий. Для... длительных курсов химиотерапии. Лечение туберкулеза кишечника должно проводиться в... наиболее эффективных режимов лечения туберкулеза кишечника является ежедневный прием изониазида и...
Лекарственное растительное сырье содержащее сапонины
Реферат >> История... лекарственного сырья. Проблема применения лекарственных растений в производстве лекарственных ... при взбалтывании с водой, как и в случае присутствия тритерпеновых сапонинов, образует устойчивую ... используются при лечении сердечной... при некоторых формах туберкулеза ...
Балабанова Я.М., Радди М., Грэм К., Маломанова Н.А., Елизарова Э.Д., Кузнецов С.И., Гусарова Г.И., Захарова С.М., Мелентьев А.С., Крюкова Э.Г., Федорин И.М., Голышевская В.И., Дорожкова И.Р., Шилова М.В., Ерохин В. В., Дробневский Ф. Анализ факторов риска возникновения лекарственной устойчивости у больных туберкулезом гражданского и пенитенциарного секторов в Самарской области России // Проблемы туберкулеза и болезней легких. - 2005. - № 5. - С. 25-31.
Баранов А.А., Марьяндышев А.О., Низовцева Н.И., Опарина Е.Н., Преснова С.Э., Гвоздовская Л.А., Маркелов Ю.М., Трекин И.А., Тунгусова О.С., Маннсокер Т. Распространение первичной лекарственной устойчивости при туберкулезе в четырех административных территориях Северо-Западного федерального округа Российской Федерации // Проблемы туберкулеза и болезней легких. – 2006. - №12. - С. 9-12.
Беляков В.Д Эпидемический процесс (теория и метод изучения).- Л.: Медицина, 1964.- 238 с.
Богородская Е. М., Стерликов С. А., Попов С. А. Проблемы формирования эпидемиологических показателей по туберкулезу // Проблемы туберкулеза и болезней легких. - 2008. - № 7. – C. 8-14.
Биглхол Р. Основы эпидемиологии. ВОЗ. Женева, 1994.- С.1-16.
Вишневский Б.И. Основные направления работы лаборатории микробиологии туберкулеза // Туберкулез: проблемы диагностики, лечения и профилактики. - СПб., 2003. - С. 34-38.
Власов В.В. Эпидемиология в современной России // Международный журнал медицинской практики. – 2001, №2:. – С.27-29.
Власов В.В. Эффективность диагностических исследований. М: Медицина 1988. - 245 с.
Дорожкова И.Р., Попов С.А., Медведева И.М. Мониторинг лекарственной устойчивости возбудителя туберкулеза в России 1979-1998 гг. // Проблемы туберкулеза и болезней легких.- 2000.- №5. –С.19-22
Дорожкова И.Р., Попов С.А., Медведева И.М. Компоненты мониторинга лекарственной устойчивости возбудителя туберкулеза для оценки эффективности национальной программы противотубркулезной помощи населению // Проблемы туберкулеза и болезней легких.- 2001.- №2. –С.18-20.
Попов С.А., Пузанов В.А., Сабгайда Т.П., Антонова Н.В., Казаков А.C. Основные проблемы региональных бактериологических лабораторий противотуберкулезных учреждений // Проблемы туберкулеза и болезней легких. - 2008. - № 5. - С. 29-35.
Попов С.А., Пузанов В.А., Сабгайда Т.П., Богородская Е.М. Мониторинг лекарственной устойчивости микобактерий туберкулеза в регионах Российской Федерации // Информационное письмо (направлено в субъекты за № 10-11/06-6013 от 18 мая 2007 Росздрав 2008). - 8с.
Попов С.А., Пузанов В.А., Сабгайда Т.П. Пути оптимизации лабораторной диагностики туберкулеза. // Справочник заведующего КДЛ, 2008, №12, С.17-28.
Приказ МЗ РФ от 21.03.2003 г. № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерации»
Руководство по эпидемиологии инфекqционных болезней. - Т. 1. Под ред. В.И. Покровского. - М.: Медицина, 1993. - 373 с.
Севастьянова Э.В., Петрова Л.В. Мониторинг лекарственной устойчивости микобактерий туберкулеза в Республике Марий Эл // Проблемы туберкулеза и болезней легких.- 2008.- №9. –С.13-26.
туберкулеза , нарастание полирезистентности грозит превратить туберкулез в неизлечимое...
а) чувствительные ко всем противотуберкулезным препара-
там
б) монорезистентные МБТ;
в) полирезистентные МБТ;
г) моножественно лекарственно устойчивые М БТ;
д) множественно лекарственно устойчивые М БТ, устойчивые
к сочетанию основных и резервных противотуберкулезных
препаратов.
56. Первичная лекарственная устойчивость МБТ свидетельствует:
а) об эндогенной реактивации;
б) об экзогенной суперинфекции;
в) о гематогенной диссеминации;
г) о лимфогенной диссеминации;
д) о бронхогенном обсеменении.
57. Токсические побочные реакции связаны:
а) с дозой и длительности приема противотуберкулезного пре-
парата;
б) с антигенным действием противотуберкулезного препарата;
д) со всем вышеперечисленным.
58. Аллергические побочные реакции связаны:
а) с индивидуальной чувствительностью организма больного;
б) с дозой и длительности приема противотуберкулезного пре-
парата;
в) с формой туберкулезного процесса;
г) с местом проживания больного;
д) со всем вышеперечисленным.
59. Какой стандартный режим химиотерапии назначают впервые вы-
явленному больному туберкулезом:
г) III;
Д) IV.
60. Какой стандартный режим химиотерапии назначают больному ту-
беркулезом с высоким риском развития лекарственной устойчиво-
стиМБТ:
61. Какой стандартный режим химиотерапии должен получать впервые
выявленный больной из длительного контакта с больным фиброз-
но-кавернозным туберкулезом:
63. В случае коррекции лечения при выявлении лекарственной устой-
чивости к изониазиду или рифампицину в режим химиотера-
пии следует добавить:
а) один препарат основного ряда;
б) один препарат резервного ряда;
в) один препарат, к которому сохранена чувствительность
МБТ;
г) один препарат, к которому определена устойчивость МБТ;
д) два и более препарата, к которым сохранена чувствитель-
ность МБТ.
64. Общая продолжительность основного курса химиотерапии лекар-
ственно-устойчивого туберкулеза составляет в месяцах:
65. Показанием для назначения кортикостероидов у больных туберку-
лезом является:
а) казеозная пневмония;
б) туберкулез бронхов;
в) экссудативный плеврит;
г) менингит;
д) все вышеперечисленное.
66. Применение иммуномодуляторов при туберкулезе обусловлено:
а) дефицитом массы тела;
б) ускоренным СОЭ;
в) эозинофилией;
г) иммунодефицитом;
д) интоксикацией.
67. Лечение искусственным пневмотораксом показано при:
а) очаговом туберкулезе;
б) кавернозном туберкулезе;
в) казеозной пневмонии;
г) экссудативном плеврите;
д) цирротическом туберкулезе.
68. Пневмоперитонеум показан при:
а) каверне в верхней доле легкого;
б) очагах в нижней доле легкого;
в) каверне в нижней доле легкого;
г) экссудативном плеврите;
д) циррозе легкого.
69. При сохранении чувствительности МБТ к 3-4 противотуберкулез-
ным препаратам основным видом оперативного вмешательства
является:
а) торакопластика;
б) экстраплевральный пневмолиз;
в) кавернотомия;
г) резекция пораженных участков;
д) плевральная пункция.
70. Длительность поствакцинального противотуберкулезного иммуни-
тета, обусловленного введением вакцины БЦЖ:
а) 1-2 года;
б) 3-- года;
г) 5-7 лет;
д)
71. В 1 дозе (0,1 мл раствора) вакцины БЦЖ содержится количество
препарата в мг:
72. Метод введения вакцины БЦЖ:
а) пероральный;
б) внутрикожный;
в) накожный;
г) подкожный;
д) внутримышечный.
73. Вторая ревакцинация БЦЖ проводится в возрасте:
б) 10-11 лет;
74. Основным противотуберкулезным препаратом для проведения хи-
миопрофилактики является:
а) изониазид;
б) этамбутол;
в) пиразинамид;
г) рифампицин;
д) стрептомицин.
75. Длительность курса химиопрофилактики составляет:
а) 1-2 недели;
б) 2-4 недели;
в) 4-8 недель;
г) 3-6 месяцев;
д) 9 месяцев.
76. Для проведения химиопрофилактики у контактных лиц наиболее
важно знать:
а) результаты исследования устойчивости источника;
б) фазу туберкулезного процесса источника;
в) длительность заболевания источника;
г) санитарно-гигиеническое состояние жилища;
д) соблюдение режима лечения больным;
е) нарастание чувствительности к туберкулину.
77. Первый противотуберкулезный диспансер был открыт в городе:
а) Эдинбурге;
г) Москве;
д) Казани.
78. День борьбы с туберкулезом называется как день:
а) Белой ромашки;
б) Голубой ромашки;
в) Синей ромашки;
г) лотоса;
д) независимости.
79. Здоровые лица, находящиеся в контакте с источником туберкулез-
ной инфекции, наблюдаются в группе диспансерного учета:
80. Впервые выявленные пациенты с сомнительной активностью ту-
беркулезного процесса наблюдаются в группе диспансерного учета:
81. В органы санитарно-эпидемического контроля сведения о впервые выявлено больном туберкулезом направляется документация в виде формы №:
82. Больной Ю., 20 лет. По профессии слесарь. Ранее туберкулезом не
болел. Последнее рентгенологическое обследование - два года на-
зад. Контакт с больными туберкулезом отрицает. В анамнезе хро-
нический вирусный гепатит В. Заболел остро с подъемом температу-
ры тела до 38 °С. Жалобы на боль в правой половине грудной клетки
при глубоком вдохе, кашель с мокротой, слабость, потливость. Вы-
полнена обзорная рентгенограммы органов грудной полости, запо-
дозрен туберкулез. Направлен в ПТД по месту жительства. Мето-
дом люминесцентной микроскопии в мокроте найдены МБТ. После
проведенного обследования больному выставлен диагноз: инфиль-
тративный туберкулез верхней доли правого легкого в фазе распада,
МБТ+. В биохимических показателях: повышение активности АЛТ
и ACT в три раза, незначительное повышение тимоловой пробы.
Какой противотуберкулезный препарат нельзя применять?
а) Стрептомицин.
б) Изониазид.
в) Рифампицин.
г) Этамбутол.
д) Фтивазид.
83. Больной В., 45 лет. Страдает алкоголизмом. Туберкулезом болеет с
1997 г. В течение последних лет периодически короткие курсы химиотерапии в условиях стационара, которые прерываются по вине
больного из-за нарушения больничного режима. Данных о лекарственной чувствительности МБТ нет. В отделение госпитализирован в состоянии средней тяжести, истощен, температура до 38 °С, кашель, одышка при физической нагрузке, боли в области левой половины грудной клетки. Печень выступает из-под реберной дуги на 4 см. Методом микроскопии по Цилю-Нельсену и при посеве в мокроте обнаружены МБТ, устойчивые к изониазиду, рифампицину и стрептомицину. Анализ крови: НЬ. - 143; Эр. - 4,5; Цв.п. - 0,95; п. - 11%; с. - 57%; э. - 4%; л. - 20%; м. - 18%; СОЭ - 34 мм в час. Больному выставлен диагноз: фиброзно-кавернозный туберкулез верхней доли левого легкого в фазе инфильтрации, М БТ+. Лекарственная устойчиовость к изониазиду, рифампицину и стрептомицину. Какой режим химиотерапии необходимо назначить больному?
г) III;
Д) IV
84. Ребенку в возрасте 7 лет перед проведением первой ревакцинации в школе поставлена проба Манту с 2 ТЕ ППД-Л. Результат - папула 10 мм. Рубчик на левом плече - 3 мм. Какое заключение можно дать на основании этих данных:
а) инфицирование микобактериями туберкулеза;
б) у ребенка сохраняется поствакцинальный иммунитет;
в) первичное инфицирование микобактериями туберкулеза;
г) гиперергическая чувствительность к туберкулину.
ОТВЕТЫ И ПОЯСНЕНИЯ
1. Правильный ответ - б.
Только М. tuberculosis bovines - бычий тип, вызывающий 10-15% всех заболеваний у людей имеет исходную устойчивость к пира-зинамиду.
2. Правильный ответ а.
Возбудителями туберкулеза у человека в 92% случаев являются М. tuberculosis humanus, a M. tuberculosis bovis и М. tuberculosis africanum вызывают развитие туберкулеза у человека соответственно, примерно, в 5% и 3% случаев.
3. Правильный ответ - в.
Устойчивость МБТ к кислотам, щелочам и спирту обусловлена высоким содержанием в клеточной стенке миколевой кислоты.
4. Правильный ответ - в.
которая проявляется в способности их сохранять окраску, даже при интенсивном обесцвечивании кислотами, щелочами и спиртом, обусловлена высоким содержанием в клеточных стенках микобактерий миколевой кислоты, липидов и в.
5. Правильный ответ - в.
Цикл простого деления материнской клетки на две дочерние за-
нимает от 13-14 часов до 18-24 часов. Микроскопически види-
мый рост микроколоний на жидких средах можно обнаружить на
день, видимый рост колоний на поверхности твердой сре-
ды - на день.
6. Правильный ответ - д.
Одним из характерных свойств М БТ является их способность изменяться под воздействием внешних факторов. Полиморфизм возбудителя проявляется в образовании нитевидных актиномицет-ных, кокковидных и L-форм. В связи с такой перестройкой меняется не только морфология МБТ, но и антигенный состав и патогенность для человека и животных.
7. Правильный ответ - д.
Одним из характерных свойств МБТ является их полиморфизм и способность изменяться под влиянием неблагоприятных факторов внешней среды.
8. Правильный ответ - в.
Корд-фактор, или фактор вирулентности, расположен в виде монослоя и состоит на 30% из трегалазы и на 70% из миколевой кислоты, с ним связывают устойчивость МБТ к растворам кислот, щелочей и спиртам.
9. Правильный ответ - г.
Геном МБТ имеет длину 4 411 529 пар нуклеотидов, которые почти в 70% представлены гуанином и цитозином. Нуклеотид содержит
4000 генов, из которых 60 кодируют компоненты РН К. Для МБТ
имеются уникальные гены, в частности гены mtp40 и mpb70, кото-
рые применяются для выявления в ре-
акции (ПЦР).
10. Правильный ответ - г.
В высохшей мокроте МБТ могут сохраняться до 10-12 месяцев (в жилом помещении).
11. Правильный ответ - г.
В сыром молоке МБТ выживают 14-18 дней, скисание молока не ведет к их гибели. При прогревании молока они выдерживают нагревание 55-60 °С в течение 60 минут, нагревание 70 °С - в течение 20 минут, кипячение убивает МБТ в течение нескольких минут.
12. Правильный ответ - б.
У больных с наличием полостей распада в легком МБТ могут быть выявлены двумя методами - микроскопией мокроты и посевом ее на питательные среды. Именно эта категория больных составляет в настоящее время основной резервуар туберкулезной инфекции в обществе. По данным ВОЗ, один такой больной может за сутки выделять до 7 млрд МБТ.
14. Правильный ответ - а.
При кашле и чиханье, даже разговоре больного туберкулезом лег-
ких в воздухе всегда присутствуют частицы, содержащие при
этом инфекция рассеивается на расстояние 80-100 см. лишь
чиханье способно создать более миллиона частиц диаметром ме-
нее 100 мкм (в среднем около 10 мкм).
14. Правильный ответ - д.
Существует критический диапазон размера частиц, которые обеспечивают максимальное вдыхание и задержку инфекционных частиц в дыхательных путях, что приводит к развитию инфекции. Этот критический диапазон - примерно от 1 до 5 мкм. По экспериментальным данным для возникновения в легких туберкулезной гранулемы при аспирационном заражении необходимо всего
15. Правильный ответ - г.
Развитие активного туберкулеза определяется различными: факторами массивностью инфекции, длительностью контакта с источником инфекции, входными путями инфекции и состоянием резистентности организма человека. Из четырех указанных факторов наибольшее значение придается уровню резистентности организма человека. Установлено, что генерализованные и остропрогрессирующие формы туберкулеза развиваются у ослабленных лиц в условиях голодания или неполноценного питания, во время стихийных бедствий и вооруженных конфликтов, в этом плане туберкулез определяется как биологическими, так и социальными факторами, что заставляет считать туберкулез медико-биологической и социальной проблемой.
16. Правильный ответ - в.
При отсутствии лечения бактериовыделитель может заразить в среднем за год от до человек из своего окружения.
17. Правильный ответ - г.
Макрофаги фиксируют на клеточной мембране, затем погружают (инвагинируют) их в цитоплазму клетки, с образованием фагосомо-лизосомных комплексов, в которых усиливается генерация перекиси водорода при кислородном взрыве и образуется оксид азота по L-аргинин зависимому цитотоксическому пути.
18. Правильный ответ - в.
МБТ, попадая в макрофаги, могут сохраняться в фагосомах и даже продолжать размножение. При этом фагоцитоз может носить незавершенный характер. Установлено, что МБТ могут продуцировать аммиак, который, с одной стороны, способен ингибировать слияние фагосомы с лизосомой, а с другой - путем защелачива-ния содержимого лизосомы снижать его ферментативную активность.
18. Правильный ответ - в.
Повышенная вирулентность МБТ связана с активностью катала-зы/пероксидазы, которая повышает внутриклеточную выживаемость возбудителя, защищая его от механизмов лизиса в макрофаге.
20. Правильный ответ - д.
Повышенная чувствительность замедленного типа (ПЧЗТ), являющаяся основным механизмом в формировании клеточного противотуберкулезного иммунитета она опосредует развитие клеточного иммунитета, направленного на локализацию туберкулезного воспаления в инфицированном организме, и создание приобретенного иммунитета, направленного на уничтожение
21. Правильный ответ - б.
CD4+ лимфоциты в значительном количестве продуцируют ин-который является главным медиатором резистентности к туберкулезу, повышающим переваривающие способности макрофагов в уничтожении МБТ.
22. Правильный ответ - д.
Морфологическим эквивалентом защитных клеточных реакций организма против туберкулезной инфекции является специфическая гранулема. При этом в гранулеме имеются четыре вида клеточных элементов. Центр и главную массу ее составляют эпите-лиоидные клетки. По периферии располагаются лимфоциты и плазматические клетки, а также нейтрофильные лейкоциты. В качестве четвертого элемента присутствуют гигантские многоядерные клетки (типа Пирогова-Лангханса).
23. Правильный ответ - в.
Вторичный иммунодефицит формируется в условиях, когда фоциты не в состоянии оказывать должного сопротивления инфекции и гибнут в большом количестве (апоптоз), что в свою очередь ведет к бурному и массивному размножению микобактериальной популяции и прогрессированию туберкулезного процесса. Повышенный апоптоз, ведущий к уменьшению количества Т-лимфо-цитов, сопровождается значительным снижением синтеза интер-лейкина-2 и интерферона-g.
24. Правильный ответ - д.
При первичном туберкулезе МБТ разносятся по организму с током крови и лимфы, возникает так называемая первичная или облигатная (обязательная) микобактеримия. МБТ оседают и фиксируются в тканях различных органах, где наиболее выражена микроциркуляторная капиллярная сеть. Это капилляры лимфатических узлов, клубочков коркового слоя почек, эпиметафизар-ных отделов трубчатых костей, ампулярно-фимбрионального отдела маточной трубы, увеального тракта глаз и т. п., при этом с момента первичного заражения туберкулезная инфекция носит генерализованный и системный характер, дающий в последующем возможность развития внелегочных форм туберкулеза.
25. Правильный ответ - д.
В развитии вторичного туберкулеза необходимым условием является снижение иммунитета, в том числе специфического, прорыв которого не обеспечивает достаточного контроля за размножающейся микобактериальной популяцией. При этом, как правило, у 90% больных развиваются клинические проявления заболевания и практически отсутствует тенденция к спонтанному излечению, что характерно для первичного туберкулеза.
26. Правильный ответ - в.
Творожистый некроз ткани легкого характеризуется образованием обширных долевых и лобарных поражений легочной ткани, состоящих из сливающихся друг с другом очагов первичного некроза легочной ткани с очень скудной специфической клеточной реакцией. При этом виде специфического воспаления быстро наступает творожистое перерождение жидких и клеточных элементов воспалительного экссудата с образованием вначале сухих, а затем разжиженных некротических масс.
27. Правильный ответ - д.
Наиболее выражена клиническая симптоматика у больных с остропрогрессирующими и распространенными деструктивными формами туберкулеза. При малых формах обычно отмечают ма-лосимптомное течение заболевания.
28. Правильный ответ - д.
Больные туберкулезом предъявляют жалобы на повышение температуры тела, потливость или ночные поты, ознобы, повышенную утомляемость, слабость, снижение или отсутствие аппетита, потерю массы тела, тахикардию. Количественной оценке легче всего поддается температурная реакция, при этом лихорадку отмечают у 40-80% больных.
29. Правильный ответ - д. Бронхолегочные жалобы не являются строго специфичными для туберкулеза легких и могут встречаться и при других воспалительных заболеваниях, таких как пневмония, хроническая обструктив-ная болезнь легких и др.
30. Правильный ответ - б. Количество МБТ, обнаруживаемых при микроскопическом исследовании, является очень важным информационным показателем, так как оно характеризует степень эпидемической опасности больного и тяжесть заболевания.
31. Правильный ответ - а. При постановке пробы Манту с 2 ТЕ ППД-легких развивается только местная, т. е. в месте введения туберкулина (укола), реакция. Эта реакция оценивается является количественной и регистрируется измерением центральной области индурации, т. е. папулы, в миллиметрах.
32. Правильный ответ - д. Туберкулиновая проба - это иммунологическая проба. Выявляет реакцию иммунитета - гиперчувствительность замедленного типа, поэтому регистрируется через 72 часа.
33. Правильный ответ - в. Проба Манту с 2 ТЕ ППД-легких считается положительной при размере папулы 5 мм и более. Точность измерения реакции очень важна. Недопустимы небрежные измерения, учет результата «на глазок».
34. Правильный ответ - а. Проба Манту с 2 ТЕ ставится детям с годовалого возраста и подросткам 1 раз в год, предпочтительно в одно и то же время года.
35. Правильный ответ - в. При туберкулезе наряду с лимфоцитозом (25-60%) отмечается увеличение количества нейтрофилов, в основном при вторичных формах активного специфического процесса (фиброзно-кавернозном и туберкулезе). При первичном туберкулезе с
поражением отмечается им-
36. Правильный ответ - б.
У ребенка наблюдается наличие положительной туберкулиновой чувствительности, которая обусловлена поствакцинальным иммунитетом. Имеется тенденция к уменьшению результата пробы, которая через 3-4 года после введения вакцины станет сомнительной и отрицательной, в том случае, если ребенок не заразится М БТ естественным путем.
37. Правильный ответ - д.
УЗ И - метод неинвазивного дополнительного обследования, используемый для диагностики плеврита и выявления субплевраль-но расположенных округлых образований.
38. Правильный ответ - в.
Обнаружение М БТ позволяет установить этиологический диагноз без особых затруднений.
39. Правильный ответ - а.
Специфическое туберкулезное воспаление имеет разнообразные рентгенологические проявления - от одиночных или множественных сливных очагов, округлых инфильтратов и перециссуритов до долевых туберкулезных пневмоний. Однако большинству присуща локализация процесса в 1 -2 и 6 сегментах легких.
40. Правильный ответ - в.
В случае сомнительной активности туберкулезных изменений. При этом назначают химиотерапию 4 препаратами - изониазидом, рифампицином пиразинамидом, этамбутолом. Через 2 месяца повторяют рентгенологическое обследование. При заболевании туберкулезной этиологии наблюдается частичное рассасывание воспалительных изменений.
41. Правильный ответ - г.
Химиотерапию проводят 4 противотуберкулезными препаратами (изониазид, рифампицин, пиразинамид и этамбутол). В таких случаях через 2 месяца необходимо повторное рентгенологическое исследование. При заболевании туберкулезной этиологии отмечается частичное или полное рассасывание воспалительных изменений.
42. Правильный ответ - в.
Дополнительным методом исследования при диагностике туберкулеза является бронхоскопия, так как обнаружение в биоптате казеозных масс и клеточных элементов специфической туберкулезной гранулемы позволяет морфологически верифицировать туберкулез легких.
43. Правильный ответ - в.
Обнаружение в биоптате специфических элементов туберкулезной гранулемы (казеоз, эпителиоидные и многоядерные клетки) позволяет морфологически верифицировать туберкулез легких и своевременно начать противотуберкулезное лечение.
44. Правильный ответ - а.
Выявление больных туберкулезом осуществляется медицинским персоналом лечебных учреждений общей медицинской сети (ЛУ ОМС) при обследовании пациентов, обратившихся за медицинской помощью, а также при плановых профилактических обследованиях определенных групп населения.
45. Правильный ответ - а.
Периодические флюорографические обследования населении 1 раз в 1-2 года позволяют выявлять туберкулез органов дыхания на сравнительно ранних этапах развития, что в значительной степени повышает вероятность полного клинического излечения.
46. Правильный ответ - г.
Лица, находящиеся в контакте с больным туберкулезом. Особенно опасен семейный контакт или производственный контакт с бактериовыделителем.
47. Правильный ответ - д.
У пациентов из групп р иска в виду снижения резистентности организма туберкулез может развиваться очень быстро (возможно в течение недель, но наверняка в течение месяцев), поэтому оптимальный срок периодичности флюорографических обследований должен не превышать 6 месяцев.
48. ответ - г.
При щадящем режиме во всех случаях рекомендуется утренняя гигиеническая гимнастика, а при наличии показаний - лечебная физкультура по методике с ослабленной нагрузкой. Длительность его в условиях стационарного лечения должна составлять не более 1 - 1,5 месяцев.
49. Правильный ответ - б.
При тренировочном режиме - 2700-2900 ккал/день (11,3- 12,2 МДж).
50. Правильный ответ - д.
Наиболее эффективными препаратами группы ГИНК являются изониазид и фенозид.
51. Правильный ответ - г.
Суточная доза рифампицина 10 мг/кг массы тела больного явля-
ется единой для ежедневного и приема ле-
карстве (3 раза в неделю).
52. Правильный ответ - г.
Суточная доза стрептомицина составляет 8 мг/кг массы тела пожилого больного, что в два раза меньше стандартной суточной дозы, что связано с большим числом побочных реакций нейро-токсического, сосудистого и гепатотоксического действия.
53. Правильный ответ - в.
Необходимо увеличение дозы рифампицина или его замена на ри-фабутин.
54. Правильный ответ - г.
Фторхинолоны как противотуберкулезные препараты применяются с 1980-х годов.
55. Правильный ответ. - д.
Больные с моножественно лекарственно-устойчивыми МБТ, устойчивыми к сочетанию основных и резервных противотуберкулезных препаратов, имеют неблагоприятный прогноз и высокую летальность ввиду того, что специфических препаратов для их лечения нет.
56. Правильный ответ - б.
Первичная лекарственная устойчивость определяется у пациентов, принимавших противотуберкулезные препараты менее 1 месяца. В данном случае подразумевается, что больной заразился этими штаммом МБТ. В России в настоящее время частота первичной множественной лекарственной устойчивости по отдельным регионам составляет
57. Правильный ответ - а.
Токсические реакции зависят от дозы и длительности применения препарата, от характера его инактивации и элиминации, а также от особенностей взаимодействия с другими препаратами в организме, от функционального состояния основных звеньев дезинтоксикаци-онной системы организма (влияние возраста, сопутствующих заболеваний, предшествующего медикаментозного лечения).
58. Правильный ответ - а.
Аллергические реакции являются индивидуальным ответом организма больного на антиген-препарат или продукты его катаболизма. Аллергическое состояние может развиться вслед за первым введением лекарств, но обычно обусловливается постепенной сенсибилизацией при его повторных приемах. Возникновение реакции не зависит от дозы препарата, но степень усиливается от ее повышения. Все противотуберкулезные препараты могут оказаться причиной сенсибилизации организма, но в наибольшей степени этими свойствами обладают антибиотики.
59. Правильный ответ - а.
I режим химиотерапии назначают впервые выявленным больным туберкулезом легких с выделением МБТ, обнаруженными при микроскопии мокроты, и впервые выявленным больным распространенными (более 2-х сегментов) формами туберкулеза легких (диссеминированный туберкулез, обширный экссудативный или двухсторонний плеврит), но при отрицательных данных микроскопии мокроты.
60. Правильный ответ - в.
Пб режим назначается больным, у которых имеются эпидемиологические (региональный уровень первичной множественной лекарственной устойчивости МБТ, превышающий 5%), анамнестические (контакт с известными диспансеру больными, выделяющими множественно лекарственно-устойчивые МБТ), социальные (лица БОМЖ, освобожденные из пенитенциарных учреждений) и клинические (больные с неэффективным лечением по I, На, Ш режиму химиотерапии, с перерывами в лечении, с распространенными формами туберкулеза, как с впервые выявленными, так и рецидивами туберкулеза легких) показания.
Правильный ответ - б. Больной фиброзно-кавернозным туберкулезом, как правило, выделяет множественно лекарственные устойчивые МБТ, поэтому пациенты, контактирующие с таким больным, должны лечиться в режиме химиотерапии Пб для больных с высоким риском развития лекарственной устойчивости.
62. Правильный ответ - д.
Перед началом химиотерапии необходимо обязательно уточнить лекарственную чувствительность МБТ по данным предшествующих исследований, а также в процессе обследования больного перед началом лечения. Поэтому желательно применение ускоренных методов бактериологического исследования полученного материала и ускоренных методов определения лекарственной чувствительности, в том числе используя систему
63. Правильный ответ - д.
При выявлении лекарственной устойчивости МБТ к изониазиду или рифампицину в режим химиотерапии никогда нельзя добавлять 1 противотуберкулезный препарат из-за риска развития множественной лекарственной устойчивости.
64. Правильный ответ - д.
Длительное назначение резервных противотуберкулезных препаратов обусловлено их низкой активностью и бактериостатическим эффектом.
65. Правильный ответ - д.
Показанием к назначению кортикостероидов являются формы туберкулеза с выраженной экссудативной реакцией - острый ми-лиарный туберкулез, инфильтративный туберкулез типа лобита, казеозная пневмония, туберкулезный менингит, экссудативный плеврит, перитонит, перикардит, полисерозит, туберкулезное поражение бронхов. Их также можно применять при побочном действии противотуберкулезных препаратов, связанных с токсическими и аллергическими реакциями при поражениях печени, почек, кожных покровов.
66. Правильный ответ - г.
В связи с выявленными в последние годы признаками иммунодефицита у больных туберкулезом, особенно при развитии тяжелых форм заболевания, в качестве патогенетического средства все шире применяют иммуномодуляторы (тактивин, тималин, лева-мизол, диуцифон и др.).
Свернуть
Особенную тревогу у врачей фтизиатров вызывает широкое распространение серьезной формы заболевания под названием множественная лекарственная устойчивость при туберкулезе или МЛУ-ТБ. Что это значит? Ответ можно найти в предлагаемой статье.
Что такое МЛУ?
Данный вид характеризуется отсутствием эффективности использования самых действенных препаратов, способных противостоять пагубному воздействию на организм палочки Коха.
Основным фактором, способствующими развитию устойчивости микобактерий туберкулеза к сильнейшим препаратам, используемым при лечении инфекции, считается нарушение пациентами рекомендаций относительно приема лекарств. Это нерегулярность или неправильная дозировка.
В большинстве случаев подобное отношение приводит к ситуации, когда самые эффективные медикаментозные средства не справляются с болезнетворными бактериями, что ставит под угрозу жизнь пациента.
Причины
Способность бактерий туберкулеза противостоять воздействию исключительно сильных лекарственных препаратов обуславливается многообразием факторов, основным их которых является неверный подход к их использованию.
Формирование устойчивости микобактерий является результатом их хромосомной мутации, вызванной отсутствием чувствительности некоторых из них к лекарственным средствам или нарушением концентрации используемого препарата. В этом случае погибают не все бактерии, выжившие наследуют резистентность к препаратам.
Среди других факторов, способствующих приобретению микобактериями устойчивой формы, следует отметить:
- Отсутствие своевременного выявления наличия у пациента первичной устойчивости к препаратам.
- Преждевременное прекращение лечения, прерывание курса.
- Несвоевременный и нерегулярный прием лекарства.
- Уменьшение предписанной дозировки.
- Низкое качество препаратов.
- Отсутствие проверки сочетаемости и эффективности используемых медикаментозных средств.
- Допущение ошибки в выборе схемы лечения.
Возникновение перекрестной резистентности, когда устойчивость к одному из используемых препаратов может спровоцировать отсутствие чувствительности и к другому.
Устойчивость возбудителя инфекции зачастую является следствием халатного отношения пациента, прекращающего прием медикаментов при улучшении самочувствия до окончания полного курса терапии. Рецидив туберкулеза способствует его прогрессированию, но уже в устойчивой форме.
Среди других причин следует отметить ошибки врачей и отсутствие необходимых препаратов.
Виды
Классификация проявления устойчивости возбудителя инфекции к медикаментозному лечению выделяет три категории. В каждой из них рассматриваются определенные химиопрепараты, на которые у микобактерий вырабатывается резистентность (устойчивость).
МЛУ-ТБ
Отличительной особенностью туберкулеза с множественной лекарственной устойчивостью является отсутствие возможности вылечить его сильнейшими препаратами, эффективными при терапевтическом воздействии на обычный туберкулез, хотя возбудителем инфекции является одна и та же палочка Коха.
Это основные и наиболее мощные противотуберкулезные химиопрепараты первого ряда — Рифампицин и Изониазид. Они признаны самыми эффективными в борьбе с туберкулезом, однако при наличии МЛУ они не могут уничтожить палочку Коха даже без проявления устойчивости к препаратам другого ряда.

Множественная лекарственная устойчивость с трудом поддается лечению, что объясняется исключительной агрессивностью и живучестью микобактерий, утративших чувствительность к препаратам противотуберкулезной направленности.
ШЛУ-ТБ
В отличие от МЛУ при туберкулезе с широкой лекарственной устойчивостью наблюдается отсутствие чувствительности не только к Иониазиду и Рифампицину, но и ко всем представителям фторхинолонов, относящихся к препаратам второго ряда противотуберкулезных средств. Кроме этого данная форма туберкулеза обладает устойчивостью к медикаментам 3 ряда (Капреомицину, Амикацину и Канамицину), что в значительной степени затрудняет выбор тактики лечения.
Абсолютно устойчивый туберкулез
Следует признать, что данный термин наиболее точно характеризует туберкулез, сопровождающийся проявлением резистентности палочки Коха ко всем противотуберкулезным препаратам.
Подобное отсутствие чувствительности микобактерий возникает вследствие мутации или упущений в ходе лечения патологии. В этом случае лечение пациента весьма затруднено и зачастую становится причиной летального исхода.
Другие виды
Кроме перечисленных видов заболевания необходимо учитывать возможность проявления:
- Первичной устойчивости микобактерий, при которой инфицирование пациента произошло от больного, являющегося носителем устойчивой бактерии.
- Приобретенной устойчивости, возникшей через определенный период после начала терапевтического курса.
- Монорезистентности – к одному какому-то лекарству.
- Полирезистентности – одновременно к нескольким препаратам.
Мультирезистентный туберкулез, сопровождающийся повышенной устойчивостью микобактерий к лекарственным противотуберкулезным средствам, характеризуется не только слабой эффективностью терапевтического воздействия на возбудителя инфекции, но и высокой вероятностью летального исхода. Лечение такой формы заболевания отличается сложностью и длительностью.
О подозрении на множественную лекарственную устойчивость можно говорить в следующих ситуациях:
- если не наблюдается улучшение от терапевтического лечения;
- если туберкулезный процесс прогрессирует, несмотря на регулярный прием лекарственных средств;
- если продолжается выделение микобактерии.
На начальном этапе туберкулеза определить наличие лекарственно устойчивой формы удается только с помощью специального тестирования.
Определение вида МЛУ является важным этапом комплексного подхода и определяющим фактором в выборе схемы терапии.

Основные принципы лечения
Медикаментозное терапевтическое воздействие предусматривает использование различных комбинаций химиопрепаратов 1 и 2 ряда. Кроме этого при тяжелом течении заболевания допускается использование лекарственной группы, относящейся к 3 ряду.
Среди непреложных принципов воздействия лекарственных средств на туберкулезную палочку следует учитывать следующие:
- адекватный выбор средств;
- комплексный подход к использованию препаратов;
- непрерывность терапевтического курса;
- систематический контроль медицинских работников над соблюдением правил приема лекарственных средств.
Кроме этого лекарственно устойчивый туберкулез предусматривает проведение терапевтического курса согласно стандартным схемам с учетом подбора эффективных средств, дозировки, соответствующего режима и продолжительности лечения.
Принципиально важными требованиями при лечении пациентов с множественной лекарственной устойчивостью становятся:
- Применение единовременного использования 5 противотуберкулезных препаратов, не утративших чувствительность к выявленным микобактериям. В зависимости от степени тяжести допускается назначение дополнительных средств.
- Использование максимальной дозировки с целью эффективного воздействия на бактерии туберкулеза.
- Обязательное продолжение курса антибиотиков на протяжении полугода после момента, свидетельствующего об отсутствии микобактерий в организме пациента.
- Общая продолжительность лечения после выздоровления составляет от полутора года до двух лет, несмотря на полученные отрицательные результаты.
- В отличие от обычной формы туберкулеза, предусматривающей одноразовое применение медикаментов в сутки, больной с МЛУ при туберкулезе получает лекарства в 2 или 3 приема на протяжении 24 часов. Процедура проходит под обязательным контролем медиков.
Обязательным условием является строгий учет пациентов и их официальное согласие на предложенную схему терапии.
Побочные действия
Использование лекарств из 2 и 3 ряда провоцирует проявление большого количества побочных эффектов. Это:
- общее недомогание;
- позывы к рвоте, тошнота;
- плохой аппетит;
- снижение слуха;
- присутствие боли в суставах;
- нервное напряжение, тревожность, головокружение.
Подобные симптомы характерны в основном для начального этапа лечебного курса. Но оставлять их без внимания не следует. Необходимо сообщить об этом врачу. Он скорректирует дозировку или подберет аналогичный препарат.
Прерывать лечение не следует, так как это приведет к еще большей агрессивности и устойчивости микобактерий, и лечить туберкулез будет еще сложнее.
Последствия и осложнения
Характерная ошибка, приводящая к устойчивости туберкулезной палочки, — это ситуация, при которой пациент при улучшении состояния считает, что окончательно вылечился и прекращает прием лекарств.
В результате возобновление лечебного курса не дает положительных результатов вследствие развития мультирезистентной устойчивости микобактерий.
Подобрать эффективные препараты в таком случае уже не представляется возможным. Это вызывает необходимость хирургического удаления пораженного органа.
Исход операции предсказать трудно. При этом после нее сохраняется необходимость в дальнейшем терапевтическом воздействии во избежание рецидива туберкулезного процесса. Однако подбор действенных препаратов в значительной мере осложняется и даже становится практически невозможным, что приводит к неминуемой смерти пациента.
Предупредить вероятность развития МЛУ при туберкулезе удается только в случае неукоснительного следования основным принципам лечения. С этой целью пациенту следует настроиться на сложный и длительный курс терапии, а также строгое выполнение указаний врача.
О.А. Воробьева (Иркутский институт усовершенствования врачей)
Российская Федерация относится к числу стран с высоким уровнем заболеваемости туберкулезом, хотя с 2003 года стала отмечаться некоторая тенденция к стабилизации эпидемической ситуации. Наиболее неблагополучной по туберкулезу была в 1999 году территория Западной Сибири, где показатели заболеваемости занимали первое место среди всех субъектов России. Неуклонный рост показателей заболеваемости туберкулезом представляет значительную угрозу для общества.
Однако еще более серьезной для современной фтизиатрии является проблема лекарственной устойчивости (ЛУ) возбудителя туберкулеза, поскольку является одним из факторов, ограничивающих эффективность антибактериальной терапии. Лекарственная устойчивость - природная или приобретенная способность возбудителя заболевания сохранять жизнедеятельность при воздействии на него лекарственных препаратов.
Согласно классификации ВОЗ (1998), микобактерии туберкулеза (МБТ) могут быть:
- монорезистентные - устойчивые к одному противотуберкулезному препарату;
- полирезистентные - к двум и более противотуберкулезным препаратам (ПТП);
- множественно лекарственно резистентные - устойчивые как минимум к сочетанию изониазида и рифампицина, независимо от наличия или отсутствия устойчивости к другим ПТП.
В международной практике выделяют понятия первичной и вторичной лекарственной устойчивости (ЛУ). В первом случае, это устойчивость, обусловленная инфицированием штаммом микобактерий, выделенных больным с приобретенной устойчивостью. Во втором - устойчивость, возникшая в результате нерациональной химиотерапии. Выделяют так же понятия «истинной», «ложной», «скрытой» и «полной» лекарственной устойчивости. Истинная резистентность чаще выявляется у постоянных бактериовыделителей. При истинной лекарственной устойчивости одна МБТ устойчива к нескольким антибактериальным препаратам (АБП). Чаще наблюдается ложная резистентность, когда одни МБТ устойчивы к одним препаратам, а другие
- к другим.
Вопрос скрытой лекарственной устойчивости требует дальнейшего изучения. Достоверная идентификация этого вида лекарственной устойчивости возможна лишь при микробиологическом исследовании каверн, т.к. при бактериологическом исследовании мокроты у данных больных обнаруживают лекарственно-чувствительные МБТ. Последний вид лекарственной устойчивости, встречается довольно редко. В настоящее время, когда для лечения применяется много новых резервных препаратов, необходимо помнить о наличии перекрестной лекарственной устойчивости.
Появление первых антибиотико-резистентных штаммов микобактерий туберкулеза (МБТ) связывают с открытием в 1943 г. и широким применением стрептомицина как эффективного противотуберкулезного препарата. Уже первые системные данные о распространенности первичной лекарственной устойчивости к изониазиду и стрептомицину были получены в 50-е годы за рубежом при проведении эпидемиологических исследований. Были выделены страны с высоким до 9,4% (Япония и Индия) и низким - от 0,6 до 2,8% (США и Великобритания) уровнем лекарственной устойчивости к этим двум препаратам. При этом показатели устойчивости к стрептомицину были несколько выше устойчивости к изониазиду.
В России подобные исследования по изучению уровня лекарственной устойчивости к стрептомицину, ПАСК, препаратам группы ГИНК стали проводиться с середины 50-х годов Центральным НИИ туберкулеза. Полученные за шестилетний период (1956-1963 гг.) данные свидетельствовали об изменении за этот период структуры лекарственной устойчивости в сторону уменьшения штаммов МБТ, устойчивых к стрептомицину, и увеличения доли резистентности к препаратам группы ГИНК, а так же к 2 и 3 препаратам одновременно.
Открытие и внедрение в практику новых противотуберкулезных препаратов (в 50-х годах - препараты группы ГИНК, пиразинамид, циклосерин, этионамид, канамицин и каприомицин; в 60-х - рифампицин и этамбутол; в 80-х - препараты группы фторхинолонов), а так же использование схем химиотерапии, включающих одновременное применение 4-5 ПТП, позволяло хотя бы временно решать проблему лекарственной устойчивости. Возможно, поэтому до конца 80-х годов суммарные показатели лекарственной устойчивости в России сохранялись на относительно невысоком уровне, а ее колебания были незначительными.
Крупномасштабное изучение тенденции развития лекарственной устойчивости в России за 20-летний период (1979-1998 гг.) к ПТП показало, что самый высокий уровень ЛУ за эти годы был зарегистрирован к стрептомицину (37%) и изониазиду (34%). Несколько ниже были показатели устойчивости к рифампицину (21%), канамицину (19%), этионамиду и этамбутолу (16%). Самый низкий уровень лекарственной устойчивости наблюдался к ПАСК (8%). Данные этого исследования хорошо согласуются с тем, что такие препараты, как стрептомицин и изониазид, имеющие самые высокие показатели лекарственной устойчивости, имели наиболее длительную историю применения, а ПАСК - не входил в стандартные схемы химиотерапии. Синтезированный одним из последних, этамбутол оставался наиболее «надежным» препаратом, к которому резистентность возбудителя держалась на относительно невысоком уровне.
Анализ данных лекарственной устойчивости к стрептомицину, изониазиду, рифампицину и этамбутолу (1991-2001 гг.), проводимый на Северо-Западе России, показал, что уровень устойчивости к последнему за этот период вырос более чем в 2 раза, хотя и продолжает оставаться ниже по сравнению с остальными препаратами. Уровень устойчивости к рифампицину лишь немногим уступает устойчивости изониазиду, а частая ассоциация лекарственной устойчивости этих двух препаратов делает рифампицин маркером множественной лекарственной устойчивости (МЛУ).
Являясь одним из основных препаратов, воздействующих на активно размножающуюся фракцию МБТ, рифампицин входит в состав всех схем химиотерапии, применяемых для лечения вновь выявленных больных активным туберкулезом, что делает особенно актуальной проблему мультирезистентности. Обсуждаются тревожные данные о вспышках мультирезистентного туберкулеза в тесных коллективах. С увеличением МЛУ связывают рост смертности от туберкулеза в мире. Наряду с этим имеются сведения о том, что больные, выделяющие микобактерии, устойчивые к изониазиду и рифампицину, являются менее заразными, чем другие пациенты.
Рост общей частоты лекарственной устойчивости, наблюдаемый при всех локализациях туберкулеза, сопровождается значительным утяжелением ее структуры за счет снижения монорезистентности и увеличения количества полирезистентных форм. Показатели лекарственной устойчивости МБТ распределены неравномерно по всей территории России и колеблются в достаточно широком диапазоне. Уже с конца 90-х годов отмечено отчетливое увеличение удельного веса показателя первичной лекарственной устойчивости от 18 до 61% по различным регионам России, показатели же вторичной лекарственной устойчивости практически повсеместно превышают 50-70, достигая в отдельных областях до 80-86%. Резистентность МБТ к основным препаратам более характерна для впервые выявленных больных с ограниченной распространенностью процесса. Развитие резистентности МБТ к сочетанию основных и резервных препаратов - для рецидивов и хронического течения туберкулеза легких.
Частота встречаемости МЛУ у вновь выявленных больных являются невысокой (2-10%), поэтому не может оказывать серьезного влияния на основные эпидемиологические показатели по туберкулезу. Большее эпидемиологическое значение имеет вторичная резистентность. Воздействие противотуберкулезных средств рано или поздно приводит к созданию популяции высокоустойчивых к лекарственному воздействию бактерий. Существует достаточно большая вероятность того, что массивное лекарственное воздействие не приводит к полной элиминации патогена из организма человека, а является дополнительным фактором его направленной эволюции.
Причины формирования лекарственной устойчивости различны . В индустриально развитых странах это может быть связано с врачебными ошибками при разработке схем лечения; в слаборазвитых - с недостатком финансирования и применением менее эффективных, более дешевых лекарственных препаратов. Группами риска по формированию лекарственно-устойчивого туберкулеза являются больные, нарушающие режим лечения и прерывающие основной курс лечения самовольно, либо по причине аллергических или токсических осложнений; злоупотребляющие алкоголем, наркотическими средствами; лица, контактирующие с больным туберкулезом, выделяющим лекарственно-устойчивые МБТ.
Лекарственная устойчивость формируется в результате одной или нескольких спонтанных мутаций в независимых генах МБТ, происходящих преимущественно при применении неадекватных схем химиотерапии. Эмпирическое назначение стандартной комбинации химиопрепаратов при наличии первичной лекарственной устойчивости, с последующей их заменой, а также прерывистые курсы терапии приводят к накоплению мутаций и являются основной причиной развития мультирезистентности.
Подобные мутации могут встречаться в микобактериальной популяции еще до контакта МБТ с противотуберкулезными препаратами. Частота возникновения спонтанных мутаций природных штаммов МБТ, влекущих за собой развитие лекарственной устойчивости к антибактериальным препаратам, вариабельна. В литературе описывается феномен кросс-резистентнтности - состояния, при котором наблюдается лекарственная устойчивость, генетически обусловленная к нескольким препаратам одновременно. Кросс-резистентность характерна для изониазида и этионамида, рифампицина и его производных, а также стрептомицина, канамицина, амикацина. Бурное развитие молекулярной генетики, наблюдаемое в последние годы, открыло возможности для изучения генов МБТ, контролирующих лекарственную устойчивость и механизмов ее развития. Наиболее полно изучены гены и механизмы формирования лекарственной устойчивости к препаратам первого ряда.
Устойчивость к изониазиду кодируется несколькими генами : kat G - осуществляет контроль клеточной каталазно-пероксидазной активности; inh A - контроль синтеза миколитических кислот; kas A - контроль протеиновых взаимодействий. Устойчивость к рифампицину связывают с единственным геном rpo B, контролирующим процесс транскрипции (синтеза РНК). Rps L и rrs - гены, кодирующие процессы трансляции и связанные с синтезом клеточного белка. Мутации в этих генах являются ключевыми при формировании устойчивости к стрептомицину и канамицину. Устойчивость к этамбутолу кодируется геном emb B, контролирующим процесс нормального построения клеточной стенки при конверсии глюкозы в моносахариды. Ген pcn A - отвечает за работу фермента энзимпиразимидазы, который осуществляет трансформацию пиразинамида в активный комплекс (пиразинодоновую кислоту).
Попадая в организм, препарат или его метаболиты вмешиваются в цикл работы микобактериальной клетки, нарушая ее нормальную жизнедеятельность. В результате приобретения клеткой генов лекарственной устойчивости метаболиты препарата становятся неактивными по отношению к своим мишеням, что и приводит к развитию картины лекарственно-устойчивого туберкулеза.
Влияние характера лекарственной резистентности на течение и исход заболевания является несомненным . Остро текущие формы туберкулеза легких в большинстве случаев развиваются на фоне множественной лекарственной устойчивости и сопровождаются большой распространенностью специфического и неспецифического воспаления в легочной ткани, отставанием темпов репарации очагов поражения и значительными нарушениями в иммунном статусе. Наличие резистентности к 1-2 препаратам практически не отражается на результатах лечения. Устойчивость к 3 и более препаратам, а особенно МЛУ, затрудняет процесс лечения и снижает его эффективность. Это выражается в замедлении темпов негативации мокроты, рассасывания инфильтративных и ликвидации деструктивных изменений, в связи с чем, наблюдается большая нуждаемость в хирургическом лечении.
Проблема повышения эффективности профилактических мероприятий, для предотвращения заражения лекарственно-устойчивым туберкулезом вызывает широкий интерес. Заболеваемость туберкулезом контактных лиц в семьях больных, выделяющих лекарственно-устойчивые штаммы МБТ, в 2 раза выше по сравнению с заболеваемостью контактов в семьях бактериовыделителей лекарственно-чувствительных МБТ.
Предпринимаются попытки совершенствования профилактических и лечебных мероприятий. Подтверждено совпадение спектра лекарственной устойчивости МБТ заболевших из контакта детей и взрослых с источником инфекции. Предпринимаются попытки разработки модели больного с лекарственно-устойчивым туберкулезом легких. Получен тренд линейности между возрастом и резистентностью. Дальнейшее изучение проблемы лекарственной устойчивости создает перспективные возможности для ограничения туберкулезной инфекции.
Лекарственная устойчивость МБТ и режимы химиотерапии туберкулеза Лекарственная устойчивость микобактерий туберкулеза и режимы химиотерапии туберкулеза, а также применение продуктов на основе личинок восковой моли для лечения туберкулеза. Администратор сайт
Лекарственная устойчивость МБТ и режимы химиотерапии туберкулеза
Лекарственная устойчивость микобактерий туберкулёза (МБТ)
Лекарственная устойчивость микобактерий туберкулёза (МБТ) – одна из самых главных причин неэффективности химиотерапии.
Основным фактором риска развития лекарственной устойчивости микобактерий туберкулёза - является неэффективное лечение, особенно прерванное или незаконченное.
Лекарственную устойчивость подразделяют на:
- первичную устойчивость
, отмечающуюся у больных, ранее не принимавших химиопрепараты или принимавших в течение месяца или менее;
- приобретенную устойчивость
, развившуюся во время лечения, наблюдается у больных, имевших в начале лечения чувствительные МБТ и ставшие устойчивыми через 6 месяцев.
Лекарственная устойчивость микобактерий туберкулёза может быть:
монорезистентной
– устойчивость к одному из противотуберкулёзных препаратов (при комплексной терапии встречается редко)
;
полирезистентной
– устойчивость к двум и более препаратам, например: одновременную устойчивость к изониазиду и рифампицину следует трактовать как полирезистентность (или множественную лекарственную устойчивость)
.
В последние годы в связи с ухудшением эпидемической ситуации существенно увеличилось число больных, выделяющих штаммы МБТ, устойчивые к основным противотуберкулёзным препаратам.
Прием экстракта личинок восковой моли помогает подавить лекарственную устойчивость микобактерий туберкулёза к различным противотуберкулёзным препаратам (в том числе и полирезистентную/множественную
).
Экстракт личинок восковой моли повышает эффективность химиотерапии и тем самым позволяет уменьшить лекарственную нагрузку на больного.
Режимы химиотерапии туберкулёза
В связи с разным состоянием бактериальной популяции на разных этапах течения болезни в процессе химиотерапии весь период лечения химиопрепаратами делят на два этапа (или фазы).
Первый этап
характеризуется проведением интенсивной насыщенной химиотерапии четырьмя-пятью противотуберкулёзными препаратами. Его назначение заключается в подавлении размножающейся бактериальной популяции и уменьшении ее количества.
Второй этап
- менее интенсивная химиотерапия. Ее назначение состоит в воздействии на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм микобактерий. На этом этапе главными задачами являются предупреждение размножения оставшихся микобактерий, в том числе резистентных штаммов микобактерий.
Приказ Минздрава РФ № 109 от 21 марта 2003 года, утверждает несколько стандартных схем лечения туберкулёза: I, IIа, IIб, III и IV. Согласно этому приказу лечение подразделяется на две фазы: интенсивную и пролонгированную фазу лечения.
1 режим (1 категория больных)
- больные с впервые выявленным бациллярным туберкулёзом легких разной протяженности;
- больные распространенными формами впервые выявленного туберкулёза легких, но без деструкции и бактериовыделения (милиарным туберкулёзом, диссеминированным туберкулёзом легких, полисерозитом, экссудативным плевритом) ;
- больные тяжелыми формами внелегочного туберкулёза (менингитом, осложненным туберкулёзом позвоночника, осложненным туберкулёзом костей и суставов, распространенным и/или осложненным туберкулёзом мочеполовой системы, распространенным и/или осложненным туберкулёзом женских гениталий, распространенным и/или осложненным абдоминальным туберкулёзом, осложненным туберкулёзным перикардитом, туберкулёзом надпочечников с гормональной недостаточностью) ;
- больные с сочетанием активного внелегочного туберкулёза любой локализации и туберкулёза органов дыхания любой активности.
В фазе интенсивной терапии назначают четыре основных препарата: изониазид, рифампицин, пиразинамид и стрептомицин или этамбутол. Интенсивную фазу химиотерапии продолжают не менее двух месяцев. За этот срок больной должен принять 60 доз комбинации из четырех основных препаратов. В случае пропуска приема полных доз длительность фазы интенсивной терапии увеличивают до 60 доз.
Через 2 месяца от начала лечения вопрос о переходе ко второму этапу решает экспертная комиссия на основании данных рентгенологического и микробиологического исследований.
При сохраняющемся после двух месяцев химиотерапии бактериовыделении фазу интенсивной терапии можно продолжить еще на месяц (30 доз) до получения данных о лекарственной чувствительности возбудителя. В зависимости от результата проводят коррекцию химиотерапии и продолжают фазу интенсивной терапии. При невозможности исследования лекарственной чувствительности и/или при отрицательной клинико-рентгенологической динамике процесса после трех месяцев химиотерапии больного направляют в вышестоящее учреждение для исследования лекарственной чувствительности и определения дальнейшей тактики лечения. В ожидании результатов лечение проводят в соответствии с интенсивной фазой терапии.
При тяжелом и осложненном течении туберкулёза любой локализации продолжительность фазы интенсивной терапии может быть увеличена.
При отрицательных результатах микроскопии мокроты после двух месяцев химиотерапии и положительной клинико-рентгенологической динамике переходят к фазе продолжения химиотерапии.
В фазе продолжения терапии назначают два основных препарата изониазид и рифампицин - в течение 4 месяцев (при туберкулёзе органов дыхании) или в течение 6 месяцев (при внелегочном туберкулёзе) ежедневно или в интермиттируюшем режиме (3 раза в неделю).
Во второй фазе лечения применяют изониазид и рифампицин в течение 4 месяцев ежедневно или интермиттирующим методом 3 раза в неделю. Как альтернативная комбинация в фазе долечивания может использоваться сочетание изониазида и этамбутола при их ежедневном приеме в течение 6 мес.
Интерминирующий режим назначают больным при амбулаторном проведении фазы продолжения терапии, при хронической почечной и печеночной недостаточности, больным с токсическими реакциями и неудовлетворительной переносимостью лечения, преклонного возраста.
2a режим (2а категория больных)
IIa режим химиотерапии назначают
при повторном курсе химиотерапии после перерыва в лечении или по поводу рецидива при невысоком риске лекарственной устойчивости микобактерий туберкулёза.
В фазе интенсивной терапии назначают 5 основных препаратов: изониазид, рифампицин, пиразинамид, этамбутол и стрептомицин. Через 2 месяца (60 принятых суточных доз) терапию продолжают четырьмя препаратами (изониазидом, рифампицином, пиразинамидом, этамбутолом) в течение еще одного месяца (30 доз). Общая длительность интенсивной фазы - не менее трех месяцев (90 суточных доз комбинации лекарств). В случае пропуска приема полных доз длительность интенсивной фазы увеличивают до приема 90 доз.
Через 3 месяца от начала фазы интенсивной терапии, вопрос о переходе ко второму этапу лечения решает комиссия на основании данных клинико-рентгенологического и микробиологического исследований.
При отрицательных результатах микроскопии мокроты через 3 месяца химиотерапии и положительной клинико-рентгенологической динамике приступают к фазе продолжения химиотерапии. К этому сроку, как правило, получают данные о лекарственной чувствительности микобактерий туберкулёза, которые могут потребовать коррекции химиотерапии.
При сохранении бактериовыделения и невозможности исследования лекарственной чувствительности микобактерий туберкулёза и/или при отрицательной клинико-рентгенологической динамике процесса через 3 месяца больного направляют в вышестоящее учреждение для исследования лекарственной чувствительности и определения дальнейшей тактики ведения. До получения результатов лечение проводят как в интенсивной фазе терапии.
При чувствительности микобактерий туберкулёза к основным химиопрепаратам в фазу продолжения терапии еще в течение 5 месяцев назначают изониазид, рифампицин и этамбутол ежедневно в интермиттирующем режиме (3 раза в неделю). Общая продолжительность терапии 8 месяцев.
2б режим (2б категория больных)
IIб режим химиотерапии назначают
больным с высоким риском лекарственной устойчивости микобактерий до получения результатов микробиологического исследования.
К 2б категории относятся:
- больные, у которых отсутствует эффект от химиотерапии либо обострен или прогрессирует процесс на фоне лечения;
- больные, не получавшие ранее противотуберкулёзные препараты, но у которых имеются веские основания для предположений о лекарственной устойчивости по анамнестическим и/или клиническим данным (контакт с больными, выделяющими микобактерий туберкулёза с множественной лекарственной устойчивостью, остропрогрессирующее течение) .
В фазе интенсивной терапии в течение 3 месяца назначают комбинацию из четырех основных препаратов (изониазида, рифампицина/рифабутина, пиразинамида, этамбутола) и двух-трех резервных (в зависимости от данных о лекарственной устойчивости по региону).
Дальнейшее лечение корректируют на основании данных о лекарственной чувствительности микобактерий туберкулёза и проводят в соответствии с режимами I, IIа или IV.
3 режим (3 категория больных)
III режим химиотерапии назначают:
- впервые выявленным больным без бактериовыделения;
- больным с малыми (ограниченными) и неосложненными формами туберкулёза;
- больным с туберкулёзом внутригрудных лимфатических узлов (поражение одной-двух групп лимфатических узлов) , ограниченным плевритом при отсутствии кислотоустойчивых бактерий при микроскопии мазка мокроты или иного диагностического материала;
- больным менее тяжелыми формами внелегочного туберкулёза (неосложненным туберкулёзом позвоночника, костей и суставов, мочеполовой системы, ограниченным и неосложненным туберкулёзом женских гениталий, туберкулёзом периферических лимфатических узлов, ограниченным и неосложненным абдоминальным туберкулёзом, туберкулёзом кожи, глаз, ограниченным и неосложненным туберкулёзным перикардитом, туберкулёзом надпочечников без явлений гормональной недостаточности) .
В фазе интенсивной терапии назначают четыре основных препарата: изониазид, рифампицин, пиразинамид, этамбутол. Интенсивную фазу продолжают 2 месяца. За этот срок больной должен принять 60 доз комбинации из четырех (у детей из трех) основных препаратов. В случае пропуска приема полных доз длительность фазы интенсивной терапии увеличивают до приема 60 доз.
Через 2 месяца от начала интенсивной фазы терапии вопрос о переходе ко второму этапу лечения решает комиссия на основании данных исследований.
При появлении бактериовыделения и в случае отрицательной клинико-ренттенологической динамики процесса после двух месяцев лечения необходимы определение лекарственной чувствительности микобактерий туберкулёза и соответствующая коррекция химиотерапии. В ожидании результатов лечение не меняют в течение месяца. При невозможности исследования лекарственной чувствительности больного направляют в вышестоящее учреждение. Режим дальнейшего лечения определяют с учетом лекарственной чувствительности возбудителя.
В фазе продолжения терапии назначают два основных препарата - изониазид и рифампицин - 4 месяца ежедневно или в интермиттирующем режиме (3 раза в неделю). Другим режимом в фазе продолжения может быть прием изониазида и этамбутола в течение 6 месяцев.
4 режим (4 категория больных)
IV режим химиотерапии назначают больным с выделением микобактерий, устойчивых к изониазиду и рифампицину одновременно.
В фазе интенсивной терапии назначают комбинацию как минимум из пяти противотуберкулёзных препаратов, чувствительность к которым сохранена, например: пиразинамид, препарат из группы фторхинолонов, канамицин/амикацин или капреомицин, протионамид/этионамид и этамбутол. Назначение препаратов резервного ряда зависит отданных исследования лекарственной чувствительности выделяемых больным микобактерий туберкулёза, причем необходимо также учитывать данные о лекарственной устойчивости микобактерий по региону.
При положительной клинико-ренттенологической динамике и отрицательных результатах культурального исследования мокроты после 6 месяцев химиотерапии переходят к фазе продолжения.
В фазе продолжения назначают не менее трех препаратов из числа тех, чувствительность к которым сохранена. Длительность фазы продолжения - не менее 12 мес.
Применение продуктов на основе личинок восковой моли для лечения туберкулёза
Экстракт , гомогенат и настойка личинок восковой моли , а также настойка ПЖВМ и оказывают губительное влияние на микобактерии туберкулёза, разрушая их восковые оболочки.
В экстракте, настойке и гомогенате ЛВМ, а также в настойке ПЖВМ и мёде с гомогенатом личинок восковой содержится специфический пищеварительный фермент личинок восковой моли - фермент цераза (химически синтезированного аналога фермента цераза - НЕТ
)
, который способствует рассасыванию очаговых изменений и препятствует их дальнейшему распространению в организме.
Под воздействием фермента цераза увеличивается проницаемость клеток микобактерий туберкулёза для противотуберкулёзных препаратов всех видов, что помогает подавить лекарственную устойчивость микобактерий.
Применение гомогената, экстракта, настойки личинок восковой моли, а также настойки ПЖВМ и мёда с гомогенатом личинок восковой моли в комплексной терапии туберкулёза позволяет значительно снизить лекарственную нагрузку на организм, оказать разноплановое лечебное воздействие и повысить эффективность химиотерапии (сократив срок приема противотуберкулёзных препаратов) .
Продукты пчеловодства на основе личинок восковой моли является мощными природными иммуностимуляторами.
Прием продуктов на основе личинок восковой моли значительно усиливает процесс фагоцитоза.
Фагоцитоз - процесс, при котором специально предназначенные для этого клетки иммунной системы организма - фагоциты защищают организм путем поглощения вредных чужеродных частиц, бактерий, мертвых /погибающих клеток. Осуществляется двумя разновидностями клеток: циркулирующими в крови зернистыми лейкоцитами (гранулоцитами) и тканевыми макрофагами.
В продуктах на основе личинок восковой моли присутствуют незаменимые природные компоненты (аланин , лейцин , треонин , валин , изолейцин , гистидин и др.), стимулирующие сопротивляемость организма, рост и размножение клеток.
Продукты пчеловодства на основе личинок восковой моли увеличиваут сопротивляемость ткани к туберкулёзной инфекции и способствуют заживлению туберкулёзных каверн в легких.
По мере затихания туберкулёзного процесса величина бактериальной популяции уменьшается вследствие подавления размножения микобактерий. В условиях продолжающейся химиотерапии и снижения бактериальной популяции в организме больного сохраняется часть микобактерий, которые находятся в состоянии персистирования. Персистируюшие микобактерий часто называют спящими или дремлющими. На этом этапе, когда интенсивное размножение бактериальной популяции сменяется состоянием персистирования оставшейся ее части, микобактерий находятся, главным образом, внутриклеточно (внутри фагоцитов - клеток иммунной системы).
Противотуберкулёзными препаратами очень трудно оказать воздействие действие на микобактерии расположенные внутриклеточно.
Применение продуктов на основе личинок восковой моли позволяет подавить жизнедеятельность внутриклеточно локализованных микобактерий.
Высокую лечебную эффективность продукты пчеловодства на основе личинок восковой моли проявляют и при лечении внелегочной туберкулёзной патологии и других органов человеческого организма: лимфатической и пищеварительной системы, костей и суставов, мочеполовых органов, кишечника, кожи, глаз, центральной нервной системы и мозговых оболочек.
Продукты на основе личинок восковой моли эффективны и против грибковых заболеваний легких (и прочих побочных реакций организма)
, являющихся частыми осложнениями химиотерапевтических курсов лечения туберкулёза.
Содержащаяся в продуктах на основе личинок восковой моли аспарагиновая кислота помогает печени выводить из организма остаточные продукты лекарств после курсов химиотерапии.
О совместимости спиртосодержащих настоек/экстрактов и антибиотиков
В течение десятилетий в обывательской и медицинской среде, существует мнение, что прием спиртосодержащих экстрактов и настоек и антибиотиков несовместимы, т. к. при этом снижается эффективность антибиотиков, и возникают различные побочные эффекты.
Однако анализ существующих научных исследований показывает, что в большей части это выдуманный миф, не имеющий за собой никаких доказательств.
Британские исследователи считают, что миф возник во время второй мировой войны, когда производство антибиотика пенициллина было трудоемким и дорого стоило. Поэтому пенициллин повторно извлекали из мочи раненых и больных военнослужащих. Для того чтобы уменьшить объем мочи и ускорить выделение пенициллина, им было запрещено принимать пиво, входящее в ежедневное довольствие.
Последние исследования, в которых определялось влияние алкоголя (до 30мг чистого этанола)
на некоторые фармокинетические показатели различных антибиотиков, показывающих распределение их по организму, не выявили их изменений либо они были незначительны.
Небольшие дозы алкоголя
(до 15мг чистого этанола)
не влияют на фармокинетику большинства
(включая все противотуберкулёзные препараты
)
антибиотиков в организме.
15мг чистого этанола – это, например, 44мл 40% алкоголя.
Одновременный прием экстракта личинок восковой моли и противотуберкулёзных препаратов
При туберкулёзе предпочтительней принимать 25% экстракт личинок восковой моли или 50% гомогенат личинок восковой моли
(при нормальной переносимости - настойку продуктов жизнедеятельности личинок восковой моли, причем концентрация фермента цераза в 20% настойке ПЖВМ выше, чем в настойке, 25% экстракте личинок восковой моли и даже чем в 50% гомогенате личинок восковой моли!
)
, т. к. они имеет большую концентрацию полезных веществ при меньшем содержании этанола (спирта)
в конечной дозе (при полной непереносимости или неприятия спиртосодержащих продуктов подойдет
мёд с гомогенатом личинок восковой моли)
.
Содержание этанола
(спирта)
в разовой дозе 25% экстракта личинок восковой моли
(на 1 прием)
- не изменит эндогенную концентрацию этанола в организме
(эндогенное - естественное содержание алкоголя в крови – в норме составляет до 0,3 промилле)
.
Максимальная разовая доза 25% экстракта личинок восковой моли для человека любого веса и дозировки - поднимает концентрацию алкоголя в крови на 0,098 промилле (т. к. в формуле расчета концентрации, также учитывается вес)
.
В среднем эндогенная (естественная и постоянно присутствующая)
концентрация этанола в организме составляет - 0,18 промилле. Непосредственно после приема экстракта личинок восковой моли концентрация увеличится до 0,278 промилле, что является допустимой нормой - можно управлять автомобилем, принимать при кодировке от алкоголизма и совместно с любым дисульфирамом (Антабус, Тетурам, Эспераль и др.)
.
Через 30 минут после приема 25% экстракта личинок восковой моли 0,098 промилле будут полностью переработаны организмом и концентрация придет к изначальному значению.
Практически во всех (95%), известных нам за 8 лет случаях приема экстракта личинок восковой моли для лечения туберкулёза, больные принимали экстракт личинок восковой моли одновременно с курсом противотуберкулёзных препаратов (в том числе и по рекомендации лечащих врачей). Случаев возникновения побочных реакций (аллергий и пр.) не было.
При правильном систематическом приеме – результат применения экстракта личинок восковой моли удивлял даже опытных врачей-фтизиатров!