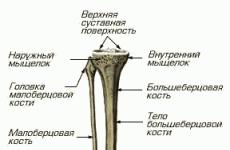
Эпителиальный рак. Плоскоклеточный рак кожи, гортани, желудка, пищевода, легкого, шейки матки и других органов - причины и механизмы развития, разновидности, стадии и симптомы, диагностика и лечение, прогноз Плоскоклеточный рак шейки матки
Чтобы понимать, что такое эпителиальная опухоль и какая она бывает, нужно разобраться, что собой представляет новообразование и является ли оно онкологией. Это очень важно. Например, эпителиальные опухоли полости рта могут быть доброкачественными или злокачественными.
К сожалению, сегодня растет количество заболевших раком людей, и смертность от этой болезни занимает третье место после смертей от заболеваний сердечно-сосудистой и дыхательной системы. Каждый год регистрируют примерно шесть миллионов новых случаев заболевания. Среди мужчин лидерами оказались те граждане, которые проживают на территории Франции. А среди женщин чаще заболевают представительницы слабого пола, живущие в Бразилии.
Рост заболеваемости можно объяснить отчасти старением жителей планеты, так как чаще страдают люди зрелого и особенно преклонного возраста. По статистике, каждый второй заболевший онкологией - это человек старше 60 лет.
Что такое рак и что собой представляют опухоли эпителиального происхождения? Чем отличаются доброкачественные и злокачественные новообразования и какими они бывают?
Что такое рак
Термин "рак" используется в медицине как общее название для онкологических заболеваний. Для него характерно бесконтрольное размножение клеток. Их агрессивный рост поражает и сам орган, откуда "неправильные" клетки берут свое начало, и близлежащие органы. Также у злокачественной формы опухоли есть склонность к метастазированию.
У мужчин чаще всего под ударом находится предстательная железа и легкие, а у женщин уязвимым органом является молочная железа, чуть реже яичники. Кстати, эпителиальные в 80-90 % случаев развивается из эпителиальной ткани.
Как здоровые клетки "превращаются" в раковые

Организм человека состоит из миллиардов клеток, все они появляются, делятся и умирают в определенный момент, если они здоровы. Все это запрограммировано, есть начало цикла жизни клетки и конец. Когда они в норме, деление происходит в соответствующих количествах, новые клетки замещают старые. Процесс не выходит за пределы органов и тканей. За это отвечают регуляторные системы организма.
Но если структура клеток меняется вследствие воздействия разных факторов, то они теряют способность к самоликвидации, перестают контролировать свой рост, перерастая в раковые, и начинают бесконтрольно размножаться. То есть для таких клеток характерен инвазивный рост.
Результатом этого являются "модифицированные клетки", которые способны на длительную жизнедеятельность. Они в итоге и формируют злокачественную способен поразить до нескольких органов сразу. Нездоровые клетки распространяются по организму по лимфатической и кровеносной системе, распространяя метастазы.
Причины развития рака

Причины развития онкологии разнообразны, но специалисты не могут однозначно ответить на вопрос, что именно вызвало рак в каждом отдельном случае. Некоторые полагают, что это экология, другие винят в этом генномодифицированные продукты. При этом все ученые выделяют факторы, способствующие нарушению работы клеток, что в конечном итоге может привести к злокачественной форме новообразования.

Известно достаточное количество факторов, влияющих на запуск канцерогенеза. Что может способствовать заболеванию?
- Химические канцерогены. К данной категории относятся винилхлорид, металлы, пластик, асбест. Их особенностью является то, что они способны влиять на ДНК-клетки, провоцируя злокачественное перерождение.
- Канцерогены физической природы. К ним относятся различного вида излучения. Ультрафиолетовое, рентгеновское, нейтронное, протонное излучение.
- Биологические факторы канцерогенеза - разные виды вирусов, такие как герпесоподобный вирус Эпштейна - Барр, который вызывает лимфому Беркитта. Вирус папилломы человека может вызвать Вирусы гепатитов B и C способствуют раку печени.
- Гормональные факторы — человеческие гормоны, например половые. Они могут повлиять на злокачественное перерождение ткани.
- Генетические факторы также влияют на появление рака. Если у предшествующих родственников были случаи заболевания, то возможность развития недуга у следующих поколений выше.
Названия доброкачественных и злокачественных опухолей
В названии опухоли всегда присутствует окончание "ома", а первая часть - это название задействованной ткани. К примеру, опухоль кости —остеома, жировой ткани —липома, сосудистой — ангиома, а железистой —аденома.
Саркома - это злокачественная форма из мезенхимы. Диагноз зависит от вида мезенхимальной ткани, например остеосаркома, миосаркома, ангиосаркома, фибросаркома и так далее.
Канцер или карцинома - это название злокачественной эпителиальной опухоли.
Классификация всех новообразований
Международная классификация новообразований исходит из патогенетического принципа с учетом морфологического строения, вида клеток, тканей, органов, мест нахождения, а также структуры в отдельных органах. Например, органоспецифические или органонеспецифические.
Все существующие новообразования подразделяются на семь групп. Группа зависит от принадлежности опухоли к определенной ткани и различает их по гистогенезу.
- эпителиальные опухоли, не имеющие специфической локализации;
- опухоли экзо- или эндокринных желез или специфических эпителиальных тканей;
- мягкотканные опухоли;
- опухоли меланинобразующей ткани;
- опухоли мозга и нервной системы;
- гемобластомы;
- тератомы, дисэмбриональные опухоли.
Медицина разделяет две формы - доброкачественную и злокачественную.
Эпителиальные доброкачественные и злокачественные опухоли

По клиническому течению разделяют:
- доброкачественные формы из эпителия или эпителиом;
- злокачественные, которые называют раком или карциномой.
По гистологии (виду эпителия) различают:
- новообразование из покровного эпителия (многослойного плоского и переходного);
- из железистого эпителия.
По органной специфичности:
- органоспецифические опухоли,
- органонеспецифические (без специфической локализации).
Доброкачественная форма
К доброкачественным эпителиальным опухолям (эпителиомам) относятся:
- Папиллома (из плоского и переходного покровного эпителия).
- Аденома (из железистого эпителия). В злокачественной форме - это карцинома.
Обе разновидности обладают исключительно тканевым атипизмом и имеют паренхиму и строму. Всем известные папилломы являются доброкачественной формой эпителиальной опухоли, которая, в свою очередь, происходит из ткани покровного эпителия.
Папилломы образуются на поверхности кожи из плоского либо переходного эпителия. Также могут быть не на поверхности, а, например, в слизистой оболочке глотки, на голосовых связках, на тканях мочевого пузыря, мочеточников и лоханок почек или в других местах.
Внешне они напоминают сосочки, а могут напоминать и цветную капусту. Могут быть в единичном проявлении, а могут быть и множественными. Папиллома часто имеет ножку, которая прикреплена к коже. Тканевый атипизм возникает вследствие нарушения основной особенности любого эпителия — комплексности. При таком нарушении происходит сбой в определенном расположении клеток и их полярности. При данной доброкачественной опухоли сохраняется экспансивный рост клеток (базальная мембрана). При клеток новообразование растет само из себя, увеличиваясь в размере. Оно не внедряется в соседние ткани, что привело бы к их разрушению, как при инвазивном росте.
Течение папиллом различно и зависит от вида пораженной ткани. Папилломы, расположенные на поверхности кожи (либо бородавки), развиваются и растут медленно. Такие образования, как правило, не доставляют большого беспокойства своим обладателям. А вот в случае появления во внутренних частях тела вызывают достаточно проблем. Например, после удаления папилломы с голосовых связок они могут появится вновь, так как носят рецидивирующий характер. Доброкачественные могут начать изъязвляться, что впоследствии ведет к кровотечению и возникновению гематурии (кровь появляется в моче).
Несмотря на то, что папилломатозные новообразования на коже являются доброкачественной формой опухоли и не вызывают особого беспокойства, малигнизирование опухоли в злокачественную все-таки возможно. Этому способствует тип ВПЧ и предрасполагающие внешние факторы. Существует более 600 видов штаммов ВПЧ, из которых более шестидесяти обладают повышенным онкогеном.
Аденома также относится к опухоли эпителиального происхождения и формируется из железистого эпителия. Это зрелое новообразование. Молочная железа, щитовидная и другие являются возможным местом дислокации аденомы. Также она может образоваться в слизистых оболочках желудка, в кишечнике, бронхах и матке.
Рост клеток аденомы, так же как и у папиллом, имеет экспансивный характер роста. Она отграничена от соседней ткани и имеет вид узла мягко-эластичной консистенции, розовато-белого цвета.
На сегодняшний день принцип развития этого образования изучен не до конца, но обычно удается увидеть первые нарушения в балансе гормонов - регуляторов функции желизистого эпителия.
В случаях, когда в таком доброкачественном новообразовании присутствует киста, то используется термин кисто- или цистоаденома.
По морфологическим видам аденомы делятся на:
- фиброаденома - аденома, в которой строма преобладает над паренхимой (часто формируется в молочной железе);
- альвеолярная или ацинарная, которая копирует концевые отделы желез;
- тубулярная, способная сохранять протоковый характер эпителиальных структур;
- трабекулярная, для которой характерно балочное строение;
- аденоматозный (железистый) полип;
- кистозная с резко выраженным расширением просвета желез и образованием полостей (это как раз и есть цистоаденома);
- кератоакантома относится к э-пителиальной опухоли кожи.
Особенностью аденом является то, что они способны перерождаться в рак, в аденокарциному.
Злокачественная форма
Этот вид рака может развиться из покровного или железистого эпителия. Эпителиальный рак способен появиться в любом органе, где присутствует эпителиальная ткань. Этот вид самый часто встречающийся среди злокачественных Для него характерны все свойства злокачественности.
Всем злокачественным новообразованиям предшествуют В какой-то момент клетки приобретают клеточный атипизм, начинается анаплазия, и они начинают постоянно размножаться. Изначально процесс не выходит за пределы эпителиального пласта и отсутствует инвазивный рост клеток. Это является начальной формой рака, для которого специалисты используют термин «рак на месте».
Если в этот период распознать прединвазивный рак, то это поможет избавиться от дальнейших серьезных проблем. Как правило, проводится хирургическое лечение, и в этом случае намечается благоприятный прогноз. Проблема в том, что пациент редко испытывает какие-либо симптомы заболевания, и этот "начальный" рак сложно обнаружить, так как он никак не проявляется на макроскопическом уровне.
Злокачественная опухоль из по гистогенезу может иметь следующий характер:
- переходноклеточный из покровного эпителия (плоского и переходного);
- базальноклеточный;
- (мелкоклеточный, полиморфноклеточный и др.);
- базальноклеточный;
- плоскоклеточный ороговевающий рак (злокачественные формы заболевания эпителиального строения чаще всего (до 95 %) представлены плоскоклеточным ороговевающим раком;
- плоскоклеточный неороговевающий рак.
Рак, происходящий из железистого эпителия:
- Коллоидный и его разновидность - перстневидноклеточный рак.
- Аденокарцинома. Кстати, название этой опухоли дал Гиппократ. Он сравнил ее внешний облик с крабом.
- Солидный рак.
Также специалисты различают по особенностям следующие опухоли из эпителиальной ткани:
- медуллярный, или мозговидный, рак;
- простой рак, или вульгарный;
- скирр, или фиброзный рак.
Симптоматика онкологических заболеваний
Симптомы заболевания зависят от того, где именно развилось опухоль, в каком органе, от скорости ее роста, а также наличия метастазов.
Распространенные признаки:
- Изменение состояния кожных покровов на определенном участке в виде растущей припухлости, которая окружена каймой гиперемии. Припухлости могут начать изъязвляться, появляются язвы, плохо поддающиеся лечению.
- Изменение тембра голоса, человеку трудно глотать, кашель приступами, боль в области груди либо живота.
- Больной может сильно похудеть, ему свойственен плохой аппетит, слабость, стойкое повышение температуры, анемия, уплотнение в молочной железе и кровянистые выделения из соска или мочевого пузыря, трудности при мочеиспускании.
Но могут присутствовать и иные симптомы.
Диагностика рака

Необходим своевременный поход к специалисту для тщательного осмотра и подробный сбор анализов. К диагностическим методам для выявления болезни относятся:
- физикальный метод изучения пациента;
- компьютерная томография, МРТ (считается очень действенным методом), рентгенография;
- анализ крови (общий и биохимический), выявление опухолевых маркеров в крови;
- пункция, биопсия с морфологическим исследованием;
- бронхоскопия, эзофагогастродуоденоскопия.

Все эти меры помогут обнаружить болезнь на ранней стадии и полностью вылечить пациента.
Железисто-плоскоклеточный рак шейки матки - клинико-прогностические характеристики заболевания
Э.К. Танривердиева, К.И. Жорданиа, Т.И. Захарова, Е.В. Приходько, Л.Т. Мамедова
НИИ клинической онкологии ФГБУ РОНЦ им. Н.Н. Блохина РАМН, Москва
Контакты: Эльнара Курбанали кызы Танривердиева [email protected]
Железисто-плоскоклеточный рак является редкой формой рака шейки матки. Из-за небольшого числа наблюдений железистоплоскоклеточный рак шейки матки остается малоизученным заболеванием, хотя первое упоминание о нем относится еще к 1956г., когда A. Glucksmann и C.D. Cherry впервые была описана аденоакантома шейки матки.
Ключевые слова: железисто-плоскоклеточный рак шейки матки, прогноз
Adenosquamous cell carcinoma of the cervix - clinical and prognostic characteristics of the disease
E.K. Tanriverdieva, K.I. Zhordania, T.I. Zakharova, E.V. Prihodko, L.T. Mamedova
Federal State Budgetary Institution N.N. Blokhin Russian Cancer Research Center, Russian Academy of Medical Sciences, Moscow
Adenosquamous cell carcinoma of the cervix is a rare form of cancer of the cervix. Because of the small number of observations adenosquamous cell carcinoma of the cervix remains poorly understood disease, although the first mention of it dates back to 1956, when A. Glucks-mann, and C.D. Cherry first described of mixed carcinoma (adenoacanthoma) of the uterine cervix.
Key words: adenosquamous cell carcinoma of the cervix, prognosis
Введение
Рак шейки матки (РШМ) по-прежнему занимает одну из ведущих позиций в структуре женской онкологической заболеваемости и смертности в развивающихся странах Азии, Африки и Латинской Америки и является важной медицинской и социальной проблемой во всех экономически развитых странах .
В России РШМ занимает 2-е место в структуре онкогинекологической заболеваемости после рака тела матки . За последние десятилетия заболеваемость железистым РШМ в западных странах увеличилась с 5 до 20-25 % от всех случаев злокачественных новообразований шейки матки . На сегодняшний день стадия РШМ, размер, гистологический тип и дифференцировка опухоли, уровень лимфоцитарной инфильтрации и метастатическое поражение регионарных лимфатических узлов (ЛУ), определяющиеся после оперативного лечения, имеют большое значение не столько в описательном, сколько в прогностическом плане.
Традиционно для составления прогноза течения РШМ в первую очередь используют следующие морфологические характеристики послеоперационного материала:
Гистологический тип опухоли;
Ее размер;
Глубина инвазии в подлежащие ткани;
Наличие метастазов в регионарные ЛУ .
Ь. FruЫing й а1. в 1962 г. впервые определили полипотентные функции резервноклеточного эпите-
лия шейки матки и выделили 2 гистологических типа плоскоклеточного РШМ (ПлРШМ) в зависимости от его происхождения - из многослойного плоского эпителия или из резервных клеток цилиндрического эпителия.
Появившееся в последующем мнение, объясняющее возникновение многообразия гистологических форм из резервных клеток, определяет зависимость изучения особенностей состояния и изменения качественных признаков этих клеток. В частности, резервные клетки цилиндрического эпителия считаются полипотентными, способными в процессе опухолевого роста образовывать как многослойный плоский, так и железистый эпителий .
Неоднозначность клинического течения данной злокачественной формы обусловлена в основном неоднородностью биологических особенностей опухоли. В гистологической классификации ВОЗ (2003) выделено более 20 вариантов РШМ, в том числе плоскоклеточный и недифференцированный.
Считается, что ЖПРШМ обладает более высокой потенцией к лимфогенному метастазированию, чем ПлРШМ и АШМ . В свою очередь низкодифференцированная слизепродуцирующая АШМ и ЖПРШМ со слизеобразованием имеют схожее клиническое тече-
Гинекология
Гинекология
ние, и для морфолога подчас крайне трудно разделить эти 2 типа опухолей .
Были выделены 3 основные формы ЖПРШМ:
Коллизионный тип, состоящий из полностью отдельных компонентов - ткани инвазивной плоскоклеточной карциномы и железистых элементов;
Ткани с диффузным распространением двух слитных элементов;
Ткани, представленные в основном плоскоклеточной формой рака, но содержащие муцин в цитоплазматических вакуолах .
Обычно полагают, что ЖПРШМ имеет худший прогноз, чем ПлРШМ. Однако Н.М. БЫ^Ыоп е! а1. не делают подобного вывода. Научные исследования в отношении этого вопроса единичны, крайне противоречивы и недостоверны.
Цель исследования - изучение влияния некоторых клинико-прогностических факторов на выживаемость больных ЖПРШМ.
Материалы и методы
В исследование включены 156 больных РШМ в возрасте от 24 до 73 лет, получавших лечение в ФГБУ РОНЦ им. Н.Н. Блохина РАМН в 1981-2005 гг. Основную группу исследования составили 56 больных ЖПРШМ в возрасте от 24 до 66 лет, 1-ю контрольную группу - 50 пациенток с АШМ и 2-ю контрольную группу - 50 больных ПлРШМ. Проведен ретроспективный анализ историй болезни пациенток, проходивших терапию в 1981-2001 гг., а также выполнено проспективное исследование течения ЖПРШМ у больных, получавших лечение в 2002-2005 гг.
До начала терапии все пациентки прошли полное клинико-лабораторное и инструментальное обследование в РОНЦ им. Н.Н. Блохина РАМН. У больных ЖПРШМ преобладали опухоли размерами 1,1-2 (35,7 % пациенток) и 4,1-6 (33,9 %) см, у пациенток с АШМ - только опухоли размерами 1,1-2 (32 %) см. В плоскоклеточной группе превалировали опухоли размерами < 1 см (30 % больных). Оценку стадии заболевания на дооперационном этапе проводили в соответствии с международной классификацией ТКМ (2002) и классификацией FIGO. У больных ЖПРШМ чаще всего встречались опухоли 1В1 (26,8 %) и 11В (21,4 %) стадий. В контрольных группах у пациенток с АШМ преобладали опухоли 11А (34 %), у больных
ПлРШМ - IB (50 %) стадий. Из 56 больных ЖПРШМ при гистологическом исследовании опухоли до начала лечения у 12 (21,4 %) был диагностирован ПлРШМ, у 2 (3,6 %) - АШМ и у 2 (3,6 %) - карцинома in situ (CIS). В 1-й контрольной группе из 50 пациенток с АШМ при обследовании до начала лечения у 3 (6 %) был верифицирован ЖПРШМ, у 2 (4 %) - ПлРШМ и у 2 (4 %) - CIS, а во 2-й контрольной группе из 50 больных ПлРШМ у 3 (6 %) была выявлена CIS. У 39,2 % (большинство) пациенток с ЖПРШМ был установлен эндофитный рост опухоли, у 28,6 % - экзофитный, у 26,8 % - смешанный, у 17,9 % обнаружена инфильтрация параметрия, не достигающая стенок таза, и у 8,9 % наблюдалось распространение опухолевого процесса на стенки таза. В 1-й контрольной группе преобладали опухоли с эндофитной (32 %), а во 2-й - с экзофитной (42 %) формой роста. Лечение больных РШМ проводили в зависимости от распространенности опухоли и тяжести сопутствующей соматической патологии. У 98,2 % пациенток с ЖПРШМ были выполнены радикальные оперативные вмешательства и у 1,8 % - паллиативные. Дополнительное (комбинированное и комплексное) лечение получили 52 (92,86 %) из 56 больных ЖПРШМ. Предоперационную терапию провели 4 (7,1 %), послеоперационную - 40 (71,4 %) и оба вида дополнительного лечения - 8 (14,3 %) пациенткам. Предоперационное лечение, включавшее лучевую (ЛТ) и химиолучевую (ХЛТ) терапию, перенесли 11 (19,6 %) и 1 (1,8 %) больная соответственно. ХЛТ была проведена 3 больным РШМ IIB стадии и 1 пациентке с IIIA стадией заболевания. Химиолучевое лечение состояло из ЛТ в комбинации с цисплатином в дозе 40 мг/м2 еженедельно в течение
Предоперационную ЛТ назначали пациенткам с IB2-IIA стадиями, а также с IB1 стадией при наличии эхографических признаков метастатического поражения ЛУ таза и при IIB стадии - при наличии пришеечного инфильтрата.
Дистанционную гамма-терапию получили 6 больных ЖПРШМ, внутриполостную - 1, сочетанную - 5.
Использовали 3 основных варианта облучения:
Дистанционное облучение первичного очага и зон регионарного метастазирования в статическом или подвижном режиме. При статической дистанционной гамма-терапии применяли два противолежащих фигурных поля размерами 15 х 17 или 16 х 18 см, в подвижном режиме - двухосевое маятниковое облучение на угол качания 180-200° при параллельных осях качания полями размерами 5 х 17 или 6 х 18 см. Разовая очаговая доза (РОД) составляла 2 Гр, суммарная (СОД) - 20-30 Гр. Операцию выполняли через 12-14 дней после окончания ЛТ;
Дистанционное облучение тазовых ЛУ четырьмя статическими фигурными полями размерами
4 х 12,5 х 14 см, расположенными наклонно к центральной оси тела. РОД - по 4 Гр на каждую из 4 фракций, СОД - 16 Гр. Для воздействия на первичный очаг использовали внутриполостную гамматерапию до и после дистанционного облучения в дозах 10 Гр за 2 фракции на аппарате Агат-В или 15-18 Гр за 2 фракции. Операцию выполняли через 3-5 дней после окончания ЛТ;
Интенсивное концентрированное дистанционное облучение в подвижном режиме полями размерами 4 х 10 х 12 см, угол качания - 90-180°, РОД - 5-5,5 Гр, СОД на каждый параметрий - 20 Гр.
Послеоперационное лечение было проведено 48 (85,7 %) из 56 больных ЖПРШМ и включало химиотерапию, ЛТ и ХЛТ у 2 (3,6 %), 43 (76,8 %) и 3 (5,4 %) пациенток соответственно.
Результаты
Средний возраст 56 больных ЖПРШМ составил
46.7 ± 9,7 года, заболевание наиболее часто встречалось у женщин в возрасте 41-60 лет (71,4 % случаев). Во время исследования 27 (48,2 %) из 56 пациенток находились в репродуктивном возрасте, 2 (3,6 %) - в пременопаузе, 22 (39,3 %) - в менопаузе и 5 (8,9 %) - в постменопаузе. Средний возраст больных с АШМ был достоверно выше и составил 55,1 ± 9,9 года, 74 % пациенток этой группы были в возрасте старше 50 лет. Достоверных различий среднего возраста между больными ЖПРШМ и ПлРШМ не отмечено.
В ходе отдельного исследования пациенток с ранними стадиями РШМ статистически достоверной разницы между показателями 5-летней выживаемости у больных ЖПРШМ (26,3 ± 22,5 %) и АШМ (31,5 ± 14,0 %) не зарегистрировано. При сравнении уровней безрецидивной выживаемости у больных РШМ ранних стадий достоверно (р = 0,02) более низкая 5-летняя выживаемость была отмечена у пациенток с ЖПРШМ (26,3 ± 22,5 %) по сравнению с таковой у больных ПлРШМ (68,6 ± 16,3 %).
Тем не менее при исследовании выживаемости пациенток с запущенными стадиями было установлено, что гистологическое строение ЖПРШМ связано со значительным снижением уровня однолетней без-рецидивной выживаемости - 10,9 ± 14,6 % (медиана - 6,7 мес). У больных ПлРШМ однолетняя выживаемость достигала 50 ± 20,4 % (медиана - 10,5 мес), а у пациенток с АШМ - 31,2 ± 25,2 % (медиана не достигнута).
В целом однолетняя безрецидивная выживаемость больных ЖПРШМ составила 79,2 ± 5,6 %, 3-летняя - 55,9 ± 7,1 % и 5-летняя - 53,5 ± 7,2 % (медиана - 80,1 мес). Аналогичные показатели у пациенток с ПлРШМ и АШМ были достоверно выше. Общая однолетняя выживаемость больных ПлРШМ достигла
91.7 ± 4,0 %, 3-летняя - 80,6 ± 5,8 % и 5-летняя -
77,0 ± 6,3 %, при АШМ эти показатели были равны
89,7 ± 4,4; 76,0 ± 6,3 и 72,3 ± 6,7 %.
Для выявления прогностических факторов прогрессирования ЖПРШМ и смертности от этого заболевания применяли одно- и многофакторный регрессионный анализ клинических, лабораторных и морфологических данных больных, включенных в исследование. При построении регрессионных моделей для создания обучающей выборки использовали данные 40 пациенток, для экзаменационной выборки - данные остальных 16 больных.
В однофакторный регрессионный анализ, учитывающий силу воздействия каждого фактора в отдельности, были включены следующие факторы: возрастная группа; состояние менструальной функции; время начала половой жизни; наличие беременности, родов и прерываний беременности в анамнезе; наличие гинекологических заболеваний в анамнезе (кроме заболеваний шейки матки); наличие заболеваний шейки матки в анамнезе; гинекологические операции в области шейки матки (крио- или лазерная деструкция, электрокони-зация, электрокоагуляция шейки матки, раздельное диагностическое выскабливание); наличие соматической патологии, сопутствующей ЖПРШМ, в том числе рак другой локализации; семейный онкологический анамнез; клинические симптомы ЖПРШМ; локализация, размеры и форма роста ЖПРШМ; состояние сводов и параметрия; состояние регионарных ЛУ; наличие инвазии опухоли в лимфатические и кровеносные сосуды; наличие некрозов и кровоизлияний в опухоли; стадия, степень злокачественности ^) и гистологический тип ЖПРШМ; вид лечения ЖПРШМ; тип и радикальность оперативного лечения ЖПРШМ; наличие пред- и послеоперационного лечения; наличие патомор-фоза опухоли.
Прогностические факторы, способные оказывать изолированное влияние на частоту прогрессирования ЖПРШМ, представлены в табл. 1. Коэффициенты значимости приведены в порядке убывания.
При однофакторном анализе было выделено только
7 факторов, способных оказывать изолированное статистически значимое (р < 0,05) влияние на частоту прогрессирования ЖПРШМ. Это гистологический тип, степень злокачественности и стадия ЖПРШМ, наличие опухолевого поражения параметрия, радикальность оперативного лечения ЖПРШМ и наличие в анамнезе прерываний беременности (аборты) и гинекологических операций в области шейки матки.
Таким образом, у больных ЖПРШМ, включенных в данное исследование, можно выделить 7 основных прогностических факторов, каждый из которых значимо повышает частоту прогрессирования заболевания. К этим факторам относят: 1) наличие III типа ЖПРШМ; 2) высокая степень злокачественности опухоли ^3); 3) Ш-ГУ стадия заболевания; 4) наличие
Гинекология
Гинекология
Таблица 1. Прогностические факторы, оказавшие статистически значимое влияние на прогрессирование ЖПРШМпо результатам однофакторного анализ
Гистологический тип 0,297 0,002
Опухолевое поражение параметрия 0,304 0,022
Степень дифференцировки ^) 0,291 0,029
Стадия заболевания 0,277 0,039
Радикальность оперативного лечения 0,267 0,046
Прерывание беременности 0,390 0,003
Гинекологические операции в области шейки матки в анамнезе 0,268 0,046
опухолевого поражения параметрия; 5) нерадикаль-ность оперативного лечения ЖПРШМ; 6) наличие в анамнезе прерываний беременности; 7) наличие в анамнезе гинекологических операций в области шейки матки.
На следующем этапе статистического анализа была построена регрессионная модель с различным набором факторов. При многофакторном анализе были отобраны 4 наиболее информативных признака, повлиявших на прогрессирование ЖПРШМ (табл. 2). Это гистологический тип, стадия и степень злокачественности ЖПРШМ, а также радикальность оперативного лечения заболевания. Остальные 3 фактора, статистически значимые при однофакторном анализе, утратили свою актуальность в результате многофакторного анализа.
Таблица 2. Прогностические факторы, оказавшие статистически значимое влияние на прогрессирование ЖПРШМ по результатам многофакторного анализа
Прогностический фактор Коэффициент P
Гистологический тип 0,180 0,04
Стадия заболевания 0,213 0,08
Степень дифференцировки ^) 0,173 0,09
Радикальность оперативного лечения 0,221 0,09
Коэффициент детерминации модели равнялся 0,57 % при р = 0,005. Чувствительность данной модели достигала 67 %, специфичность - 86 %, точность - 77 %. Для экзаменационной выборки чувствительность модели составила 70 %, специфичность - 67 %, точность - 69 %.
Таким образом, у больных ЖПРШМ, включенных в данное исследование, можно выделить 4 основных прогностических фактора, которые в совокупности статистически значимо повышали частоту прогрессирования заболевания. Это, в первую очередь, III тип ЖПРШМ (у больных с III гистологическим типом ЖПРШМ безрецидивная выживаемость была минимальной: 1-летняя - 68,4 ± 15,0 %, 3-летняя - 31,3 ± 15,0 % и 5-летняя - 21,7 ± 13,1 %, медиана - только 24,4 мес), а также III-IV стадии заболевания (однолетняя безрецидивная выживаемость всех больных ЖПРШМ, получивших комплексное лечение, составила только 10,9 ± 14,6 %, медиана - 6,7 мес), высокая степень злокачественности опухоли ^3) и не-радикальность оперативного лечения ЖПРШМ.
Для определения прогностических факторов, повлиявших на частоту смертности больных ЖПРШМ, нами был проведен аналогичный одно- и многофакторный анализ с построением регрессионной модели. Весовые коэффициенты факторов, оказавших статистически значимое влияние на частоту смертности, представлены в порядке убывания в табл. 3.
Таблица 3. Прогностические факторы, оказавшие статистически значимое влияние на частоту смертности от ЖПРШМ
Прогностический фактор Коэффициент P
Однофакторный анализ:
стадия заболевания 0,330 0,013
размер опухоли 0,326 0,014
опухолевое поражение параметрия 0,248 0,065
Многофакторный анализ:
стадия заболевания 0,353 0,006
У больных ЖПРШМ, включенных в данное исследование, по результатам однофакторного анализа можно выделить 2 основных прогностических фактора, каждый из которых сам по себе значимо повышал частоту смертности больных: 1) III-IV стадии заболевания; 2) большой размер опухоли. Кроме того, выявлена тенденция к статистической достоверности повышения частоты смертности при наличии такого фактора риска, как опухолевое поражение параметрия.
Многофакторный регрессионный анализ позволил нам выделить только один значимый фактор, оказавший влияние на частоту смертности. Это стадия ЖРПШМ (см. табл. 3).
Построенная регрессионная модель имела коэффициент детерминации 0,42 при р = 0,006, что позволяет использовать ее на практике. Чувствительность данной модели - 47 %, специфичность - 94 %, точ-
ность - 78 %. Для экзаменационной выборки чувствительность модели составила 60 %, специфичность - 90 %, точность - 81 %.
Заключение
С учетом полученных результатов можно сделать вывод о том, что при ранних стадиях заболевания выживаемость больных ЖПРШМ имеет сходные показатели с выживаемостью пациенток с АШМ на тех же стадиях (26,3 ± 22,5 и 31,5 ± 14,0 % соответственно). При
поздних стадиях выживаемость больных ЖПРШМ хуже, чем выживаемость пациенток с АШМ (10,9 ± 14,6 и 31,2 ± 25,2 % соответственно). ПлРШМ в целом имеет более благоприятный прогноз, чем АШМ и ЖПРШМ.
Данные, представленные в настоящем обзоре, свидетельствуют об актуальности темы и необходимости проведения дальнейших, более детальных и глубоких исследований в этой области и рассмотрения вопроса о том, что все случаи ЖПРШМ должны интерпретироваться как высокоагрессивные.
Р Е К О М Е Н Д УЕМАЯ ЛИТЕРАТУРА
1. Бохман Я.В. Руководство по онкогинекологии. Л.: Медицина, 1989.
2. Давыдов М.И., Аксель Е.М. Статистика злокачественных новообразований в России и странах СНГ в 2006 г. Вестн РОНЦ им. Н.Н. Блохина РАМН 2008;19(2).
3. Hopkins M.P., Smith H.O. Chapter II. Adenocarcinoma of the cervix.
In: Gynecologic cancer. Controversies in management. Ed. by Gershenson D.M. et al., 2004. P. 149-60.
4. Wang S.S., Sherman M.E., Hildesheim A. Cervical adenocarcinoma and squamous cell carcinoma incidence trends among white woman and black woman in the United States for 1976-2000. Cancer 2004;100:1035-44.
5. Бохман Я.В. Клиническая онкология для семейного врача. СПб., 1995. С. 62-9.
6. Aoki Y., Sasaki M., Watanabe M., et al. High-risk group in node-positive patients with stage IB, IIA, and IIB cervical carcinoma after radical hysterectomy and postoperative pelvic irradiation. Gynecol Oncol 2000;77:305-9.
7. Fruhling L., Korn R., LaVillaureix J. et al. La myoendocardite chronique fibroelastique du nouveau-ne et du nourisson. Ann D’anat Pathol 1962;7(1).
8. Яковлева ИА., Черный А.П., Ботнарь Э.Р. Эпителий шейки матки в процессе малигни-зации. Кишинев: Штиинца, 1981.
9. Platz C.E., Benda J.A. Femall genetal tract cancer. Cancer 1995;75:270-94.
10. Hale R.J, Wiicox F.L, Buskley C.H. et al. Prognostic factors in uterine cervical carcinoma: A clinicopathological analysis.
Int J Gynecol Cancer 1991;1:1923.
11. Yazigi R., Sandstad J., Munoz A.K. et al. Adenosquamous carcinoma of the cervix:
prognosis in stage IB. Obstet Gynecol 1990;75:1012-5.
12. Fujiwara H., Mitchell M.P., Arseneau J. Clear cell adenosquamous carcinoma
of the cervix. Cancer 1995;76(9):1591-600.
13. Harrison T.A., Sevin B.U., Koechli O. et al. Adenosquamous carcinoma of the cervix: prognosis in early stage disease treated by radical hysterectomy. Gynecol Oncol 1993; 50:310-5.
14. Shingleton H.M., Bell M.S., Fremgen A. et al. Is there really a difference in survival of women with squamous cell carcinoma, adenocarsinoma, and adenosquamous cell carcinoma of the cervix? Cancer 1995;76:1948-55.
15. Бохман Я.В., Лютра У.К. Рак шейки матки. Кишинев: Штиинца, 1991.
16. Новик В.И. Эпидемиология и профилактика рака шейки матки. Медлайн-экспресс, 2008;(5):36-41.
17. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ Statistica.
М.: МедиаСфера, 2003.
18. Соколовский P.M. Carcinoma in situ шейки матки. В кн.: Вопросы патологической анатомии (труды ЛСГМИ). Л., 1963.
19. Ульрих Е.А., Урманчеева А.Ф. Онкологические аспекты заместительной менопаузальной гормональной терапии. Практ онкол 2009;10(2):76-83.
20. Чиссов В.И., Дарьялова Л.С. Клинические рекомендации. Онкология. М.: ГЭОТАР-Медиа, 2006.
21. Хмельницкий O.K. Цитологическая
и гистологическая диагностика заболеваний шейки и тела матки. СПб.: СОТИС, 2000.
22. Юнкеров В.И., Григорьев С.Г. Математико-статистическая обработка
данных медицинских исследований. 2-е изд., доп. СПб.: ВМедА, 2005.
23. American Cancer Society: Cancer facts and figures 2007. Atlanta, 2007. www.cancer.org
24. Christopherson W.M., Nealon N.,
Gray L.A. Noninvasive precursor lesions of the adenocarcinoma and mixed adenosquamous carcinoma of the cervix uteri. Cancer 1979;44:975-83.
25. Farley J.H., Hickey K.W., Carlson J.W.
et al. Adenosquamous histology predicts a poor outcome for patients with advanced-stage, but not early-stage, cervical carcinoma. Conference: Armed Forces District Meeting, Hawaii, 19 October 2002.
26. Gallup D.G., Harper R.H., Stock R.J.
Poor prognosis in patients with adenosquamous cell carcinoma of the cervix. Obstet Gynecol 1985;65:416-22.
27. Ishikawa H., Nakanishi T., Inoue T., Kuzuya K. Prognostic factors of adenocarcinoma of the uterine cervix. Gynecol Oncol 1999;73:42-6.
28. Look K.Y., Brunetto V.L., Clarke-Pearson D.L. et al. An analysis of cell type in patients with surgically staged stage IB carcinoma of the cervix: a Gynecologic Oncology Group study. Gynecol Oncol 1996;63:304-11.
29. Steiner G., Friedell H. Adenosquamous carcinoma in situ of the cervix. Cancer 1965;7:807-10.
30. Vizcaino A.P., Moreno V., Bosch F.X. et al. International trends in the incidence of cervical cancer: I. Adenocarcinoma and adenosquamous cell carcinomas. Int J Cancer 1998;75:536-45.
31. Waggoner S.E. Cervical cancer. Lancet 2003;361:2217-25.
– злокачественная неоплазия, формирующаяся из клеток плоского эпителия, приобретающих различную степень атипии. Плоскоклеточный рак шейки матки может носить «немое» течение. В клинически выраженных случаях проявляется кровянистыми выделениями, белями разного характера, при запущенном онкопроцессе – болями в области таза, нарушением функции мочевого пузыря и прямой кишки. Патология диагностируется по данным вагинального осмотра, ПАП-теста, кольпоскопии, биопсии, определения уровня онкомаркера SCС в крови. Методы лечения плоскоклеточного РШМ - хирургические вмешательства (конизация шейки матки, трахелэктомия, гистерэктомия), химиолучевая терапия.

Общие сведения
Плоскоклеточный рак шейки матки – гистологическая разновидность цервикального рака , происходящего из многослойного плоского эпителия, выстилающего влагалищную часть шейки матки. В структуре инвазивного РШМ данный гистологический тип диагностируется в 70-80% случаев, в 10-20% встречается аденокарцинома шейки матки, в 10% - низкодифференцированный рак, прочие злокачественные опухоли шейки матки составляют менее 1%. Максимальная заболеваемость плоскоклеточным раком шейки матки приходится на женщин в возрасте 40-60 лет. Длительный период «немого» течения приводит к тому, что свыше 35% случаев плоскоклеточного рака шейки матки диагностируется уже в запущенной стадии, что оказывает негативное влияние на прогноз и исход заболевания. Разработка стратегии профилактики и проведение массового скрининга женского населения на РШМ являются приоритетными задачами практической гинекологии и онкологии .

Причины плоскоклеточного рака шейки матки
Однозначные причины возникновения плоскоклеточного рака шейки матки не определены, однако на современном этапе достаточно хорошо изучены факторы, запускающие процесс малигнизации многослойного плоского эпителия. В первую очередь, к таким факторам принадлежит вирус папилломы человека (HPV), главным образом 16 и 18 типов, реже - 31 и 33 типов. В большинстве случаев при плоскоклеточном раке шейки матки идентифицируется HPV-16. Среди других вирусных агентов, передаваемых половым путем, роль онкогенов могут играть вирус простого герпеса II типа, цитомегаловирус и др. Фоновыми процессами, при которых в дальнейшем может развиваться плоскоклеточный рак шейки матки, служат эрозия, эктропион , полип цервикального канала , лейкоплакия , цервицит и др.
Кроме этого, клеточному перерождению способствуют и другие факторы: гормональные расстройства, курение, прием иммуносупрессоров (глюкокортикостероидов, цитостатиков), иммунодефицит. Определенную негативную роль играет травматизация шейки матки при многократных родах, установке ВМС , проведении оперативных вмешательств: абортов , диагностических выскабливаний, диатермокоагуляции и диатермоконизации и пр. В группу риска по возникновению плоскоклеточного рака шейки матки входят женщины, рано начавшие сексуальную жизнь, часто меняющие половых партнеров, пренебрегающие методами барьерной контрацепции, перенесшие ЗППП.
Классификация плоскоклеточного рака шейки матки
Внутри рассматриваемого гистологического типа выделяют плоскоклеточный с ороговением и плоскоклеточный без ороговения РШМ. В микроскопическом отношении плоскоклеточный ороговевающий рак шейки матки отличается наличием признаков кератинизации клеток – «раковых жемчужин» и кератогиалиновых гранул. Эпителиальные клетки аномально крупные, плеоморфные, с неровными контурами. Митотические фигуры представлены скудно. В препаратах неороговевающего плоскоклеточного рака шейки матки отсутствуют кератиновые «перлы». Раковые клетки преимущественно крупные, полигональной или овальной формы. Отмечается их высокая митотическая активность. Степень дифференцировки РШМ может быть высокой, умеренной или низкой.
С учетом направления опухолевого роста различают экзофитную, эндофитную и смешанную формы плоскоклеточного рака шейки матки. Язвенно-инфильтративная форма характерна для запущенных стадий РШМ; обычно она формируется при распаде и некрозе эндофитно растущей опухоли.
В своем развитии РШМ проходит четыре клинических стадии. Также выделяют нулевую, или начальную стадию (внутриэпителиальный рак), при которой поражаются только клетки покровного эпителия без инвазии в базальную пластинку. Первая стадия подразделяется на два периода: микроинвазивный рак с глубиной проникновения в строму до 3 мм (стадия 1А) и инвазивный рак с инвазией более 3 мм (стадия 1В). Признаком второй стадии служит распространение опухолевого процесса на тело матки. Третью стадию РШМ характеризует прорастание опухоли в малый таз; при сдавлении или обтурации мочеточника развивается гидронефроз . В течение четвертой стадии отмечается инвазия в прямую кишку и крестец, распад опухоли, появление отдаленных метастазов .
Симптомы плоскоклеточного рака шейки матки
В нулевой и 1А стадии клинические проявления РШМ, как правило, отсутствуют. В этот период диагностика плоскоклеточного рака шейки матки возможна во время планового обследования у врача-гинеколога. В дальнейшем, по мере углубления инвазии и экспансивного роста опухоли появляется характерная патологическая триада: бели, кровотечения и болевой синдром. Выделения из половых путей могут иметь различный характер: быть серозными прозрачными или с примесью крови (в виде «мясных помоев»). В случае присоединения инфекции или распада опухолевого узла бели могут приобретать мутный, гноевидный характер и зловонный запах.
Кровотечение из половых путей при плоскоклеточном раке шейки матки различаются своей интенсивностью – от мажущих выделений до ациклических или менопаузальных кровотечений. Чаще кровотечения имеют контактное происхождение и провоцируются гинекологическим осмотром, половым актом, спринцеванием, натуживанием при дефекации.
Болевой синдром при плоскоклеточном раке шейки матки также может носить различную выраженность и локализацию (в области поясницы, крестца, промежности). Как правило, он свидетельствует о запущенности онкопроцесса, прорастании параметральной клетчатки и поражении поясничных, крестцовых или копчиковых нервных сплетений. При прорастании рака в соседние органы могут отмечаться дизурические расстройства, запоры, образование мочеполовых свищей. В терминальной стадии развивается раковая интоксикация и кахексия.
Диагностика плоскоклеточного рака шейки матки
Клинически «немые» формы плоскоклеточного рака шейки матки можно обнаружить при проведении кольпоскопии или по результатам цитологического ПАП-мазка. Важную роль в диагностике играет тщательно собранный гинекологический анамнез (количество сексуальных партнеров, родов, абортов, перенесенные ЗППП), а также обнаружение высокоонкогенных штаммов ВПЧ в исследуемом соскобе методом ПЦР.
При осмотре в зеркалах плоскоклеточный рак шейки матки определяется в виде папилломатозного или полиповидного разрастания либо язвенного образования. Эдофитные опухоли деформируют шейку матки, придавая ей бочкообразную форму. При контакте новообразование кровоточит. Для определения стадии онкозаболевания и исключения метастазов в органы малого таза проводится двуручное влагалищное и влагалищно-прямокишечное исследование. Во всех случаях обнаружения патологически измененной шейки матки в обязательном порядке проводится расширенная кольпоскопия , забор мазка на онкоцитологию, прицельная биопсия и выскабливание цервикального канала . Для морфологического подтверждения диагноза биоптат и соскоб направляются на гистологическое исследование.
Определенную информативность имеет определение уровня SCC (маркера плоскоклеточного рака) в сыворотке крови. Методами уточняющей диагностики плоскоклеточного рака шейки матки, призванными оценить степень распространенности неоплазии и помочь в выборе оптимального метода лечения пациентки, служат трансвагинальное УЗИ , КТ или МРТ малого таза , экскреторная урография , - удаление матки с аднексэктомией . При III–IV стадиях плоскоклеточного рака шейки матки стандартом является химиолучевая терапия (лучевое лечение + цисплатин), однако некоторые авторы допускают потенциальную возможность оперативного лечения. При поражении мочеотводящих путей может потребоваться проведение стентирования мочеточника.
В функционально неоперабельных случаях, обусловленных сопутствующими заболеваниями, назначается внутриполостная лучевая терапия . При рецидивах РШМ показано выполнение экзентерации малого таза, проведение паллиативной химиолучевой и симптоматической терапии.
Прогноз и профилактика
По окончании лечения динамическое наблюдение за пациенткой производится ежеквартально в течение первых 2-х лет, а затем раз в полгода до 5-летнего срока. Если плоскоклеточный рак шейки матки обнаружен на нулевой стадии, то своевременно проведенное лечение дает шансы на практически 100% выздоровление. Процент безрецидивной пятилетней выживаемости при РШМ I стадии составляет 85%, II стадии – 75%, III - менее 40%. При IV стадии заболевания можно говорить лишь о продлении жизни, но не излечении. Рак культи шейки матки развивается менее чем у 5% пациенток.
Профилактика плоскоклеточного рака шейки матки заключается в проведении массового и регулярного цитологического скрининга женского населения, диспансеризации женщин, имеющих фоновые и предраковые заболевания шейки матки . Большую превентивную роль играет отказ от курения, предупреждение ЗППП и проведение профилактический вакцинации против РШМ в подростковом возрасте.
Раком считается опухолевый процесс злокачественного характера, произрастающий из тканей эпителия. Эти ткани располагаются не только на кожной поверхности, как ошибочно полагают многие, но и выстилают поверхности репродуктивной системы, мочевыводящих и воздухопроводящих путей, пищеварительного тракта и пр.
Все эти структуры определенным способом сообщаются с внешней средой, вредными и канцерогенными веществами, что повышает вероятность злокачественной онкологии. Существует несколько разновидностей рака, но плоский эпителий поражает плоскоклеточный рак.
Понятие
Плоскоклеточным раком называют злокачественный опухолевый процесс, развивающийся из эпителия кожи или слизистых тканей.
Подобной онкологической форме свойственно агрессивное течение со стремительным развитием.
Онкопроцесс начинается в кожном либо слизистом слое, но очень быстро распространяется на лимфоузлы местного значения, соседние ткани и органические структуры, разрушая их строение и подрывая их деятельность. В результате формируется недостаточность полиорганного масштаба, ведущая к смерти.
Среди всех разновидностей слизистого и на долю плоскоклеточной онкологии приходится порядка четверти случаев. Примерно в 75% подобный рак характеризуется локализацией в зоне головы и лица. Патология более характерна для пациентов пожилого возраста (старше 65) преимущественно мужского пола.
Какие органы поражает?
Как уже говорилось, плоскоклеточный рак обычно поражает органы, имеющие плоский эпителий.
Подобные структуры присутствуют в различных системах и органах:
- и влагалище;
- и пр.
Самым распространенным считается плоскоклеточный легочный рак, затем следует злокачественная шеечная онкология. Плоскоклеточная онкология занимает одно из первых мест по распространенности, поэтому является серьезной проблемой.
Классификация
Плоскоклеточная онкология классифицируется по нескольким принципам.
По распространенности рак бывает инвазивным и микроинвазивным.
По степени клеточной дифференцировки различают ороговевающий, неороговевающий и низкодифференцированный плоскоклеточный рак.
Классифицируют плоскоклеточный рак и по стадиям, форме опухоли и пр.
Плоскоклеточный ороговевающий рак
Для этой онкоформы свойственно медленное развитие и рост. Основным ее отличием является наличие дифференцированных онкоклеток, из которых эта раковая опухоль и состоит. Она формируется из «жемчужин» – ограниченных структур, имеющих серовато-белую блестящую поверхность.
Подобная форма плоскоклеточного рака с прогностической точки зрения условно считается наиболее благоприятной.
Ороговевающий рак может иметь высоко- или умереннодифференцированную форму. Причем с повышением степени дифференциации повышается и благоприятность прогнозов, потому как такие образования прогрессируют значительно медленней.
Еще одним характерным проявлением дифференцированного плоскоклеточного рака является наличие чешуйчатых ороговевших частиц, располагающихся на внешней стороне образования и образующих желтоватую окантовку.
Ороговевающая форма плоскоклеточной онкологии практически всегда образуется на поверхности кожи, хотя в исключительных случаях может обнаружиться и в других структурах организма.
Неороговевающий
Неороговевающая форма плоскоклеточного рака составляет скопление недифференцированных клеточных структур, отчего отличается самым высоким показателем злокачественности, агрессивным течением и быстрым прогрессированием.
Вскоре после начала опухолевого процесса такой рак начинает активно метастазировать, поэтому его считают самой злокачественной плоскоклеточной онкологией.
Подобная раковая форма способна образовываться на любом органе, но все же чаще она встречается на слизистых тканях. На кожных покровах такая онкоформа выявляется всего лишь в 1 случае из 100, т. е. в 10%.
Низкодифференцированный
Плоскоклеточная онкология низкодифференцированного типа имеет много общего с , поскольку состоит из веретенообразных клеточных структур.
Такой рак отличается повышенной злокачественностью и быстрым прогрессированием.
Микрофото низкодифференцированного плоскоклеточного рака

Для низкодифференцированного рака плоскоклеточного типа характерна локализация преимущественно на слизистых тканях различных органических структур.
Железистый
Железисто-плоскоклеточная плоскоклеточная онкология обычно формируется на органических структурах, имеющих помимо слизистых оболочек разветвленную железистую сеть, например, в матке или легочных тканях.
Опухоль, кроме плоскоклеточного эпителиального компонента, содержит еще и железистые структуры, что негативно отражается на течении онкопроцесса.
Чаще всего подобная плоскоклеточная онкоформа локализуется в тканях матки, характеризуется агрессивным и стремительным прогрессированием, имеет неблагоприятные прогнозы.
Инвазивный
Высокий показатель инвазивности говорит о способности онкопроцесса прорастать в соседние с опухолью структуры и местные лимфоузлы.
Инвазивный рак имеет менее благоприятные прогнозы, нежели неинвазивный, но при раннем выявлении неплохо поддается специфической комплексной противоопухолевой терапии.
Причины
Сложно точно определить причины развития плоскоклеточной онкологии. Немалое значение в этом процессе имеет патологически низкая сопротивляемость раковым клеткам и наличие специфических повреждающих факторов вроде:
- Радиоактивного облучения (у лиц, занятых на атомном производстве, при злоупотреблении диагностическими процедурами с применением рентгена, гама-лучей и пр.);
- Агрессивной экологической среды (загрязненная атмосфера вблизи от промышленных предприятий, а также в крупных мегаполисах);
- Злоупотребления ультрафиолетом (частое и многочасовое пребывание на солнце или в солярии вызывает генетические мутации, провоцирующие возникновение аномальных злокачественных клеток);
- Генетической склонности;
- Приема препаратов иммуносупрессивного действия, угнетающих иммунитет (Меркаптопурин или Азатиоприн);
- Нездоровых привычек в питании;
- Наличия производственных вредностей (у шахтеров, трубочистов, металлургов или на деревообрабатывающих производствах);
- Инфекционных поражений (ВИЧ или );
- Возрастных особенностей (после 65).
Кроме того, повышают вероятность возникновения плоскоклеточного рака разного рода предраковые патологические кожные состояния вроде , или старческого , кератоакантомы и пр.
Симптомы
 Клинические проявления плоскоклеточной онкологии обуславливаются конкретной локализацией опухолевого процесса, однако, все типы такого рака имеют и некоторые общие характеристики.
Клинические проявления плоскоклеточной онкологии обуславливаются конкретной локализацией опухолевого процесса, однако, все типы такого рака имеют и некоторые общие характеристики.
Плоскоклеточный рак может развиваться в нескольких клинических формах: инфильтративно-язвенной, папиллярной или смешанной.
- Инфильтративно-язвенная или эндофитная клиническая форма плоскоклеточного рака отличается наличием изъязвлений первичного узлового очага, на котором образуется крупная язва. Для нее свойственны неправильные очертания, края более плотные и располагаются выше центра, дно язвы белесое, шероховатое и источает зловоние. Опухолевый процесс растет и распространяется инвазивно, т. е. прорастает вглубь тканей, поэтому внешне язва практически не увеличивается. Зато быстро поражаются мышечные и костные ткани, близлежащие структуры и пр.
- Папиллярная или экзофитная клиническая плоскоклеточная онкоформа отличается наличием четко отграниченного от соседних структур узелкового очага, который постепенно растет, приобретая все большие размеры. В итоге формируется опухоль красно-коричневого оттенка, похожая на цветную капусту. Она имеет бугристые неровные поверхности с четко заметной выемкой в центре. Подобные опухоли бывают на ножке или на широком основании, постепенно может разрастаться и переходить в инфильтративно-язвенную клиническую форму.
Остальные клинические признаки обуславливаются расположением опухолевого процесса. Например, плоскоклеточный кожный рак характеризуется наличием болезненной и зудящей опухоли, кровоточащей, с отеками и покраснениями вокруг очага.
Рак легкого подобного типа сопровождается хриплым голосом и неизлечимым кашлем, беспричинным похудением и болезненными ощущениями в груди, отхождением слизистой и кровянистой мокроты и постоянной гипертермией.
А для плоскоклеточного рака матки свойственно наличие маточных кровотечений и белей, болезненности в зоне живота и таза, отдающей в поясницу и промежность, хронической усталости и общей слабости организма.
Стадии
Развитие и течение плоскоклеточного рака происходит в несколько этапов:
- Нулевая стадия – характеризуется отсутствием первичного опухолевого очага, метастаз в лимфоузлах и других органах;
- Первая стадия – когда опухоль имеет размеры до 5 см, а метастазы в лимфоузловых и прочих органических структурах по-прежнему отсутствуют;
- Вторая стадия – опухоль больше 5 см либо она имеет любой размер и проросла в ближайшие структуры, хотя любое метастазирование отсутствует;
- Третья стадия – определяется при любых размерах опухоли при наличии лимфоузлового метастазирования, но в других органах метастаз нет;
- Четвертая стадия выявляется, если опухоль имеет любой размер, может прорасти в соседние ткани, с наличием или без лимфоузлового метастазирования, но с обязательными метастазами в другие отдаленные органические структуры.
Диагностика
 Диагностические исследования плоскоклеточной онкологии включают следующие процедуры:
Диагностические исследования плоскоклеточной онкологии включают следующие процедуры:
Любое расположение плоскоклеточной онкологии предполагает использование следующих терапевтических методик:
- – предполагает применение противоопухолевых препаратов;
- – основывается на использовании в лечении облучения гамма-лучами;
- Хирургическое вмешательство – предполагает удаление самой опухоли и метастазных лимфоузловых структур.
Если образование небольшого размера, то показано оперативное удаление, после которого рекомендуется пройти профилактический курс лучевой или химиотерапии. Если же образование слишком крупное и неоперабельное, то для его уменьшения также назначается радиолечение, затем опухоль удаляют, а уже после этого назначается курс химиотерапии для уничтожения оставшихся онкоклеток.
При небольших поверхностных опухолях могут применяться альтернативные методы терапии вроде электрокоагуляции, фотодинамической терапии или криолечения. После полученного лечения пациент периодически посещает онколога, чтобы избежать рецидива.
Прогнозы при плоскоклеточном раке обуславливаются расположением онкопроцесса и его стадией:
- РШМ при первой стадии 90% выживаемости, при второй – 60%, при третьей – 35%, при четвертой – 10%;
- Легочный плоскоклеточный рак характеризуется выживаемостью на первой стадии – около 35-40%, на второй – 15-30%, на третьей – 10%;
- Рак кожи при I-III стадии – 60% выживаемости, на 4 стадии – 40%.
Выявленные на ранних этапах опухоли обычно проще поддаются лечению и имеют более положительные прогнозы, нежели запущенные раковые образования.
Осторожно! Видео операции по удалению плоскоклеточного рака (нажмите чтобы открыть)
Карциномы известны человечеству с незапамятных времен. Первые упоминания о таких опухолях можно найти в папирусах древних египтян, а Гиппократ определил их название – карцинома, так как внешне они имели сходство с крабом. Позднее Цельс перевел термин на латынь, так возник «рак». Еще в древности карциному считали неизлечимым заболеванием, но уже тогда предлагалось удалять пораженные опухолью ткани в ранних стадиях, а запущенные случаи не лечить вовсе.
Время шло, представления менялись, однако и сегодня карцинома остается зачастую неизлечимым заболеванием. Чем больше ученые узнают о ней, тем больше возникает новых вопросов. Даже современные методы диагностики не всегда способны выявить рак на ранней стадии, а лечение часто не приносит ожидаемых плодов.
Злокачественные опухоли считают лидерами по числу смертей во всем мире, первое место они уступили лишь болезням сердечно-сосудистой системы, а среди всех неоплазий карцинома – наиболее частая разновидность.
Термином «рак» в медицине обозначают злокачественные опухоли из эпителия. Это понятие тождественно карциноме.
Такие новообразования имеют своеобразное строение, подчиняются некоторым общим механизмам развития и поведения. Источником их могут стать кожа, слизистые оболочки, паренхима внутренних органов, состоящая из высокоспециализированных в функциональном отношении клеток (печень, поджелудочная железа, легкие и т. д.). Часто люди, не имеющие отношения к медицине, называют раком и другие опухоли, например, из костной, мышечной или нервной ткани, однако, это неверно. В этой статье мы попробуем разобраться, что же такое карцинома (рак), где она растет и как с ней бороться.
Карциномы встречаются намного чаще всех других видов злокачественных новообразований, и этому есть свое объяснение. Дело в том, что эпителий, покрывающий внутреннюю поверхность многих органов либо составляющий верхний слой кожи, постоянно обновляется, а это сопряжено с непрерывным делением клеток. Чем интенсивнее делятся и размножаются клетки, тем больше вероятности, что на каком-то этапе может произойти сбой, и это послужит причиной появления спонтанной генетической мутации. Мутировавшая клетка дает начало целому клону новых, измененных, с нехарактерным строением или свойствами, которые, к тому же, способны делиться неограниченное количество раз. Так, за короткое время возникнет образование, отличное по строению от эпителия, из которого оно произошло, а способность интенсивно увеличиваться, врастать в окружающее пространство, разноситься посредством крови или лимфы по всему организму и предопределит его злокачественный характер.

Другой возможной причиной распространенности опухолей из эпителия можно считать высокую вероятность контакта с . Так, кожа испытывает на себе всевозможные влияния окружающей среды (солнце, бытовая химия, ветер), эпителий желудочно-кишечного тракта постоянно контактирует с канцерогенами, содержащимися в пище, в легкие попадает загрязненный воздух и табачный дым, а печень вынуждена перерабатывать разнообразные токсические вещества, лекарства и т. д., в то время как сердечная мышца или нервная ткань мозга ограничены от таких опасностей барьерами.
Эпителий женских половых органов и предстательной железы подчиняются действию гормонов, которые вызывают там сложные превращения, поэтому при любых гормональных сбоях, особенно вероятных у возрастных пациентов, может произойти нарушение созревания эпителиальных клеток.
Карцинома не появляется внезапно на неизмененном эпителии, ей всегда предшествует предраковое изменение. Поскольку далеко не каждый мчится к врачу при появлении каких-либо жалоб, а отдельные виды предрака и вовсе протекают бессимптомно, то и случаи, когда диагностируется сразу опухоль, минуя ее предшественников, нередки.

стадии предраковых изменений на примере шейки матки
К предопухолевым изменениям относят дисплазию, лейкоплакию, атрофические или гиперпластические процессы, но наибольшее значение имеет дисплазия, тяжелая степень которой, по сути, является «раком на месте», то есть неинвазивной формой рака.
Виды опухолей из эпителия
Карциномы чрезвычайно разнообразны, как по внешнему виду, так и по микроскопическим признакам, однако на основе общих свойств они были классифицированы в группы.
Внешне опухоль может напоминать узел либо расти в виде инфильтрата, внедряясь в окружающие ткани, четкие границы для рака не свойственны, а процесс нередко сопровождается выраженным воспалением и склонностью к изъязвлению, особенно на коже и слизистых оболочках.
В зависимости от вида эпителия, давшего начало карциноме, принято выделять :
- Аденокарциному – железистая опухоль, чаще поражающая слизистые оболочки и железы (желудок, бронхи, и т. д.).
- Плоскоклеточный рак (ороговевающий или неороговевающий), источником которого становится многослойный плоский эпителий кожи, гортани, шейки матки, а также участки метаплазии на слизистых оболочках, когда появляются очаги плоского эпителия там, где его быть не должно.
- Смешанные формы – так называемые диморфные раки, в которых обнаруживаются и плоскоклеточный, и железистый компоненты, каждый из которых несет признаки злокачественности.

Могут иметь самое разное строение, напоминая те или иные структуры здоровых тканей, поэтому выделены отдельные их виды:
- Папиллярная карцинома – когда опухолевые комплексы образуют ветвящиеся сосочковые разрастания (напр. в ).
- Тубулярная аденокарцинома – опухолевые клетки складываются в подобие трубочек и протоков.
- Ацинарная – напоминает ацинусы или округлые скопления клеток рака.
В зависимости от степени зрелости опухолевых клеток, железистая карцинома может быть высоко-, умеренно- и низкодифференцированной. Если строение опухоли приближено к здоровому эпителию, то говорят о высокой степени дифференцировки, в то время как низкодифференцированные опухоли подчас теряют сходство с изначальной тканью, из которой образовались. Всегда в карциномах присутствуют такие признаки злокачественности как атипия клеток, увеличенное, крупное и темноокрашенное ядро, обилие неполноценных (патологических) митозов (делящихся ядер), полиморфизм (одна клетка не похожа на другую).
Плоскоклеточная карцинома устроена несколько иначе. В ней можно найти поля многослойного плоского эпителия, но состоящего из измененных, атипичных клеток. В более благоприятных случаях такой раковый эпителий сохраняет способность к образованию рогового вещества, которое скапливается в виде жемчужин, тогда говорят о дифференцированной разновидности плоскоклеточного рака – ороговевающем. Если такой способности эпителий лишен, то рак будет называться неороговевающим и иметь низкую степень дифференцировки.
Описанные разновидности устанавливаются с помощью гистологического исследования фрагментов опухолевой ткани после биопсии или удаления ее в процессе операции, а внешний вид может лишь косвенно указывать на степень зрелости и строение карциномы.
Чем ниже дифференцировка, то есть развитие раковых клеток, тем более злокачественна опухоль, поэтому так важно произвести микроскопическое ее исследование и описать все характеристики.
Наибольшие сложности могут возникнуть при диагностике низкодифференцированной карциномы , когда клетки в такой степени разнообразны либо, наоборот, имеют практически одинаковый вид, что не укладываются ни в один из выше перечисленных вариантов рака. Однако, отдельные формы все же удается выделить: слизистый, солидный, мелкоклеточный, фиброзный (скирр) и т. д. Если строение опухоли не соответствует ни одному из известных типов, то ее называют неклассифицируемой карциномой.

высокодифференцированная карцинома (слева) и низкодифференцированная (справа) – в первом случае отличие раковых клеток очевидно визуально
Особенности основных видов низкодифференцированных карцином:
- Слизистый рак , нередко встречающийся в желудке или яичниках, способен образовывать огромное количество слизи, в которой клетки карциномы и погибают.
- Солидная карцинома состоит из клеток, «уложенных» в подобие балок, ограниченных прослойками соединительной ткани.
- Мелкоклеточная карцинома представляет скопления клеток, напоминающих лимфоциты, и характеризуется крайне агрессивным течением.
- Для фиброзного рака (скирр) свойственно значительное количество соединительнотканной стромы, что делает его очень плотным.
Из желез внутренней и внешней секреции могут развиваться неоплазии, клетки которых сохраняют сходство с исходной тканью органа, например, гепатоцеллюлярная карцинома, и растущая крупным узлом либо множеством мелких узелков в паренхиме органа.
В редких случаях можно обнаружить так называемую карциному невыясненного происхождения . По сути, это , первоначальное расположение которого установить так и не удалось даже при привлечении всех существующих методов исследований.

метастазирование рака – одна из причин появления карцином невыясненного происхождения
Карциномы из неизвестного источника чаще находят в , печени, лимфатических узлах. В такой ситуации решающее значение может иметь биопсия и иммуногистохимическое исследование фрагментов опухоли, позволяющее определить в ней наличие белков, свойственных конкретному виду рака. Особую сложность представляет диагностика низкодифференцированных или недифференцированных форм таких карцином, когда их строение не имеет сходства с предполагаемым источником метастазирования.
Говоря о злокачественных опухолях, важно определить понятие инвазивности . Переход предракового процесса в карциному сопровождается изменениями, свойственными раку, во всей толще эпителиального пласта, но при этом за его пределы опухоль может не выходить и не прорастать базальную мембрану – «рак на месте», карцинома «in situ». Так до поры до времени ведет себя протоковая карцинома молочной железы или рак «in situ» шейки матки.

Ввиду агрессивного поведения, способности клеток неограниченно делиться, вырабатывать разнообразные ферменты и биологически активные вещества, карцинома, преодолев стадию неинвазивного рака, прорастает сквозь базальную мембрану, на которой располагался эпителия, внедрятся в подлежащие ткани, разрушает стенки кровеносных и лимфатических сосудов. Такую опухоль будут называть инвазивной.
Немного подробностей
Одной из наиболее распространенных злокачественных эпителиальных опухолей является , встречающаяся преимущественно среди мужского населения Японии, России, Беларуси, стран Прибалтики. Строение ее в большинстве случаев соответствует аденокарциноме – железистой опухоли, которая может быть сосочковой, тубулярной, трабекулярной и т. д. Среди недифференцированных форм возможно обнаружение слизистого (перстневидноклеточного рака), а такая разновидность как плоскоклеточная карцинома в желудке встречается крайне редко.

развитие карцином на эпителии желудка/кишечника
также нельзя назвать редкой патологией. Диагностируется она не только у пожилых, но и у молодых пациенток репродуктивного возраста на фоне разнообразных предраковых процессов (псевдоэрозия, лейкоплакия), вирусного поражения или рубцовых деформаций. Поскольку большая часть шейки покрыта многослойным плоским эпителием, то наиболее вероятно развитие здесь плоскоклеточного рака, а для цервикального канала, который ведет внутрь матки и выстлан железистым эпителием, больше свойственна аденокарцинома.
чрезвычайно разнообразны, но самым частым вариантом по праву считается базально-клеточная карцинома (базалиома). Это новообразование поражает людей пожилого возраста, а излюбленным местом локализации является лицо и шея. Базалиома имеет особенность: при наличии признаков злокачественности в клетках и способности врастать в подлежащие ткани, она никогда не метастазирует, а очень медленно растет и проявляет склонность к рецидивированию или образованию множественных узелков. Эту форму рака можно считать благоприятной в отношении прогноза, но только при условии своевременного обращения к врачу.

Светлоклеточная разновидность карциномы является самой частой . Название ее говорит о том, что состоит она из светлых клеток различной формы, внутри которых обнаруживаются включения жира. Этот рак растет быстро, рано дает метастазы и склонен к некрозам и кровоизлияниям.
представлена разнообразными формами, среди которых выделяют дольковую и протоковую разновидности, являющиеся «раком на месте», то есть неинвазивными вариантами. Такие опухоли начинают свой рост в пределах дольки или млечного протока, долгое время могут не давать о себе знать и не проявляться никакими симптомами.

протоковая (слева) и дольковая (справа) карциномы молочной железы, различие – в зоне появления атипичных раковых клеток
Момент развития инфильтрирующей карциномы молочной железы характеризует прогрессирование заболевания и переход его в следующую, более тяжелую стадию. Боль и другие симптомы для инвазивного рака не свойственны, а женщины часто сами обнаруживают новообразование (либо при прохождении плановой маммографии).
Особую группу злокачественных опухолей составляют нейроэндокринные карциномы . Клетки, из которых они образуются, рассеяны по всему организму, а функция их заключается в образовании гормонов и биологически активных веществ. При опухолях из нейроэндокринных клеток появляется характерная симптоматика, зависящая от типа образуемого опухолью гормона. Так, возможны тошнота, диарея, подъемы артериального давления, гипогликемия, истощение, развитие язв желудка и др. По своим клиническим особенностям нейроэндокринные карциномы чрезвычайно разнообразны.
Всемирной организацией здравоохранения было предложено выделять:

- Высокодифференцированные нейроэндокринные карциномы доброкачественного течения;
- Высокодифференцированные карциномы с низкой степенью злокачественности;
- Низкодифференцированные опухоли с высокой степенью злокачественности (крупноклеточная и мелкоклеточная нейроэндокринная карцинома).
Карциноидные опухоли (нейроэндокринные) чаще встречаются в органах желудочно-кишечного тракта (аппендикс, желудок, тонкий кишечник), легких, надпочечниках.
Уротелиальная карцинома – это переходно-клеточный , составляющий более 90% злокачественных новообразований этой локализации. Источником такой опухоли становится переходный эпителий слизистой оболочки, имеющий черты сходства с многослойным плоским и однослойным железистым одновременно. Уротелиальный рак сопровождается кровотечениями, дизурическими расстройствами и чаще выявляется у пожилых мужчин.
Метастазирование карцином происходит преимущественно лимфогенным путем, что связано с хорошим развитием лимфатической сети в слизистых оболочках и паренхиматозных органах. Первым делом, метастазы обнаруживают в близлежащих лимфоузлах (регионарных) по отношению к месту роста рака. При прогрессировании опухоли, врастании ее в кровеносные сосуды появляются и гематогенные отсевы в легкие, почки, кости, головной мозг и т. д. Наличие гематогенных метастазов при злокачественной эпителиальной опухоли (раке) всегда свидетельствует о далеко зашедшей стадии заболевания.
Как выявлять и как лечить?
Довольно разнообразны и зависят от места локализации опухоли. Так, для того чтобы заподозрить некоторые виды рака достаточно обычного осмотра ( , кожи), а для других опухолей на помощь онкологам приходят инструментальные и лабораторные методы исследования.

После осмотра и беседы с пациентом, врач всегда назначает проведение общего и биохимического анализа крови, мочи . В случае локализации карциномы в полостных органах прибегают к эндоскопии – фиброгастродуоденоскопия, цистоскопия, гистероскопия. Большой объем информации могут дать рентгенологические методы – рентгенография легких, экскреторная урография.
Для исследования лимфоузлов, распространения опухоли в окружающие ткани незаменимыми становятся КТ , МРТ , ультразвуковая диагностика .
В целях исключения метастазов обычно проводятся рентгенография легких, костей, УЗИ органов брюшной полости.
Самым информативным и точным способом диагностики считаются морфологические исследования (цитологическое и гистологическое) , позволяющие установить вид новообразования и степень его дифференцировки.
Современная медицина предлагает и цитогенетический анализ для обнаружения генов, свидетельствующих о высоком риске развития того или иного вида карциномы, а также определение в крови (простатспецифический антиген, SCCA при подозрении на плоскоклеточный рак и др.).

Ранняя диагностика рака основана на определении специфических опухолевых белков (маркеров) в крови пациента. Так, при отсутствии видимых очагов роста новообразования и повышении определенных показателей можно предположить наличие заболевания. Кроме того, при плоскоклеточных раках гортани, шейки матки, носоглотки обнаружение специфического антигена (SCC) может говорить о вероятности рецидивирования или прогрессирования опухоли.
Лечение карцином заключается в применении всех возможных методов борьбы с опухолью, а выбор остается за онкологом, врачом радиологом, хирургом.
Основным по-прежнему считается , а объем вмешательства зависит от размеров новообразования и характера его врастания в окружающие ткани. В тяжелых случаях хирурги прибегают к полному удалению пораженного органа (желудок, матка, легкое), а в ранних стадиях есть возможность произвести резекцию опухоли (молочная железа, печень, гортань).

и применимы не во всех случаях, поскольку разные виды карцином имеют разную чувствительность к этого рода воздействиям. В запущенных случаях эти методы призваны не столько удалить опухоль, сколько уменьшить страдания больного, вынужденного терпеть сильную боль и нарушение функции пораженных органов.
Прогноз при наличии карциномы всегда серьезен, однако в случаях обнаружения раннего рака и своевременного его лечения возможно полностью избавиться от проблемы. В других стадиях заболевания выживаемость пациентов снижается, появляется вероятность рецидивов рака и метастазирования. Для того, чтобы лечение и прогноз были успешными, нужно вовремя обращаться к специалисту, а при наличии предопухолевых поражений, повышенного риска развития опухоли, неблагоприятной семейной ситуации, пациент должен сам регулярно проходить соответствующие обследования и лечение, чтобы предотвратить развитие карциномы.
Автор выборочно отвечает на адекватные вопросы читателей в рамках своей компетенции и только в пределах ресурса ОнкоЛиб.ру. Очные консультации и помощь в организации лечения в данный момент не оказываются.