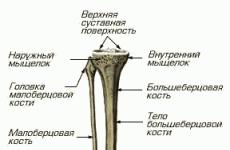
Отечный экзофтальм лечение. Следствие аутоиммунных заболеваний щитовидной железы или эндокринная офтальмопатия: лечение тяжелого поражения глаз. Лечение лёгкой ЭОП
Содержание
Пучеглазие – главный симптом эндокринной офтальмопатии. Это заболевание известно также как офтальмопатия Грейвса, получив название в честь ученого, который впервые описал признаки патологии. При данном состоянии поражаются задние (ретробульбарные) ткани органа зрения и мышцы глазного яблока, что приводит к его смещению. Проявляется патология пучеглазием, слезоточивостью, отечностью век, конъюнктивы. На запущенной стадии атрофируется зрительный нерв и значительно ухудшается зрение.
Как проявляется офтальмопатия Грейвса
В 95% случаях причиной поражения мягких тканей глазницы является диффузный токсический зоб, развивающийся из-за тиреотоксикоза, при котором щитовидная железа вырабатывает избыточное количество йодсодержащих гормонов. Офтальмопатия может проявится как во время заболевания, так и до его появления, и десять лет спустя. Механизмы, из-за которых поражаются ретробульбарные ткани, неясны. Считается, что пусковыми факторами являются бактериальная или ротавирусная инфекции, интоксикация организма, радиация, стрессы, курение, инсоляция.
Патология носит аутоиммунный характер. Так называют состояние, при котором иммунитет начинает атаковать и уничтожать здоровые ткани, приняв их за патогенные клетки. По одной из версий, иммунная система воспринимает клетчатку, которая окружает глазное яблоко, как носителя рецепторов йодсодержащих гормонов щитовидной железы. Это расценивается как ненормальное состояние, и чтобы ликвидировать проблему, иммунитет вырабатывает антитела для их уничтожения.

Проникнув в ткани глазницы, антитела вызывают воспаление с инфильтратом (скоплением чужеродных частиц). В ответ клетчатка синтезирует гликозаминогликаны – вещества, притягивающие жидкость. Результатом является отек тканей глаз и увеличение глазодвигательных мускулов, которые отвечают за давление в костной основе глазницы.
Это приводит к экзофтальму – смещению глазного яблока вперед и появлению пучеглазия. Иногда оно уходит в сторону, симптомом чего является косоглазие. Со временем воспаление стихает, инфильтрат преобразуется в соединительную ткань. На его месте формируется рубец, после появления которого смещение становится необратимым.
Чтобы этого избежать, важно вовремя заметить симптомы патологии, обратиться к эндокринологу и начать лечение основного недуга. На начальной стадии эндокринная офтальмопатия как самостоятельное заболевание не лечится. В тяжелых случаях может быть назначено хирургическое вмешательство. Это может быть операция на веках, глазодвигательных мускулах, декомпрессия орбит при экзофтальме.
Ранние признаки
Офтальмопатия при тиреотоксикозе имеет благоприятный прогноз в лечении: в 10% случаях наблюдается улучшение, в 60% – стабилизация состояния. По этой причине очень важно вовремя заметить ранние признаки заболевания. На начальной стадии патология проявляется следующими симптомами:
- «песок», чувство давления в органе зрения;
- слезотечение или сухость глаз;
- светобоязнь;
- отечность вокруг органа зрения;
- небольшое пучеглазие.

Стадия развернутых клинических проявлений
По мере развития эндокринной офтальмопатии ситуация ухудшается. Симптомом этого состояния является заметное увеличение глазных яблок, покраснение белка, припухлость век, раздвоение предметов. Из-за того, что глаза неспособны смыкаться до конца, образуются язвы на роговице, развиваются конъюнктивит и иридоциклит – воспаление радужной оболочки и ресничного тела. Часто развивается синдром сухого глаза.
На выраженной стадии эндокринной офтальмопатии атрофируется зрительный нерв, ограничивается подвижность глаза, из-за чего повышается внутриглазное давление и развивается псевдоглаукома. Может наблюдаться окклюзия (закупорка) вен сетчатки, что приводит к потере зрения. Если патологический процесс затрагивает мышцы органа зрения, нередко развивается косоглазие.
Классификация
Существует несколько типов классификации эндокринной офтальмопатии. В зависимости от проявлений симптоматики, выделяют три стадии патологии:
- Для первой степени характерно небольшое пучеглазие, когда глазное яблоко вперед выступает не больше, чем на 16 мм. Симптомами этой стадии является умеренный отек век, без нарушения работы глазодвигательных мускулов и конъюнктивы.
- Для второй степени эндокринной офтальмопатии характерно выступление глазного яблока на 18 мм. На этой стадии наблюдается сильный отек век, конъюнктивы, периодически двоится в глазах.
- Симптомом третьей степени является выраженное пучеглазие: отклонение вперед составляет до 21 мм. Больной не может полностью закрыть глаза, на роговице появляются эрозии, язвы, глазное яблоко теряет подвижность, атрофируется зрительный нерв.
Особенности симптоматики в зависимости от вида заболевания
В медицинской практике выделяют три формы патологии – тиреотоксический экзофтальм, отечная форма, эндокринная миопатия. Симптомы этих разновидностей имеют некоторые отличия, что можно увидеть из следующей таблицы:
|
Вид эндокринной офтольпатии |
Симптомы |
|
|
Тиреотоксический экзофтальм |
|
|
|
Отечный экзофтальм |
||
|
1 стадия компенсации |
|
|
|
2 стадия: субкомпенсаторная |
|
|
|
3 стадия: декомпенсаторная |
|
|
|
Эндокринная миопатия |
||
|
В большинстве случаев этот вид эндокринной офтальмопатии наблюдается у мужчин на фоне усиленной выработки щитовидной железой йодсодержащих гормонов. Патология сопровождается следующими симптомами:
|
||

Видео
Нашли в тексте ошибку?
Выделите её, нажмите Ctrl + Enter и мы всё исправим!
Эндокринная или офтальмопатия Грейвса – это поражение мышц и ретробульбарных тканей глазного яблока, возникающее при аутоиммунных заболеваниях щитовидной железы. У большинства пациентов патология развивается при , реже причиной является тиреоидит или наблюдается изолированное поражение глазной орбиты.
Недуг приводит к развитию пучеглазия, повышению внутриглазного давления, раздвоенности изображения.
Симптомы эндокринной офтальмопатии чаще всего выявляют у женщин возрастной категории 40–45 и 60–65 лет. Заболевание может диагностироваться и у детей младше 15 лет. Причем молодые люди переносят недуг легко, а пожилые пациенты страдают тяжелыми формами ЭОП.
Основной причиной развития эндокринной офтальмопатии являются аутоиммунные процессы в организме. При этом иммунная система человека начинает воспринимать глазную клетчатку как инородное тело и вырабатывать специфические антитела к рецепторам тиреотропного гормона (АТ к ТТГ). Т-лимфоциты провоцируют образование отека, увеличение объема мышечных волокон, воспалительный процесс, инфильтрацию.

По мере утихания воспаления происходит замещение здоровых тканей соединительной, еще через 1–2 года формируются рубцы, после чего экзофтальм сохраняется пожизненно.
Эндокринная офтальмопатия может диагностироваться при следующих заболеваниях:
- тиреотоксикоз;
- аутоиммунный тиреоидит Хашимото;
- рак щитовидной железы;
- сахарный диабет;
- гипотиреоз.
У 15% больных фиксируется эутиреоидное состояние, при котором функционирование щитовидной железы не нарушено. К провоцирующим факторам развития эндокринной офтальмопатии относится бактериальная, вирусная инфекция, радиационное облечение, курение, стресс.
Поражение тканей орбиты может возникать во время острого течения диффузного зоба или задолго до его начала, у некоторых больных симптомы сохраняются еще несколько лет после проведенного лечения (3–8 лет).
Клинические признаки эндокринной офтальмопатии
При тиреотоксикозе развивается экзофтальм, характеризующийся выпячиванием наружу глазных яблок. Уменьшается объем верхнего века, благодаря чему увеличивается разрез глазной щели, больной не может полностью закрывать глаза. Признаки обычно нарастают в течение 18 месяцев.

Симптомы эндокринной офтальмопатии:
- ощущение песка в глазах;
- светобоязнь;
- слезотечение;
- при офтальмопатии появляется сухость глаз;
- диплопия – двоение изображения при отведении взгляда в сторону;
- головная боль;
- экзофтальм – пучеглазие;
- симптом Кохера – появление видимого участка склеры между верхним веком и радужной оболочкой при взгляде вниз;
- косоглазие;
- офтальмопатия вызывает покраснение конъюнктивы, склер;
- пигментация кожи век;
- редкое моргание;
- невозможность отведения газ в стороны;
- дрожание, загибание век.
Экзофтальм при эндокринной офтальмопатии бывает односторонним или поражает оба глаз. Из-за неполного смыкания век происходит изъязвление роговицы, развивается хронический конъюнктивит, иридоциклит, синдром сухого глаза. При сильном отеке наблюдается сдавливание глазного нерва, приводящее к ухудшению зрения, атрофии нервных волокон. Поражение мышц глазного дна приводит к повышению внутриглазного давления, формируется косоглазие, тромбоз вен сетчатки.
Если при эндокринной офтальмопатии развивается миопатия глазодвигательных мышц, то возникает двоение изображения, патология носит прогрессирующее течение. Такие симптомы встречаются преимущественно у мужчин при гипотиреозе щитовидной железы или эутиреозном состоянии. Позже присоединяется экзофтальм, отечность клетчатки не наблюдается, но увеличивается объем мышц, больной не может двигать глазами вниз и вверх. Участки инфильтрации в короткие сроки замещаются фиброзными тканями.
Симптомы отечного экзофтальма
Отечная эндокринная офтальмопатия характеризуется двухсторонним поражением глаз, патология наблюдается не одновременно, интервал может составлять до нескольких месяцев. Такая форма заболевания имеет 3 стадии течения:
- Компенсация офтальмопатии развивается постепенно. Пациенты отмечают опущение верхнего века в первой половине дня, а к вечеру состояние нормализуется. По мере прогрессирования недуга происходит ретракция века, увеличение глазной щели. Повышается тонус мышц, возникает контрактура.
- Субкомпенсация эндокринной офтальмопатии сопровождается повышением внутриглазного давления, отеком ретробульбарных тканей невоспалительного характера, экзофтальмом, нижнее веко поражается хемозом. Четко проявляются симптомы пучеглазия, веки не смыкаются полностью, мелкие сосуды склер становятся извилистыми и формируют рисунок в виде креста.
- Для стадии декомпенсации эндокринной офтальмопатии характерно усиление клинической картины. Из-за отека клетчатки глаз становится неподвижным, повреждается зрительный нерв. Роговица изъязвляется, развивается кератопатия. Без проведения терапии нервные волокна атрофируются, ухудшается зрение за счет формирования бельма.
Эндокринная офтальмопатия в большинстве случаев не приводит к потере зрения, но значительно его ухудшает из-за осложнения кератитом, компрессионной нейропатией.

Классификация эндокринной офтальмопатии
В зависимости от степени проявления клинических симптомов ЭОП классифицируют по методике Баранова:
- I степень офтальмопатии проявляется незначительным экзофтальмом менее 16 мм, отмечается припухлость век, песок в глазах, сухость слизистых оболочек, слезотечение. Нарушений двигательных функций не происходит.
- II степень эндокринной офтальмопатии – экзофтальм до 18 мм, небольшие изменения склер, глазодвигательных мышц, песок, слезотечение, светобоязнь, диплопия, отечность век.
- III степень эндокринной офтальмопатии – пучеглазие резко выражено до 22 мм, фиксируется неполное смыкание век, язвы роговицы, нарушение подвижности глаз, ухудшение зрения, симптомы стойкой диплопии.
Согласно методике Бровкиной эндокринную офтальмопатию классифицируют на тиреотоксический, отечный экзофтальм и миопатию. Каждая из стадий может переходить в следующую без проведения своевременного лечения.
Международная классификация NOSPECS имеет свои особенности.
0 класс N эндокринной офтальмопатии – отсутствие симптомов.
1 класс О – ретракция верхнего века.
2 класс S эндокринной офтальмопатии – поражение мягких тканей:
- отсутствуют;
- минимальные;
- средней степени тяжести;
- ярко выражены.

3 класс Р эндокринной офтальмопатии – наличие признаков экзофтальма:
- менее 22 мм;
- 22–25 мм;
- 25–27 мм;
- более 27 мм.
4 класс Е эндокринной офтальмопатии – поражение глазодвигательных мышц:
- симптомы отсутствуют;
- незначительное ограничение подвижности глазных яблок;
- выраженное ограничение подвижности;
- постоянная фиксация.
5 класс D эндокринной офтальмопатии – симптомы поражения роговицы:
- отсутствуют;
- умеренные;
- изъязвления;
- перфорации, некрозы.
6 класс S офтальмопатии – поражение зрительного нерва:
- менее 0,65;
- 0,65–0,3;
- 0,3–0,12;

К тяжелым относятся степени, начиная с 3, а 6 класс диагностируют как осложненную форму эндокринной офтальмопатии.
Дифференциальная диагностика
Для оценки состояния щитовидной железы больные сдают анализ крови на уровень тиреоидных гормонов, антитела к рецепторам и ТПО. При эндокринной офтальмопатии концентрация Т3 и Т4 значительно превышает норму.
Ультразвуковое исследование, позволяет определить размеры и степень увеличения органа, выявить узловые образования. Если обнаруживаются крупные узлы, превышающие в диаметре 1 см, выполняют тонкоигольную аспирационную биопсию.
Офтальмологическое обследование включает УЗИ орбиты глазного дна, измерение внутриглазного давления, периметрию, проверку остроты и полей зрения. Оценивается состояние роговицы, степень подвижности яблока. Дополнительно может быть назначена КТ, МРТ орбиты, биопсия мышц.
Аутоиммунная офтальмопатия дифференцируется с миостенией, псевдоэкзофтальмом при близорукости, флегмоной глазницы, злокачественными опухолями орбиты, нейропатиями другой этиологии.
Методы лечения
Лечение офтальмопатии назначается с учетом степени тяжести и причины развития патологии. Применяют консервативный и хирургический метод терапии. Нарушения работы щитовидной железы устраняется под контролем эндокринолога. Пациентам прописывают заместительную гормональную терапию или прием тиреостатиков, подавляющих гиперсекрецию Т3, Т4. При неэффективности медикаментов проводят частичное или полное удаление щитовидной железы.

Для снятия симптомов острого воспаления при эндокринной офтальмопатии назначаются глюкокортикоиды (Преднизолон), стероиды. Циклоспорин показан для подавления иммунных процессов, препарат изменяет функции Т-лимфоцитов, назначается в комплексном лечении эндокринной офтальмопатии.
Пульс-терапия проводится при нейропатиях, тяжелой степени воспаления. Гормоны вводят внутривенно большими дозами за короткое время. Если через 2 суток не будет достигнут желаемый результат, выполняют хирургическое вмешательство.
Для лечения эндокринной офтальмопатии применяется метод ретробульбарного введения глюкокортикоидов. Препараты вводят в верхне-нижний отдел орбиты на глубину 1,5 см. Этот способ помогает увеличить концентрацию лекарства непосредственно в пораженных тканях.
Эндокринная офтальмопатия, сопровождающаяся стойкой диплопией, снижением зрения, воспалительным процессом, лечится с помощью лучевой терапии. Рентгеновское излучение помогает разрушить фибробласты и патологические Т-лимфоциты. Хороший результат достигается при раннем лечении ЭОП с комплексным применением глюкокортикостероидов.
В качество симптоматической терапии эндокринной офтальмопатии назначаются средства, нормализующие метаболизм (Прозерин), глазные антибактериальные капли, гели, витамины А, Е. Проводят физиотерапевтические процедуры: магнитотерапию, электрофорез с алоэ.
Терапия тиреотоксикоза
Консервативное лечение назначается при незначительном увеличении размеров щитовидной железы без симптомов сдавливания пищевода, трахеи и выраженных признаков эндокринной офтальмопатии. Пациентам с узлами щитовидки и экзофтальмом медикаментозную терапию назначают перед хирургическим лечением или применением радиоактивного йода.

Добиться эутиреоидного состояния удается через 3–5 недель после курса тиреостатиков. В 50% случаев ремиссия сохраняет до 2 лет, у остальных пациентов происходят рецидивы. При этом в крови пациентов обнаруживается высокий титр антител к ТТГ.
Тиреостатическую терапию у больных офтальмопатией проводят препаратами группы тионамидов:
- Тимозол;
- Мерказолил.
Дополнительно назначаются β-адреноблокаторы для предотвращения тканевого превращения тироксина в трийодтиронин. Существует 2 вида тиореостатического лечения: монотерапия или комплексное сочетание тиреостатиков с L-тироксином. Эффективность результатов оценивают по уровню Т3, Т4, показатели ТТГ неинформативны.
При эндокринной офтальмопатии проводится путем приема активной молекулы йода, которая способна накапливаться в тканях щитовидной железы и вызывать разрушение ее клеток. В результате уменьшается секреция тиреоидных гормонов с последующим развитием гипотиреоза и назначением заместительной терапии тироксином.
Хирургическое вмешательство показано при больших щитовидной железы, компрессии пищевода, трахеи, аномальном расположении зоба и неэффективности консервативного лечения. Проводят частичное иссечение органа или удаляют щитовидку полностью.

Хирургическое лечение эндокринной офтальмопатии
Показанием к хирургическому вмешательству служит:
- неэффективность консервативной терапии;
- компрессионная оптическая нейропатия;
- подвывих глазного яблока;
- выраженный экзофтальм;
- симптомы тяжелого поражения роговицы.
Декомпрессия орбит при эндокринной офтальмопатии предотвращает гибель глаза, увеличивает объем глазниц. В ходе операции выполняют частичное удаление стенок орбиты и пораженной клетчатки, это позволяет замедлить прогрессирование недуга, снизить внутриглазное давление, уменьшить экзофтальм.
Декомпрессия орбит проводится несколькими способами:
- Трансантральный метод заключается в удалении нижней, медиальной или наружной стенки орбиты. Осложнением операции может быть нарушение чувствительности в периорбитальной области.
- Трансфронтальная декомпрессия выполняется за счет иссечения передней стенки орбиты с доступом через лобную кость. В результате уменьшаются симптомы экзофтальма, снижается давление. При этом методе существует риск развития кровотечения, повреждения структур головного мозга, ликвореи, менингита.
- Внутренняя ДО – это удаление ретробульбарной клетчатки объемом до 6 мм³. Такой способ применяют при нормальном состоянии мягких тканей (офтальмопатия 2 класс Sа), что определяется по результатам КТ, МРТ.
- Трансэндмоидальная эндоскопическая декомпрессия – удаление медиальной стенки орбиты до клиновидной пазухи. В результате операции ретробульбарные ткани смещаются в область решетчатого лабиринта, нормализуется положение глазного яблока, удается добиться регрессии экзофтальма.

Хирургическая коррекция глазодвигательных мышц при косоглазии, диплопии проводится в период стабилизации состояния больного. Чтобы достичь желаемого результата, улучшить бинокулярное зрение у больных офтальмопатией может потребоваться несколько операций. Для устранения косметических дефектов проводят хирургическое удлинение век, делают инъекции Ботулоксина, субконъюнктивального Триамцинолона для уменьшения ретракции и полного закрытия глаза.
Латеральная тарзорафия (ушивание краев век) при эндокринной офтальмопатии помогает провести коррекцию верхнего и нижнего века, но эффективность этой процедуры меньше, чем ДО. Тенотомия мышц Мюллера позволяет добиться опущения века. Заключительным этапом является блефаропластика и дакриопексия слезных точек.
Прогноз
Эффективность лечения эндокринной офтальмопатии зависит от того, как быстро были назначены медикаменты. Правильная терапия недуга на ранних стадиях позволяет предотвратить прогрессирование и развитие осложнений, можно добиться затяжной ремиссии. Ухудшение состояния при этом отмечается лишь у 5% больных.
Людям, страдающим симптомами эндокринной офтальмопатии, рекомендуется отказаться от вредных привычек, носить темные очки, использовать капли глазные капли для защиты роговицы от пересыхания. Пациенты должны находиться на диспансерном учете, регулярно проходить осмотр у эндокринолога и офтальмолога, принимать тиреостатики или препараты заместительной терапии, назначенные врачом. Один раз в 3 месяца следует сдавать кровь на уровень гормонов щитовидной железы.
Эндокринная офтальмопатия характеризуется поражением ретробульбарных тканей глазных орбит с различной степенью интенсивности. Симптомы патологии чаще всего развиваются при тиреотоксикозе щитовидной железы, вызванном гиперсекрецией тиреоидных гормонов на фоне аутоиммунных процессов. Лечение должно проводиться комплексно, включать прием тиреостатиков, глюкокортикоидов, стероидов, иммунодепрессантов. При выраженной оптической нейропатии, экзофтальме выполняется хирургическая декомпрессия глазных орбит.
Эндокринная офтальмопатия (тиреоид-ассоциированная орбитопатия, офтальмопатия Грейвса, сокращенно - ЭОП) – аутоиммунный процесс, часто сочетающийся с аутоиммунными заболеваниями щитовидной железы, поражающий орбитальные и периорбитальные ткани и приводящий к их дистрофическим изменениям. Она может предшествовать, сопутствовать либо являться одним из проявлений системных осложнений нарушения уровня гормонов щитовидной железы. В некоторых случаях ЭОП проявляется совокупно с миастенией гравис, болезнью Аддисона, витилиго, пернициозной анемией, иерсиниозом. Существует явная взаимосвязь риска развития проявлений тиреоид-ассоциированной орбитопатии и их тяжести с курением. Применение радиойодтерапии в лечении заболеваний щитовидной железы может способствовать манифестации и прогрессированию ЭОП.
Причины возникновения
В настоящее время не существует единого мнения относительно патогенеза развития ЭОП. Однако все суждения сходятся в том, что ткани орбиты вызывают патологический иммунный ответ организма, в результате чего проникновение в эти ткани антител приводит к воспалению, отеку, а в дальнейшем, спустя 1-2 года, к рубцеванию. По одной из теорий предполагается, что клетки тканей щитовидной железы и ретроорбитального пространства обладают общими фрагментами антигенов (эпитопами), которые, вследствие различных причин, начинают распознаваться иммунной системой человека, как чужеродные. Как аргумент, выдвигается тот факт, что диффузный токсический зоб и ЭОП в 90% случаев сопутствуют друг другу, выраженность глазных симптомов при достижении эутиреоза снижается, а уровень антител к рецептору тиреотропного гормона при данном сочетании заболеваний высокий. По другой теории, ЭОП представляется как самостоятельное заболевание с преимущественным поражением тканей орбиты. Аргументом в пользу данной теории является то, что при ЭОП приблизительно в 10% случаев не выявляется дисфункция щитовидной железы.
Причина ЭОП, вопреки распространенному мнению, кроется не в щитовидной железе и регуляция ее функции не может обратить развитие этого заболевания вспять. Скорее, аутоиммунный процесс затрагивает данную эндокринную железу вкупе с глазными мышцами и клетчаткой орбиты. Тем не менее, восстановление нормального уровня гормонов щитовидной железы может облегчить течение ЭОП, хотя в некоторых случаях это не помогает остановить ее прогрессирование.
У большого количества пациентов с ЭОП отмечается гипертиреоидное состояние, однако в 20% случаев встречается эутиреоз, а иногда даже выявляются заболевания, сопровождающиеся понижением уровня тиреоидных гормонов - тиреоидит Хашимото, рак щитовидной железы. При наличии гипертиреоза глазные симптомы обычно развиваются в течение 18 месяцев.
Заболеваемость составляет в среднем около 16 и 2,9 случаев на 100000 женщин и мужчин соответственно. Таким образом, женщины гораздо больше предрасположены к этому заболеванию, но при этом более тяжелые случаи отмечаются все же у мужчин. Средний возраст больных составляет 30-50 лет, тяжесть проявлений напрямую коррелирует с возрастом (чаще после 50 лет).
Симптомы эндокринной офтальмопатии
Симптоматика ЭОП зависит от наличия сопутствующих заболеваний щитовидной железы, которые добавляют свои характерные проявления. Глазными же проявлениями эндокринной офтальмопатии являются ретракция (подтянутость кверху) века, чувство сдавливания и боль, сухость глаз, нарушение цветовосприятия, экзофтальм (выступание глазного яблока кпереди), хемоз (отек конъюнктивы), периорбитальный отек, ограничение глазных движений, приводящее к значительным функциональным и косметическим нарушениям. Симптомы могут наблюдаться как с одной стороны, так и с обеих. Их проявление и выраженность зависят от стадии заболевания.
У ЭОП существует множество симптомов, названных по именам авторов, впервые их описавших:
. симптом Гифферда-Энроса (Gifferd - Enroth) - отек век;
. симптом Дальримпля (Dalrymple) - широко раскрытые глазные щели вследствие ретракции век;
. симптом Кохера (Kocher) - появление видимого участка склеры между верхним веком и радужкой при взгляде вниз;
. симптом Штельвага (Stelwag) - редкое мигание;
. симптом Мебиуса-Грефе-Минза (Mebius - Graefe - Means) - отсутствие координации движений глазных яблок;
. синдром Похина (Pochin) - загибание век при их закрытии;
. симптом Роденбаха (Rodenbach) - дрожание век;
. симптом Еллинека (Jellinek) - пигментация век.
Хотя подавляющее большинство случаев ЭОП не приводит к потере зрения, они могут вызывать его ухудшение из-за развития кератопатии, диплопии, компрессионной оптиконейропатии.
Диагностика
При выраженной клинической картине ЭОП для диагностики может быть достаточно офтальмологического осмотра. В него входят исследование оптических сред глаза, визометрия, периметрия, исследование цветового зрения и глазных движений. Для измерения степени экзофтальма применяется экзофтальмометр Гертеля. В неясных случаях, а также для оценки состояния глазодвигательных мышц, тканей ретробульбарной области могут проводиться УЗИ, МРТ и КТ- исследования. При сочетании ЭОП с тиреоидной патологией исследуется гормональный статус (уровень общих Т 3 и Т 4 , связанных Т 3 и Т 4 , ТТГ). Также на наличие ЭОП могут указывать повышенная экскреция гликозамингликанов с мочой, наличие в крови антитиреоглобулиновых и ацетилхолинэстеразных антител, офтальмопатического Ig, экзоофтальмогенного Ig, AT к «64кД» глазному протеину, альфа-галактозил-AT, антител к микросомальной фракции.
Классификация
Существует несколько классификаций ЭОП. Самая простая из них выделяет два типа, которые, впрочем, не взаимоисключают друг друга. К первому относят ЭОП с минимальными признаками воспаления и рестриктивной миопатии, ко второму – со значительными их проявлениями.
За рубежом пользуются классификацией NOSPECS.
|
Изменения |
Степень выраженности |
||
|
N (no signs or symptoms) - нет признаков или симптомов |
|||
|
O (only sings) - признаки ретракции верхнего века |
|||
|
S (soft-tissue involvement) - вовлечение мягких тканей с симптомами и признаками |
Отсутствуют |
||
|
Минимальные |
|||
|
Средней степени выраженности |
|||
|
Выраженные |
|||
|
P (proptosis) - наличие экзофтальма |
|||
|
E (extraocular muscle involvement) - вовлечение глазодвигательных мышц |
Отсутствует |
||
|
Ограничение подвижности глазных яблок незначительное |
|||
|
Явное ограничение подвижности глазных яблок |
|||
|
Фиксация глазных яблок |
|||
|
C (сorneal involvement) - вовлечение роговицы |
Отсутствует |
||
|
Умеренное повреждение |
|||
|
Изъязвления |
|||
|
Помутнения, некрозы, перфорации |
|||
|
S (sight loss) - вовлечение зрительного нерва (снижение зрения) |
|||
К тяжелым формам по этой классификации относят: класс 2, степень с; класс 3, степень b или с; класс 4, степень b или с; класс 5, все степени; класс 6, степень а. Класс 6, степени b и с рассматриваются как очень тяжелые.
В России более широко пользуются классификацией Баранова.
|
Проявления |
|
|
Небольшой экзофтальм (15,9 ± 0,2 мм), припухлость век, периодически возникающее непостоянное ощущение "песка" в глазах, иногда слезотечение. Нарушения со стороны функции глазодвигательных мышц отсутствуют. |
|
|
(средней тяжести) |
Умеренный экзофтальм (17,9 ± 0,2 мм) с нерезкими изменениями со стороны конъюнктивы и легким либо умеренным нарушением функции экстраокулярных мышц, ощущение засоренности в глазах ("песка"), слезотечение, светобоязнь, нестойкая диплопия. |
|
(тяжелый) |
Резко выраженный экзофтальм (22,2 ±1,1 мм), как правило, с нарушением смыкания век и изъязвлением роговицы, стойкая диплопия, резко выраженные нарушения функции глазодвигательных мышц, признаки атрофии зрительных нервов. |
Также существует классификация Бровкиной, выделяющая три формы ЭОП: тиреотоксический экзофтальм, отечный экзофтальм и эндокринную миопатию. Каждая из этих форм может переходить в последующую.
Лечение эндокринной офтальмопатии
Лечение ЭОП зависит от стадии процесса и наличия сопутствующей патологии щитовидной железы, однако есть общие рекомендации, которых следует придерживаться независимо от этого:
1) прекращение курения;
2) использование увлажняющих капель, глазных гелей;
3) поддержание стойкого эутиреоза (нормальной функции щитовидной железы).
При наличии нарушения функции щитовидной железы проводится ее коррекция под контролем эндокринолога. При гипотиреозе применяется заместительная терапия тироксином, а при гипертиреозе – лечение тиреостатическими препаратами. При неэффективности консервативного лечения возможно хирургическое удаление части или всей щитовидной железы.
Консервативное лечение
Для устранения симптомов воспаления, отека наиболее часто системно применяют глюкокортикоиды, или стероиды. Они позволяют снизить продукцию клетками-фибробластами мукополисахаридов, играющих важную роль в иммунных реакциях. Существует много различных схем применения глюкокортикоидов (преднизолон, метилпреднизолон), рассчитанных на период от нескольких недель до нескольких месяцев. Альтернативой стероидам может быть циклоспорин, который также может применяться в комбинации с ними. При тяжелом воспалении или компрессионной оптиконейропатии может проводиться пульс-терапия (введение сверхвысоких доз в короткое время). Оценка ее эффективности производится спустя 48 часов. В случае отсутствия эффекта целесообразно выполнение хирургической декомпрессии.
В постсоветских странах до сих пор широко используется ретробульбарное введение глюкокортикоидов. Однако за рубежом в последнее время отказались от такого метода лечения пациентов с данной патологией по причине его травматичности, образования рубцовой ткани в области введения препарата. Кроме того, эффект глюкокортикоидов связан больше с их системным действием, нежели с местным. Обе точки зрения являются предметом дискуссий, поэтому использование данного метода введения остается на усмотрение врача.
Для лечения умеренного и тяжелого воспаления, диплопии, снижения зрения может применяться лучевая терапия. Ее действие связывается с оказанием повреждающего эффекта на фибробласты и лимфоциты. Ожидаемый результат проявляется через несколько недель. По причине того, что рентгеновское излучение временно может усиливать воспаление, пациентам назначаются стероидные препараты в течение первых недель облучения. Наилучший эффект лучевой терапии достигается в стадии активного воспаления, лечение которого было начато в срок до 7 месяцев от начала ЭОП, а также в комбинации с глюкокортикоидами. К возможным рискам его относят развитие катаракты, лучевой ретинопатии, лучевой оптиконейропатии. Так, в одном из исследований образование катаракты было зафиксировано у 12% пациентов. Также не рекомендовано применение лучевой терапии у больных с сахарным диабетом из-за возможного прогрессирования ретинопатии.
Хирургическое лечение
Около 5% пациентов с ЭОП нуждаются в хирургическом лечении. Часто оно может потребовать нескольких этапов. При отсутствии таких серьезных осложнений ЭОП, как компрессионная оптиконейропатия или тяжелое поражение роговицы, вмешательство должно быть отложено до затихания активного воспалительного процесса или проводиться в стадии рубцовых изменений. Также важен порядок выполнения этапов вмешательств.
Декомпрессия орбиты может проводиться как в качестве первичного этапа лечения компрессионной оптиконейропатии, так и при неэффективности консервативной терапии. Потенциальными осложнениями его могут быть слепота, кровотечение, диплопия, потеря чувствительности в периорбитальной зоне, смещение век и глазного яблока, синусит.
Хирургия косоглазия обычно выполняется в неактивном периоде ЭОП, когда угол отклонения глаза стабилен в течение не менее 6 месяцев. Лечение в первую очередь проводится с целью минимизации диплопии. Достичь постоянного бинокулярного зрения часто бывает затруднительно, а одного вмешательства может быть недостаточно.
С целью уменьшить легкий и умеренно выраженный экзофтальм могут проводиться хирургические вмешательства, направленные на удлинение век. Они являются альтернативой введению ботулин-токсина в толщу верхнего века и триамцинолона субконъюнктивально. Возможно также выполнение боковой тарзоррафии (сшивание латеральных краев век), позволяющей уменьшить ретракцию века.
Финальным этапом хирургического лечения ЭОП являются блефаропластика и пластика слезных точек.
Перспективы в лечении эндокринной офтальмопатии
В настоящее время разрабатываются новые методы и препараты для лечения ЭОП. Эффективность приема микроэлемента - селена (антиоксидант), противоопухолевого средства - ритуксимаба (антитела к CD20 антигену), ингибиторов фактора некроза опухолей – этанерцепта, инфликсимаба, даклизумаба, находится на стадии клинических исследований.
Существуют методы лечения ЭОП, которые не являются основными, но могут с успехом применяться в некоторых ситуациях. К таким, например, относят введение пентоксифиллина и никотинамида, которые блокируют образование мукополисахаридов фибробластами в ретроорбитальной области.
Одним из возможных медиаторов патологического процесса в орбитах является инсулиноподобный фактор роста 1. В связи с этим для лечения ЭОП применяется аналог соматостатина – октреотид, рецепторы к которому имеются в ретробульбарных тканях. В последнее время начато использование длительно действующего аналога соматостатина – ланреотида.
Роль плазмофереза и внутривенного введения иммуноглобулина в лечении ЭОП в настоящее время не достаточно изучена. Применение последнего в сравнении с пероральным применением преднизолона в одном из исследований показало аналогичный эффект, но при меньшем количестве побочных эффектов.
Эндокринная офтальмопатия - это заболевание, при котором происходит поражение мягких тканей глаза, что развивается по причине патологии щитовидной железы. Выражается эндокринная офтальмопатия в основном экзофтальмом и отечностью с воспалением тканей глаза. Для диагностики эндокринной офтальмопатии назначается проведение таких обследований, как экзофтальмометрия, биомикроскопия и КТ орбиты. Также проводятся тесты на состояние иммунной системы.
Причины эндокринной офтальмопатии
Эндокринная офтальмопатия может появиться при первых возникающих аутоимунных процессах в щитовидной железе.
Что же провоцирует появление офтальмопатии так до конца и не выяснено. Но в основном пуском для развития являются такие факторы, как респираторные инфекции и курение, радиация в малых дозах и соли тяжелых металлов, также стресс и аутоиммунные заболевания типа сахарного диабета. Облегченные формы эндокринной офтальмопатии встречаются чаще всего у молодых людей, ну а тяжелая форма характерна для людей пожилого возраста.
Выясняется, что при мутации Т-лимфоциты начинают взаимодействовать с рецепторами мембран клеток глазных мышц, провоцируют в них образование специфических изменений. Аутоиммунная реакция Т-лимфоцитов провоцирует высвобождение цитокинов, они в свою очередь индуцируют пролиферацию фибробластов, выработку коллагена и гликозаминогликанов. Выработка гликозаминогликанов образует отеки при связывании воды и способствует увеличению объема ратробульбарной клетчатки. Такой отек тканей орбиты в течение времени заменяется фиброзированием, что в итоге приводит к необратимому процессу экзофтальма.
Классификация эндокринной офтальмопатии
При развитии эндокринной офтальмопатии наблюдается несколько фаз воспалительной экссудации, инфильтрации и фазы пролиферации и фиброза.
Также выделяют три стадии эндокринной офтальмопатии: тиреотоксический экзофтальм, отечный экзофтальм и эндокринная миопатия. Рассмотрим подробнее их.
Тиреотоксический экзофтальм
Тиреотоксический экзофтальм характеризуется истинной или ложной протрузией глазного яблока, также происходит отставание века при опущении глаза и излишний блеск.
Отечный экзофтальм
Отечный экзофтальм проявляется при выраженном выстоянии глазного яблока на два-три сантиметра и двустороннем отеке периорбитальных тканей. Также происходит резкое ухудшение подвижности глазных яблок. В будущем происходит прогрессирование эндокринной офтальмопатии с полной офтальмоплегией и несмыканием глазных щелей, язвами роговицы - процессом, проходящим в роговой оболочке глаза вместе с которым проявляется образование кратерообразного язвенного дефекта. Протекает такое заболевание со снижением зрения и помутнением роговой оболочки.
Эндокринная форма
Эндокринная форма миопатии поражает чаще всего прямые глазодвигательные мышцы и в итоге приводит к диплопии, это так называемое отсутствие движения глаз, косоглазие.
Для определения выраженности офтальмопатии применяют таблицу степени Баранова, итак для определения первой степени потребуются такие критерии:
- маловыраженный экзофтальм;
- небольшая отечность века;
- интактность коньюктивных тканей;
- не нарушена мышечная подвижность глаз.
Для второй степени существует следующая характеристика:
- умеренная выраженность экзофтальма;
- отек века значительно увеличен, по сравнению с первой степенью;
- наличие отечности коньюнктивы.
Третья степень эндокринной офтальмопатии отличается от двух предыдущих степеней ярко выраженной диплопией и язвами роговицы, также происходит атрофия зрительного нерва, при этом наблюдается полная деструкция нервных волокон, которые передают зрительное раздражение из сетчатки в головной мозг. Такая атрофия глазного нерва провоцирует полную потерю зрения.
Симптомы офтальмопатии
Ранние клинические проявления офтальмопатии характеризуются опущением давления в глазу, сухостью либо наоборот слезотечением, наличием неприятных ощущений от яркого света, также отечностью периорбитальной области глаза. В будущем развивается экзофтальм, наличие которого сначала имеет асимметричное или одностороннее развитие.
На период уже отчетливо заметных проявлений клинических симптомов эндокринной офтальмопатии, начинают появляться признаки увеличения глазных яблок, опухлость век, а также ярко выраженные головные боли. Также при неполном смыкании века обеспечено появление язв роговицы и коньюктивита.
Ярко выраженный экзофтальм приводит к возникновению компрессии зрительного нерва и дальнейшей его атрофии. Также экзофтальм при наличии эндокринной офтальмопатии требует более тщательного уточнения и сравнения отличий его от псевдоэкзофтальма, такое часто происходит при повышенной степени близорукости или разных опухолях типа саркомы орбиты или менингиома.
При невозможной подвижности глазных яблок наступает давление внутри глаза и развитие псевдоглаукомы.
Диагностика эндокринной офтальмопатии
В диагностировании особое, но не единственное и главное, значение имеет сопутствующий диффузный токсический зоб. При наличии характерного двухстороннего процесса у пациента практически сразу определяется диагноз. Достаточно редко приходится использовать ультразвуковое исследование для определения толщины глазодвигательных мышц.
По ряду случаев такое исследование проводится для активной диагностики клинически невыраженной эндокринной офтальмопатии, ее определение позволяет выявить токсический зоб в тех случаях, когда существует сложность отличия от других заболеваний, развивающихся с тиреотоксикозом. Такую же функцию несет проведение исследования методом МРТ, оно является наиболее информативным анализом в данном случае. Основная причина для назначения данного исследования - показание у больного одностороннего экзофтальма, для исключения ретробульбарной опухоли.
При диагностировании диабетической офтальмопатии важно перед назначением лечения установить активность эндокринной офтальмопатии с помощью клинической картины. Для этого существует шкала клинической активности от одного до семи баллов:
- Спонтанная ретробульбарная боль;
- Болевые ощущения при осуществлении движений глазом;
- Покраснение век;
- Отечность;
- Инъекции конъюктива;
- Хемоз;
- Отек карункулы.
Эндокринная офтальмопатия по такой шкале считается активной от четырех баллов.
Лечение эндокринной офтальмопатии
Лечение проводится совместно с врачом-офтальмологом и эндокринологом при учете тяжелых стадий заболевания и дефектов в работе функции щитовидной железы. Успешное лечение проверяется достижением стойкого эутиреоидного состояния.
Неблагоприятно влияет на течение эндокринной офтальмопатии гипотиреоз и тиреотоксикоз, также ухудшение состояния фиксируется при достаточно быстром переходе от одного к другому состоянию, поэтому после применения оперативного лечения, стоит четко контролировать уровень тиреоидных гормонов в крови, следует проводить профилактические мери по отношению к гипотиреозу.
Особенности лечения эндокринной офтальмопатии
Достаточно часто клиническая картина эндокринной офтальмопатии наблюдается у пациентов без клинических нарушений работы щитовидной железы. У таких больных при обследовании возможно выявление субклинического тиреотоксикоза или субклинического гипотиреоза, также возможно отсутствие патологических изменений. При отсутствии каких-либо патологических изменений назначается взятие пробы с тиролиберином. Далее больной наблюдается у врача-эндокринолога, у которого и проводится динамический контроль тиреоидного статуса.
При определении лечения, следует также понимать, что заболевание имеет свойство самопроизвольной ремиссии. Лечение также назначается с учетом тяжести и активности заболевания.
Какое лечение предусмотрено для разных стадий заболевания
При любой тяжести заболевания, необходимо прекратить курение и защищать роговицы с помощью капель, стоит носить затемненные очки.
- При облегченной форме офтальмопатии проводится только контроль процесса без вмешательства.
- При умеренной тяжести офтальмопатии и активной фазе стоит применить противовоспалительную терапию. Умеренная тяжесть офтальмопатии и неактивная фаза провоцирует применение реконструктивной хирургии.
- При тяжелой эндокринной офтальмопатии применяется пульс-терапия глюкокортикоидами, декомпрессия орбит.
Активная терапия в большинстве своих случаев не применяется при эндокринной офтальмопатии, так как заболевание имеет достаточно легкую форму и склонно к природной ремиссии вне зависимости от действий. Но все же пациенту стоит придерживаться некоторых правил, например, прекратить курение и использование глазных каплей.
Что потребуется для лечения
Основным условием ремиссии является поддержание эутиреоза. При умеренной и тяжелой стадии эндокринной офтальмопатии достаточно часто применяется пульс-терапия метилпреднизолоном, которая является самым эффективным и наиболее безопасным методом. Противопоказаниями к применению пульс-терапии может послужить язвенная болезнь желудка или двенадцатиперстной кишки, панкреатит или артериальная гипертензия.
Также применяется пероральный прием преднизолона, но такой способ имеет большой риск возникновения побочных эффектов. Достаточно частая проблема при применении лечения глюкокортикоидами - часто развивающиеся рецидивы эндокринной офтальмопатии после прекращения приема препаратов.
Лучевая терапия
Лучевая терапия назначается людям с диагнозом эндокринная офтальмопатия как при умеренных, так и тяжелых стадиях воспалительной симптоматики, диплопии и полной потере зрения. Радиация имеет свойство разрушения орбитальных фибробластов и лимфоцитов. Для наступления нужной реакции после применения радиации, потребуется пару недель. В этот период воспалительный процесс набирает оборотов. В течение первых пары недель лечения состояние большей части людей с таким заболеванием стимулируется с помощью стероидов. Наилучшая реакция на лучевую терапию возникает у пациентов на пике воспалительного процесса. Применение радиации может давать лучший эффект в сочетании со стероидной терапией.
Если учитывать тот факт, что применение лучевой терапии может влиять на улучшение положения при сбоях работы моторики, для лечения диплопии применение облучения, как одного вида лечения, не назначается. Орбитальная иррадиация при эндокринной офтальмопатии становится самым безопасным методом лечения. Облучение не назначается людям с сахарным диабетом из-за возможности ухудшения ретинопатии.
Рентгенотерапия
Также на ряду с применением различных препаратов стоит метод рентгенотерапии на область орбит с синхронным применением глюкокортикоидов. Рентгенотерапия применяется при ярко выделенном отечном экзофтальме, при неэффективном лечении одними глюкокортикоидами, проводится дистанционное облучение орбит с прямых и боковых полей с защитой переднего поля глаза.
Рентгенотерапия имеет противовоспалительное и антипролиферативное действия, провоцирует снижение цитокинов и секреторной активности фибробластов. Эффективность рентгенотерапии оценивается по истечении двух месяцев после проведения лечения. Тяжелая форма эндокринной офтальмопатии предполагает применение оперативного лечения по декомпресии орбит. Хирургическое лечение применяется на стадии фиброза.
Также существует три вида хирургического лечения, это:
- операции на веках при поражении роговицы;
- корректирующее оперирование на двигательных мышцах глаз, проводятся при наличии косоглазия;
- хирургическая декомпрессия орбит, которая применяется для устранения сдавливания зрительного нерва.
В случае малой ретракции века при восстановлении эутиреоидного состояния, применяется оперативное лечение по удлинению века. Такое вмешательство уменьшает экспозицию роговицы и проводится для скрытия проптоз от легкой стадии до умеренной формы. Для пациентов, которые не имеют возможности в операбельности века, вместо удлинения хирургическим путем верхнего века, применяют инъекции ботулотоксина и субконъюнктивального триамцинолона в верхнее веко.
Латеральная тарзорафия уменьшает верхнюю и нижнюю ретракцию века, такая операция менее желательна, так как косметические результаты и их стабильность хуже.
Опущение верхнего века случается за счёт дозированной тенотомии леватора.
Такое лечение применяется также при неактивной фазе эндокринной офтальмопатии при ярко выраженных зрительных и косметических нарушениях. Наиболее эффективной терапией считается лучевая с применением глюкокортикоидов.
Прогноз при эндокринной офтальмопатии
Лишь у двух процентов пациентов встречается тяжелая форма течения эндокринной офтальмопатии, что приводит к тяжелым глазным осложнениям. На сегодняшнем этапе медицина находится на таком уровне, при котором лечение помогает добиться стойкой ремиссии и обойтись без тяжелых последствий болезни.
(см.: эндокринная офтальмопатия, инфильтративная эндокринная офтальмопатия, отечный экзофтальм, нейродистрофический экзофтальм, офтальмопатия Грейвса и т. д.) - органоспецифическое аутоиммунное заболевание, сопровождающееся вовлечением в патогенетический процесс всех образований орбиты и проявляющееся различной степенью экзофтальма и офтальмоплегии.
Аутоиммунная офтальмопатия (АИО) возникает в любом возрасте, но особенно часто после 35 лет. Соотношение лиц мужского и женского пола с этой патологией 2-5:1. Офтальмопатия может сочетаться с другой аутоиммунной патологией, как эндокринной, так и неэндокринной. АИО встречается в 15-18 % случаев диффузного токсического зоба, 3-26 % случаев аутоиммунного тиреоидита.
Этиология и патогенез. Факторы, инициирующие аутоиммунный процесс при АИО, остаются до сих пор не выясненными. Обсуждается "пусковая" роль респираторных инфекций, малых доз радиации, солей тяжелых металлов и т. д. у лиц с генетическими особенностями иммунного ответа. АИО достоверно часто ассоциируется с определенными антигенами системы HLA: HLA В8, HLA DR3, HLA DR5.
При развитии аутоиммунной реакции и Т-лимфоцит, и клетка-мишень экспрессируют антигены гистосовместимости II класса или Ia-белки (на β-лимфоцитах Ia-белки присутствуют постоянно). В норме же Ia-белки на органах и тканях не экспрессируются. Предполагают, что избыточная экспрессия Ia-белков на органах и тканях делает их объектом аутоиммунной атаки. Комплекс аутоантигена с Ia-белками дает сигнал Т-лимфоцитам-хелперам, которые, взаимодействуя с Т- и β-клетками-эффекторами, вызывают активацию последних и продукцию аутоантител (β-лимфоциты) либо непосредственную атаку органа-мишени Т-лимфоцитами-киллерами (эффекторами). Целый ряд регуляторных звеньев контролирует этот процесс. Т-супрессоры подавляют развитие этой реакции в норме, однако при АИО наблюдается недостаточность функции супрессии: снижение функциональной активности клеток-супрессоров либо их количества. Обсуждаются и другие варианты поломок. Проявлением аутоиммунного процесса при АИО является воспалительная реакция в глазодвигательных мышцах, ретробульбарной клетчатке, конъюнктиве, которая сопровождается выделением в области очага поражения большого количества медиаторов и модуляторов воспаления (простагландины, гепарин, гистамин, серотонин, ферменты и т. д.).
В соединительной ткани орбиты увеличивается количество тучных клеток, вырабатывающих мукополисахариды, содержащие гиалуроновую и хондроитинсерную кислоты, которые обладают большой гидрофильностью. Нарастает отек и увеличивается объем ретробульбарной клетчатки. Отмечаются блок венозной орбитальной циркуляции, явления миозита и разрастание соединительной ткани экстраокулярных мышц, пролиферация соединительной ткани орбиты и инфильтрация ее лимфоцитами, плазматическими клетками. На ранних стадиях офтальмопатии в орбите происходит накопление жира, а по мере прогрессирования процесса - уменьшение его количества. Основной причиной выстояния (протрузии) глазного яблока является увеличение ретробульбарной клетчатки и объема глазодвигательных мышц. Со временем инфильтрация и отек ретробульбарной клетчатки и экстраокулярных мышц переходят в фиброз, вследствие чего экзофтальм становится необратимым. Таким образом, фаза воспалительной экссудации при АИО сменяется фазой инфильтрации, а далее пролиферации и фиброза.
Клиническая картина. Ранние признаки: одним из ранних клинических проявлений АИО являются периодически появляющееся ощущение "песка в глазах", светобоязнь, слезотечение. При этом явного увеличения выстояния глазных яблок может и не быть. У большинства больных наблюдается гиперпигментация век различной степени выраженности (синдром Еллинека), блеск глаз (синдром Крауса). Позднее присоединяется экзофтальм, вначале чаще асимметричный либо односторонний.
Стадия развернутой клинической симптоматики. При АИО больные предъявляют жалобы на слезотечение, светобоязнь, чувство засоренности в глазах ("песка"), боли в глазных яблоках, ощущение распирания, увеличение выстояния глазных яблок, инъецированность конъюнктивы, диплопию, головные боли, припухлость век.
Клиническая симптоматика АИО включает в себя изменения со стороны конъюнктивы, роговицы, век, экзофтальм, поражение глазных мышц, осложнения со стороны зрительного нерва.
- Изменения конъюнктивы, роговицы
[показать]
Может наблюдаться инъецированность конъюнктивы, слезотечение. У больных с выраженным экзофтальмом и отсутствием смыкания век - изъязвление роговицы, развитие иридоциклита.
- Изменения век
[показать]
Обнаруживаются при внешнем осмотре. Из многочисленных симптомов отек и ретракция век имеют практическое значение.
Отек век. В активной фазе заболевания обращает на себя внимание периорбитальная отечность, в ряде случаев с пигментацией периорбитальных тканей (синдром Еллинека - коричневые веки), либо краснота, синюшность век. Отечность обычно локализуется в области верхнего века, но может также захватывать и нижнее. Ее выраженность обычно варьирует в течение суток (меньше - в дневное время). Истинный отек следует дифференцировать от псевдоотека, который также может наблюдаться при АИО, но обусловлен пролапсом орбитального жира из-за слабости орбитальной перегородки либо развивается вследствие воспалительной инфильтрации слезной железы. Псевдоотечность обычно остается стабильной и не меняется в течение дня.
Феномен ретракции. Ретракция верхнего века, известная как симптом Дальримпля, обусловлена утолщением мышцы-леватора или симптоматической гипериннервацией. Истинную ретракцию следует отличать от псевдоретракции, которая наблюдается при гипотрофии одного или обоих глаз либо вследствие ограничения поднятия верхнего века и повышенной его иннервации. Обычно эти изменения исчезают при взгляде вниз, в то время как истинная ретракция остается. При АИО могут встречаться оба эти варианта, хотя они и должны быть четко отдифференцированы, что связано с различными подходами в лечении. При истинной ретракции верхнее веко должно быть опущено удлинением, а при псевдоретракции производят корригирующую операцию на глазных мышцах - рецессию (удаление) одной или обеих нижних прямых мышц.
При АИО возможна и ретракция нижнего века, которая возникает вследствие сокращения и укорочения ретракторов нижнего века.
Истинная и псевдоретракция при АИО могут имитировать экзофтальм.
- Экзофтальм
[показать]
Экзофтальм, обусловленный АИО,- наиболее частая причина протрузии одного либо обоих глазных яблок, особенно в регионах, где эта патология эндемична (К. Boorgen, 1991).
Истинный экзофтальм следует отличать от псевдоэкзофтальма, наблюдаемого у лиц с высокой степенью миопии либо при конституциональной особенности - наличии широкой глазной щели.
Истинный экзофтальм, в свою очередь, делится на экзофтальм воспалительного генеза, который и наблюдается у больных с АИО, при орбитальных целлюлитах, а также опухолевого происхождения. Последний в 70 % случаев обусловлен первичными гемангиомами и саркомами орбиты, в 25 % возникает в результате прогрессирующего роста в направлении глазницы карцином, менингиом, в 5 % является метастатическим (карциномы бронхов, груди).
Для количественной оценки выстояния глазного дна и последующего контроля за выраженностью экзофтальма используют экзофтальмометр Гертеля. При увеличении протрузии глазных яблок в сочетании с ретракцией верхнего века нарушается смыкание век, присоединяются симптомы конъюнктивита с вовлечением радужки, ее изъязвлением. Вследствие воспалительной инфильтрации слезной железы усугубляется так называемым синдромом "сухих глаз".
Выраженный экзофтальм может осложняться и компрессией зрительного нерва с соответствующей симптоматикой.
- Изменения глазных мышц
[показать]
Первичные изменения глазных мышц при АИО характеризуются воспалительной инфильтрацией, затем фиброзной и липоматозной трансформацией. Указанные изменения и приводят к характерной глазной симптоматике, которая диагностируется офтальмологом. В процесс могут вовлекаться все глазные мышцы либо преимущественно одна из них.
Изменения со стороны глазных мышц хорошо диагностируются при сонографии орбит и обычно четко дифференцируются от другой патологии (псевдотуморозных образований, артериовенозной фистулы, опухолей). Стенографический контроль в динамике за состоянием глазных мышц часто дает больше информации, чем другие методы (тонометрия и т. д.).
Увеличение глазного давления вследствие механического ограничения движения глазных яблок может приводить к так называемой псевдоглаукоме (Wulle е.а., 1987).
Из-за асимметричного ограничения движения глазных яблок возникает диплопия. В ряде случаев ее исчезновение вовсе не свидетельствует об улучшении процесса, так как развивается симметричное ограничение движения глазных яблок и диплопия уходит. Уточнить истинное состояние помогает проведение диагностических процедур - измерение угла косоглазия при взгляде в различных направлениях, теста с перекрестным закрыванием и открыванием глаз, теста Гиршберга (световой рефлекс на роговице) и т. д.
- Осложнения со стороны зрительного нерва
[показать]
При прогрессировании АИО развиваются осложнения со стороны зрительных нервов (с компрессией либо, что более часто, без компрессии).
Выявление снижения остроты зрения имеет ограниченное значение, так как может быть обусловлено другими проявлениями АИО (повреждения роговицы, астигматизм, extrafoveal fixation). Тем не менее измерения остроты зрения и полей зрения являются обязательными при осмотре больных с АИО. Офтальмоскопия глазного дна и сонография позволяют выявить признаки компрессии зрительного нерва (отек соска зрительного нерва, гиперемия, отечная перипапиллярная сетчатка).
При АИО наблюдается следующая симптоматика, которая имеет название авторов, впервые ее описавших: отек век - синдром Гифферда, Энроса (Gifferd, Enroth); широко раскрытые глазные щели вследствие ретракции век - синдром Дальримпля (Dalrymple); появление участка склеры между верхним веком и радужкой при взгляде вниз - синдром Кохера (Kocher); редкое мигание - синдром Штелльвага (Stellwag); отсутствие координации движений глазных яблок - синдром Мёбиуса, Грефе, Минза (Mebius, Graefe, Means); загиб век при их закрытии - синдром Похина (Pochin); дрожание век - синдром Роденбаха (Rodenbach); пигментация век - синдром Еллинека (Iellinek).
В нашей стране для оценки тяжести АИО пользуются классификацией В. Г. Баранова, при которой выделяют три степени тяжести офтальмопатии.
При АИО I степени наблюдают небольшой экзофтальм (15,9±0,2 мм), припухлость век, периодически возникающее непостоянное ощущение "песка в глазах", иногда слезотечение. Нарушения со стороны функции глазодвигательных мышц отсутствуют. При II степени АИО (средней тяжести) диагностируют умеренный экзофтальм (17,9±0,2 мм) с нерезкими изменениями со стороны конъюнктивы и легким либо умеренным нарушением функции экстраокулярных мышц. Больных II степени АИО беспокоит ощущение засоренности в глазах ("песка"), слезотечение, светобоязнь, нестойкая диплопия.
Для III степени АИО, или тяжелой формы АИО, характерны следующие изменения: резко выраженный экзофтальм (22,2±1,1 мм), как правило, с нарушением смыкания век и изъязвлением роговицы, стойкая диплопия, резко выраженные нарушения функции глазодвигательных мышц, признаки атрофии зрительных нервов.
| Табл. 7. NOSPECS-классификация аутоиммунной офтальмопатии (цитируется по М. P. Mourits, 1990) | ||
| Класс | Степень | Изменения |
| 0 | Нет признаков или симптомов | |
| 1 | Только признаки (ощущение инородного тела, слезотечение, фотофобия) | |
| 2 | Вовлечение мягких тканей с симптомами и признаками | |
| о | отсутствуют | |
| а | минимальные | |
| b | средней выраженности | |
| с | выраженные | |
| 3 | Проптоз (Proptosis) | |
| о | < 23 мм | |
| а | 23-24 мм | |
| b | 25-27 мм | |
| с | > 28 мм | |
| 4 | Вовлечение глазодвигательных мышц | |
| о | отсутствует | |
| а | ограничение подвижности глазных яблок незначительное | |
| b | явное ограничение подвижности глазных яблок | |
| с | фиксация глазных яблок | |
| 5 | Вовлечение роговицы | |
| o | отсутствует | |
| а | умеренное повреждение | |
| b | изъязвление | |
| с | помутнения, некрозы, изъязвления | |
| 6 | Вовлечение зрительного нерва (visual activity) | |
| о | >0,67 | |
| а | 0,67-0,33 | |
| b | 0,32-0,10 | |
| с | < 0,10 | |
В 1977 г. Американская тиреоидная ассоциация утвердила классификацию аутоиммунной офтальмопатии, предложенную G. Werner, в которой выделены 6 классов, отражающих возможные клинические проявления данного заболевания. В последние годы пользуются модифицированной классификацией G. Werner (NOSPECS) с отражением степени выраженности тех или иных проявлений АИО (о - когда данный признак отсутствует, а - минимальные проявления, b - средние, с - выраженные).
По классификации NOSPECS, тяжелые формы АИО: класс 2, степень с; класс 3 b или с; класс 4 b или с; класс 5 (все степени), класс 6а (степени b и с рассматриваются как очень тяжелые) (табл. 7).
Диагноз и дифференциальный диагноз. При диагностике аутоиммунной офтальмопатии обращают внимание на то, является ли АИО самостоятельным заболеванием или ассоциирована с другой аутоиммунной эндокринной или неэндокринной патологией, поскольку от этого зависит объем диагностических и лечебных мероприятий.
Офтальмологический осмотр является обязательным элементом обследования больных с АИО. При этом оценивают общий внешний вид глазных яблок и периорбитальных тканей, состояние оптических сред и поля зрения, степень координации и конвергенции зрительных осей. Проводят экзоофтальмометрию экзоофтальмометром Гертеля (в норме расстояние от наружного края орбиты до выступающей части глазного яблока равно 14±0,5 мм). При необходимости выполняют биомикроскопическое исследование (с помощью щелевой лампы).
Степень АИО оценивают по классификации В. Г. Баранова (1971) либо NOSPECS (G. Werner). Оценить состояние глазодвигательных мышц, ретробульбарной области помогает выполнение сонографии орбиты, КТ орбит (с толщиной томографического среза и шагом степа, равными 2 мм).
Характерными КТ-признаками АИО является изменение размеров, формы и плотности глазодвигательных мышц, объема и структуры ретробульбарной клетчатки. Общее увеличение объема ретробульбарных тканей приводит к смещению глазного яблока кпереди и формированию экзофтальма. Изменения глазодвигательных мышц нередко бывают асимметричными в правой и левой орбитах. Наиболее часто поражаются наружные и внутренние прямые мышцы. Увеличение мышцы обычно начинается с середины, при прогрессировании процесса и нарастании тяжести АИО глазодвигательная мышца поражается на всем протяжении. На начальных стадиях АИО плотность глазодвигательных мышц может быть даже ниже нормальной, при большей длительности заболевания - повышается, появляются отчетливые очаги уплотнений.
Проведение КТ орбиты у больных с АИО позволяет выделить начальные стадии заболевания, когда есть КТ-признаки АИО, но нет экзофтальма, определить прогрессирование или стабилизацию процесса. По данным КТ можно выделить варианты (либо стадии) АИО, когда в патологический процесс вовлечена только ретробульбарная клетчатка либо только глазодвигательные мышцы или имеет место сочетание этих поражений.
Исследование состояния иммунной системы у больных с АИО позволяет в ряде случаев зарегистрировать разнообразные отклонения со стороны как клеточного, так и гуморального звена иммунитета: снижение абсолютного и относительного числа Т-лимфоцитов, изменение соотношения Т- и β-лимфоцитов, уменьшение числа Т-супрессоров, возрастание уровня IgG; повышение титра антител к тиреоглобулину, микросомальной фракции, ко 2-му коллоидному АГ, антител к глазным мышцам, антиядерных АТ.
При сочетании АИО с тиреоидной патологией контролируют показатели тиреоидного статуса - уровень общего Т3 и Т4 св. Т3 и св. Т4, ТТГ (базального и стимулированного < 22 МЕД/л).
Потенциальными "биологическими маркерами" АИО, по данным D. Glinovor (1991), являются антитиреоглобулиновые антитела, ацетилхолинэстеразные антитела, офтальмопатический Ig, экзоофтальмогенный Ig, АТ к "64КД" глазному протеину, альфа-галактозил-АТ, АМ-Аb (антитела к микросомальной фракции), повышенная экскреция гликозамингликанов с мочой.
Дифференциальная диагностика экзофтальма при АИО проводится с псевдоэкзофтальмом при высокой степени миопии. В случае последней отсутствуют такие клинические проявления АИО, как ощущение "песка", инъецированность конъюнктивы, покраснение и отечность периорбитальных тканей, сонографические признаки увеличения объема ретробульбарной клетчатки, глазодвигательных мышц. Проведение офтальмологического осмотра обычно позволяет четко верифицировать диагноз высокой степени миопии.
Псевдоэкзофтальм конституционального генеза , наблюдаемый у лиц с широкой глазной щелью, дифференцируют с АИО на основании отсутствия воспалительных признаков АИО, фотофобии, слезотечения, ощущения инородного тела, инъецированности конъюнктивы, отека и покраснения периорбитальных тканей, наличия диплопии, глазных симптомов (Штелльвага, Еллинека, Грефе, Кохера и ряда аналогичных).
Уточнить диагноз позволяют анамнестические данные - отсутствие изменений выстояния глазных яблок с детского возраста (помогает изучение фотографий прошлых лет), отсутствие сопутствующих аутоиммунных болезней щитовидной железы, отсутствие признаков АИО при офтальмологическом и сонографическом осмотре.
Экзофтальм как следствие орбитальных целлюлитов исключается у больных АИО на основании офтальмологического осмотра и сонографии орбит.
Экзофтальм опухолевого генеза , который чаще бывает односторонним, дифференцируют с асимметричным выстоянием глазных яблок при АИО . Верификации диагноза помогает проведение сонографии орбит либо КТ орбит, в ряде случаев - КТ черепа. Данные методы исследования позволяют подтвердить либо исключить опухолевый генез экзофтальма (первичные гемангиомы и саркомы орбиты; менингиомы и карциномы с прогрессирующим ростом в направлении глазницы; орбитальные метастазы карцином бронхов, опухолей молочных желез).
Двусторонний экзофтальм, обусловленный двусторонними артериовенозными аневризмами пещеристых пазух , дифференцируют с АИО на основании отсутствия клинических признаков АИО и наличия данных Rh-графии и компьютерной томографии черепа, подтверждающих локализацию двусторонних артериовенозных аневризм, исходящих из пещеристых пазух.
Реже приходится проводить дифференциальную диагностику АИО с экзофтальмом при врожденных аномалиях черепа (краниостеноз), костном ксантоматозе (болезнь Хенда - Шюллера - Крисчена), с синдромом Мёбиуса , который наследуется по аутосомно-рецессивному типу и характеризуется врожденной двусторонней офтальмоплегией, лицевой диплегией, полиневропатическим компонентом, аномалиями развития костной системы (дизрафический статус), ожирением.
Лечение. Выбор схемы терапии больных с АИО зависит от того, сочетается ли данное заболевание с другой аутоиммунной патологией-болезнью Грейвса, тиреоидитом Хасимото, наблюдается ли тиреотоксикоз либо гипотиреоз, какова тяжесть офтальмопатии и выраженность симптомов воспаления.
В течении АИО можно выделить периоды обострения и спонтанных ремиссий, захватывающие от 3 мес до 3 лет (М. P. Mourits, 1990). Менее чем у 10 % больных развивается тяжелая глазная симптоматика АИО. В 50 % случаев ретракция век исчезает при коррекции тиреотоксикоза. Часто временны и дисфункции экстраокулярных мышц. Проптоз глазных яблок, однажды достигнув своего максимума, обычно имеет тенденцию оставаться мало измененным. Вовлечение зрительного нерва в патологический процесс порой сложно предотвратить, несмотря на то что пациенты с риском развития нейропатии могут быть выявлены методами, позволяющими оценить объем экстраокулярных мышц.
Нет единой схемы лечения АИО, оптимальной для всех случаев заболевания, однако можно выделить основные общепринятые принципы терапии и коррекции, базирующиеся на следующих положениях: у больных с АИО необходимо достигать эутиреоидного состояния и поддерживать его в течение всей болезни; воспалительный компонент АИО должен быть ликвидирован первично до хирургических реконструктивных операций; хирургическую реконструкцию при АИО необходимо выполнять в четко определенной последовательности.
- Коррекция тиреоидной функции
[показать]
При наличии признаков нарушения функции щитовидной железы проводят ее коррекцию:
- коррекция тиреотоксикоза у больных диффузным токсическим зобом, сочетающимся с аутоиммунной офтальмопатией.
В начале лечения применяются оптимальные терапевтические дозы, которые постепенно снижаются под контролем клинических симптомов и уровней Т3 и Т4 в крови (табл. 8).
Производные имидазола (тиамазол, метимазол, карбимазол) блокируют синтез Т3 и Т4 на уровне йодированных тирозинов, что приводит к снижению циркулирующих в крови тиреоидных гормонов и способствует уменьшению симптомов тиреотоксикоза.
Критериями для снижения дозы являются: нормализация массы тела, стабилизация артериального давления, ликвидация вегетативных реакций. Лечение поддерживающей дозой проводится не менее 12-18 мес, так как ранняя отмена препарата неизбежно приводит к рецидиву ДТЗ. При назначении мерказолила либо других производных имидазола возможно развитие лейкопении, поэтому необходимо 1 раз в 7-14 дней контролировать общий анализ крови. Кроме того, возможны тошнота, кожная сыпь, боли в суставах. При развитии побочных явлений уменьшают дозу мерказолила или прекращают дальнейший прием препарата. Бесконтрольное лечение мерказолилом может привести к развитию медикаментозного гипотиреоза, который обычно подтверждается результатами теста с тиролиберином. Медикаментозный гипотиреоз сопровождается компенсаторным ростом щитовидной железы ("струмогенное" действие мерказолила) или прогрессированием офтальмопатии. Своевременное снижение дозы мерказолила, включение в схему терапии левотироксина (50-100 мкг) позволяют избежать этих нежелательных эффектов.
Для лечения ДТЗ в случаях непереносимости перечисленных выше препаратов может быть использован карбонат лития. Препараты лития снижают синтез тиреоидных гормонов на стадии образования йодтиронинов и влияют на периферический метаболизм тиреоидных гормонов, увеличивая соотношение Т4: Т3 (в связи с повышением Т4 и снижением Т3). Карбонат лития назначают по 0,3 г 2-3 раза в день. Побочные явления выражаются в чувстве усталости, сонливости, жажде, диплопии, нарушениях сердечного ритма. Появление указанных симптомов свидетельствует о передозировке препарата, что требует перерыва в лечении на несколько дней с последующим уменьшением дозы. Длительность лечения карбонатом лития не должна превышать 6 мес.
Комплексная терапия ДТЗ включает применение блокаторов бета-адренергических рецепторов. Блокада β-адренергических рецепторов приводит к уменьшению проявлений тиреотоксикоза (урежение частоты сердечных сокращений, снижение артериального давления). Кроме того, β-адреноблокаторы влияют на внетиреоидный метаболизм Т4, уменьшая образование из него Т3 и повышая образование малоактивной гормональной формы - реверсивного Т3 (обратный Т3). Непосредственно на функцию щитовидной железы эти препараты не влияют, поэтому целесообразно использовать их одновременно с тиреостатическими препаратами. Средняя доза β-адреноблокаторов (анаприлин, обзидан, тразикор) - 40-120 мг/сут. Начинают терапию с дозы 60-80 мг/сут, увеличивая ее до необходимой, под контролем пульса и артериального давления. После достижения эутиреоидного состояния доза постепенно снижается. Продолжительность лечения - от 6 до 12 мес. Величина поддерживающей дозы колеблется от 20 до 40 мг/сут. Следует помнить, что на фоне лечебной дозы адреноблокаторов частота сердечных сокращений не может служить критерием компенсации ДТЗ.
В дополнение к тиреостатикам и блокаторам бета-адренергических рецепторов применяют гормоны щитовидной железы (тиреотом, левотироксин) для профилактики медикаментозного гипотиреоза, сопровождающегося увеличением размеров щитовидной железы. Доза тиреоидных гормонов устанавливается индивидуально.
- Коррекция повышенной функции щитовидной железы у больных аутоиммунным тиреоидитом, сочетающимся с аутоиммунной офтальмопатией.
Проявления гиперфункции щитовидной железы при аутоиммунном тиреоидите - от легких явлений гипертиреоза до симптомокомплекса тиреотоксикоза - легко ликвидируются небольшими дозами тиреостатических препаратов (10-15 мг мерказолила либо тиамазола) за сравнительно короткий промежуток времени - 1-3 нед.
Параллельно в схему тиреостатической терапии можно вводить небольшие дозы β-адреноблокаторов (40-60 мг обзидана и т. д.). В случае использования глюкокортикоидов при лечении аутоиммунного тиреоидита, сочетающегося с аутоиммунной офтальмопатией, доза производных имидазола (мерказолила, тиамазола, карбимазола) может еще более снижаться (5 мг/сут) - вплоть до полной отмены вследствие потенцирования тиреостатического эффекта.
При лечении больных аутоиммунным тиреоидитом принимают во внимание волнообразный характер этого заболевания (чередование состояний гипертиреоза, эутиреоза и гипотиреоза - особенно в начале болезни), возможность быстрого возврата симптомов гиперфункции щитовидной железы после респираторных инфекций и т. д., провоцирующих клинико-иммунологическую декомпенсацию.
В случае развития гипертиреоза у больного с аутоиммунным тиреоидитом, помимо тиреостатической терапии, сохраняют прием L-тироксина в небольших дозах (25- 50 мкг), учитывая его иммуномодулирующее и антиструмогенное действие.
- Коррекция гипотиреоза.
Проводится тиреоидными синтетическими гормонами (L-тироксин, трийодтиронин, тиреотом), которые устраняют клинико-метаболические проявления симптомокомплекса гипотиреоза. Средние дозы заместительной терапии - от 75 до 150 мкг/сут. У пожилых больных начинают лечение с малых доз - 25-50 мкг/сут. Каждые 3-5 дней дозу увеличивают, доводя ее до оптимальной, позволяющей поддерживать эутиреоидное состояние. Адекватность дозы тиреоидных гормонов оценивается по исчезновению клинической симптоматики гипотиреоза, нормализации уровней тироксина, трийодтиронина и тиротропина, биохимических параметров крови (липидограммы, протеинограммы).
- Иммуносупрессивная терапия
[показать]
Кортикостероиды широко используются в лечении АИО для устранения симптомов воспаления и уменьшения орбитального отека, в том числе и при развитии невропатии зрительного нерва. Они наиболее эффективны на ранних стадиях заболевания до развития выраженного фиброза, однако их истинные механизмы действия при АИО до конца не ясны.
Используются следующие схемы приема преднизолона:
- преднизолон в дозе 60 мг/день в течение 2 нед; 40 мг/день - 2 нед; 30 мг/день - 4 нед и 20 мг/день - 4 нед;
- преднизолон в дозе 1,0-1,5 мг/кг веса по альтернирующей схеме через день в течение 4-6-8-12 нед. При необходимости схема продолжается до 48-52 нед.
В последние годы офтальмологические центры за рубежом, занимающиеся проблемой АИО, отказались от техники ретробульбарного введения глюкокортикоидов и других препаратов у больных с данной патологией.
Циклоспорин как препарат, ингибирующий иммунокомпетентные клетки, является альтернативой преднизолону, однако он также обладает целым рядом побочных эффектов. Начальная ежедневная доза циклоспорина - 7,5 мг на кг веса. Продолжительность терапии - 12 нед. Циклоспорин дается дважды в день в виде раствора (100 мг на 1 мл), который добавляется к молоку, соку, киселям. При повышении содержания креатинина в плазме крови более 150 ммоль/л на фоне терапевтических концентраций циклоспорина в крови (250-750 нг/мл) дозу препарата снижают либо переходят на прием глюкокортикоидов в дозе 60 мг/день в течение 2 нед, 40 мг - следующие 2 нед, 30 мг - 4 нед, 20 мг - 4 нед.
В некоторых случаях используется комбинированная терапия преднизолоном и циклоспорином. При начальной терапии глюкокортикоидами в течение 12 нед назначают циклоспорин в дозе 7,5 мг/кг веса в сочетании с преднизолоном 20 мг/день на следующие 12 нед.
Динамическое наблюдение за больным выполняет врач-офтальмолог (осмотры через 4, 6, и 12 нед монотерапии и через 4 и 12 нед комбинированной терапии). Продолжительность терапии при необходимости может быть увеличена до 52 нед и более. При этом выполняются сонография орбит, КТ орбит, контролируются биохимические параметры крови, содержание Т3, Т4, базальный ТТГ и ТТГ, стимулированный тиреотропин-рилизинг-гормоном (до лечения, через 12, 24 и 52 нед).
- Иммунокоррекция методами гравитационной хирургии
[показать]
Проводится при тяжелых формах АИО, особенно в случаях сочетания данного заболевания с другими аутоиммунными болезнями (болезнь Грейвса, тиреоидит Хасимото, претибиальная микседема, болезнь Аддисона, ИЗСД, ревматоидный артрит и т. д.).
Плазмаферез эффективен у больных в активной воспалительной фазе АИО и неэффективен при хронической непрогрессирующей АИО в состоянии клинико-иммунологической компенсации.
Проводятся 4 сеанса плазмафереза в течение 5-8 дней с удалением за сеанс 2 л плазмы и замещением этого объема донорской свежезамороженной плазмой и изотоническим раствором хлорида натрия. Концентрация циркулирующих иммунных комплексов, органоспецифических аутоантител уменьшается в среднем в 3 раза. Второй курс плазмафереза проводят при необходимости через 3-6 мес.
Плазмаферез обычно сочетается с иммуносупрессивной терапией глюкокортикоидами (1,0 мг/кг веса в сут) либо цитостатиками (азатиоприн, 100 мг/день, или циклоспорин 7,5 мг/кг веса в день) в течение 3 мес, так как в случае монолечения плазмаферезом обычно достигается только временный эффект на 1-2-й нед с последующим возобновлением активности болезни и нарастанием клинической симптоматики.
Из других методов гравитационной хирургии в клинике используется гемосорбция; апробируются различные схемы иммуносорбции.
- Иммуномиметическая терапия
[показать]
При изменениях в Т-клеточном звене иммунной системы проводится терапия иммуномиметиками под контролем иммунограммы: тималин (10 мг/день внутримышечно) N 5-10 каждый день либо через день на ночь; Т-активин (0,1 %-1,0 мл) подкожно по 1-2 мл на ночь N 5-7 каждый день либо через день.
Более мягкий иммуностимулирующий эффект оказывает дибазол - препарат из группы имидазола. Обладает свойствами адаптогена, стимулирует гликолиз, усиливает синтез белка и нуклеиновых кислот. Назначается по 0,3 мг 3 раза в день в течение мес.
Из "легких" иммуностимуляторов при АИО, сочетающейся с тиреоицной патологией, используются производные пирамидина (метилурацил, 0,5; пентоксил, 0,2 - 3-4 раза в день в течение 2-3 нед); нуклеинат натрия (по 0,75-1,5 г/сут 10-30 дней); спленин (внутримышечно, по 1,0-2,0 мл в течение 10 дней); витамины А и Е.
NB! Не существует такого понятия как "легкие" или "мягкие иммуностимуляторы". Есть препараты, воздействующие на то или иное звено иммунной системы с его стимуляцией или угнетением
- Облучение орбит
[показать]
Эффективность облучения орбит в целях уменьшения симптоматики АИО варьирует от 20 до 60 %. Часто комбинируется стероидная терапия с рентгеновским облучением орбит. Полагают, что данный метод лечения следует использовать при большей длительности АИО. Однако он нежелателен при наличии сопутствующей патологии - сахарного диабета (из-за ухудшения течения диабетической ретинопатии).
Суммарная доза, которая дается на область орбит, достигает 20 Гр (2000 рад). Обычно при такой дозе не наблюдается побочных эффектов (они возможны при ошибках в расчете доз или методике выполнения).
- Хирургическое лечение
[показать]
Экстренное хирургическое вмешательство у больных с АИО выполняется только в случае прогрессирующей невропатии зрительного нерва, не поддающейся консервативной терапии. Во всех остальных ситуациях корригирующие хирургические вмешательства откладываются до ликвидации активной фазы АИО.
Большинство орбитальных хирургов полагает, что оперативные вмешательства должны выполняться в такой последовательности: сначала декомпрессия орбит, затем коррекция диплопии и только потом - операция на веках.
Декомпрессия орбит проводится как в случае прогрессирующего падения зрения из-за компрессии зрительного нерва, так и у больных с выраженным экзофтальмом. Техника декомпрессии орбит постоянно совершенствуется, используются венечный, нижнемедиальный и боковые доступы.
- Местная терапия
[показать]
У больных с АИО для предотвращения развития кератита широко используются "искусственные слезы" и разнообразные глазные капли, гели, обладающие протективным действием.
У больных с незначительным проявлением АИО (фотофобия, слезотечение, ощущение инородного тела) часто бывает достаточно местной терапии глюкокортикоидами. Используются 0,5 % суспензия гидрокортизона, 0,1 % раствор дексаметазона.
В ряде случаев, помимо указанных основных (1-7) методов коррекции АИО, проводится терапия ферментными препаратами (урокиназа местно в виде аппликаций, инъекции лидазы подкожно); средствами, влияющими на метаболические процессы (инъекции пирацетама, солкосерила, ФиБС, АТФ) и микроциркуляцию (дицинон, этамзилат), препаратами, улучшающими венозный отток из орбиты (кавинтон), и т. д.
В отечественных клиниках используются физиотерапевтические методы лечения (магнитотерапия, лазеротерапия, трансорбитальный ионофорез глюкокортикоидов, аспирина и т. д.).
В схему лечения больных АИО с выраженным отеком периорбитальных тканей либо при начальных признаках компрессии зрительного нерва включаются диуретики (фуросемид, лазикс, гипотиазид, триампур, диакарб и т. д.) (схема).